-
1、将气体和按体积之比导入管式反应器(如图1)热解制 , 高于T℃下发生如下两个反应(反应过程用稀释):
Ⅰ:
Ⅱ:
在常压下反应相同时间后,不同温度下测得气体、及体积分数随温度的变化(如图2)。下列说法错误的是
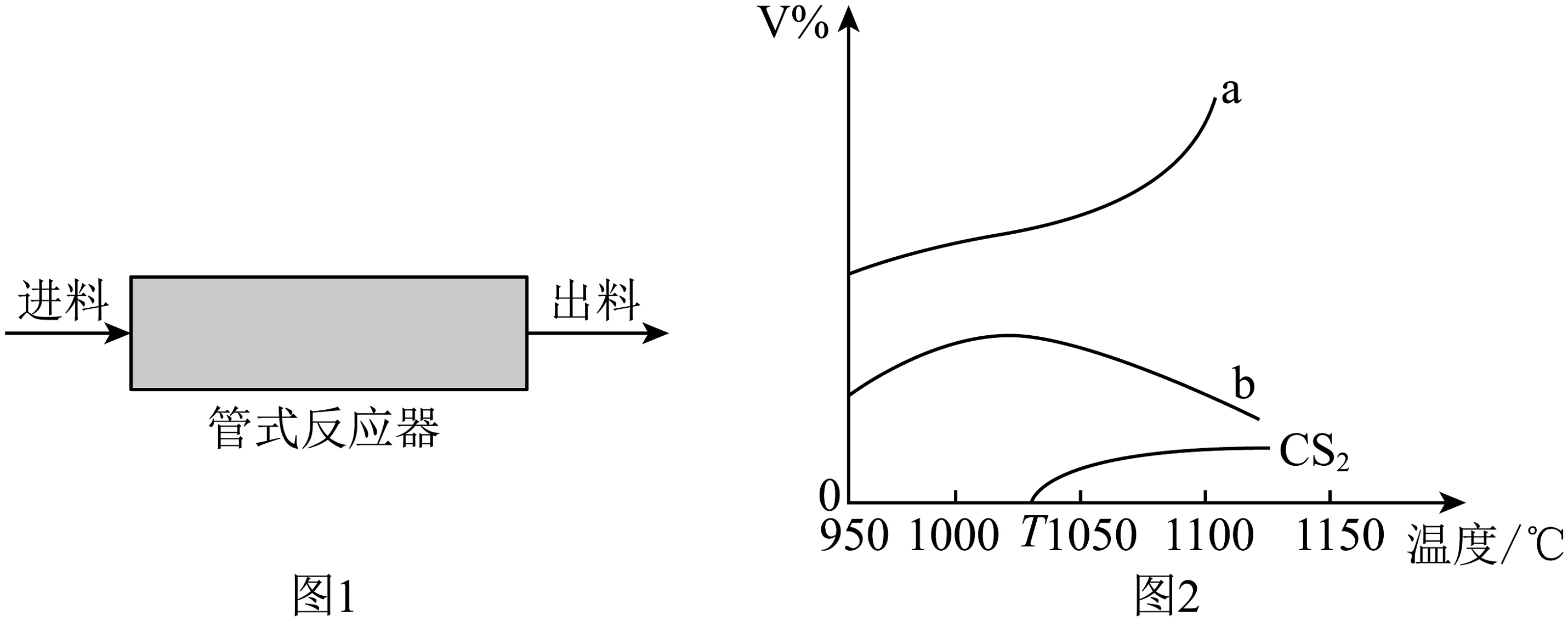 A、高于T℃,该体系总反应为: B、曲线b表示的体积分数随温度的变化 C、1000℃时,反应的活化能:反应Ⅰ<反应Ⅱ D、在1000℃、常压下,通入的体积分数保持不变,提高投料比 , 的转化率减小
A、高于T℃,该体系总反应为: B、曲线b表示的体积分数随温度的变化 C、1000℃时,反应的活化能:反应Ⅰ<反应Ⅱ D、在1000℃、常压下,通入的体积分数保持不变,提高投料比 , 的转化率减小 -
2、W、X、Y、Z、M为短周期主族元素,原子序数依次增大,分别位于三个不同短周期,最外层电子数之和为20。Z的最外层电子数与其K层电子数相等,是形成酸雨的物质之一。下列说法不正确的是A、熔点:ZY>ZM B、键角: C、热稳定性: D、分子的极性:
-
3、有机物A经元素分析仪测得有C、H、O三种元素组成,A的质谱、红外光谱、核磁共振氢谱图如下所示。下列关于A的说法不正确的是
 A、所有的原子可能在同一个平面上 B、能与溶液反应放出 C、能发生银镜反应 D、能与酸性溶液反应
A、所有的原子可能在同一个平面上 B、能与溶液反应放出 C、能发生银镜反应 D、能与酸性溶液反应 -
4、下列方程式正确的是A、碳酸钠溶液中通入少量二氧化硫: B、氢氧化铁溶于氢碘酸中: C、乙酰胺在足量盐酸中发生水解反应: D、铜片上电镀银的总反应(银作阳极,硝酸银溶液作电镀液):
-
5、物质微观结构决定宏观性质,进而影响用途。下列结构或性质不能解释其用途的是
选项
结构或性质
用途
A
金刚石中的碳采取杂化轨道形成共价键三维骨架结构
金刚石可用作地质钻探材料
B
铝是活泼金属,常温下表面易形成致密的氧化膜
用铝粉可通过铝热反应制备金属镁
C
聚乳酸(
 )中含有酯基
)中含有酯基聚乳酸可用于制备可降解塑料
D
1-丁基-3-甲基咪唑六氟磷酸盐(
 )由体积较大的阴、阳离子组成的离子液体,有良好的导电性
)由体积较大的阴、阳离子组成的离子液体,有良好的导电性1-丁基-3-甲基咪唑六氟磷酸盐可被开发为原电池的电解质
A、A B、B C、C D、D -
6、反应 , 下列说法不正确的是A、中S的价态为 B、是氧化产物 C、氧化剂和还原剂的物质的量之比是 D、若消耗时,则反应转移的电子数为(表示阿伏加德罗常数的值)
-
7、化学与人类社会可持续发展息息相关。下列说法正确的是A、用碳原子取代晶体硅中的部分硅原子,可增强晶体的导电性 B、煤的干馏可以得到焦炭、煤油、出炉煤气等主要产品 C、生铁的硬度大,抗压性强,可用于铸造机器底座 D、味精的主要成分是谷氨酸,添加味精可增加食品的鲜味
-
8、利用下列装置和试剂进行实验,下图能达到实验目的的是
 A、图①可用于实验室制 B、图②可用于熔化固体烧碱 C、图③可用于除去中的HCl D、图④可用于向容量瓶转移溶液
A、图①可用于实验室制 B、图②可用于熔化固体烧碱 C、图③可用于除去中的HCl D、图④可用于向容量瓶转移溶液 -
9、下列表示不正确的是A、分子的球棍模型:
 B、HCl中共价键的电子云图:
B、HCl中共价键的电子云图: C、甲基的电子式:
C、甲基的电子式: D、2,3-二甲基丁烷的键线式:
D、2,3-二甲基丁烷的键线式:
-
10、物质的性质决定用途。下列说法正确的是A、具有漂白性,葡萄酒中添加起到漂白作用 B、溶液具有酸性,可用于腐蚀覆铜板制作印刷电路板 C、具有强氧化性,可清洗附在试管内壁的银镜 D、维生素C具有氧化性,可用于水果罐头的抗还原剂
-
11、按物质组成分类,下列物质属于碱的是A、CH3OH B、Cu2(OH)2CO3 C、LiOH D、HCOOH
-
12、已知:A(g)+2B(g)3C(g) ΔH<0,向一恒温恒容的密闭容器中充入1 mol A和2 mol B发生反应,t1时达到平衡状态I,在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
 A、t2时改变的条件:向容器中加入A B、平衡时B的体积分数φ:φ(II)=φ(I) C、t2~ t3时反应向正方向移动 D、平衡时A(g)的物质的量浓度:c(I)>c(II)
A、t2时改变的条件:向容器中加入A B、平衡时B的体积分数φ:φ(II)=φ(I) C、t2~ t3时反应向正方向移动 D、平衡时A(g)的物质的量浓度:c(I)>c(II) -
13、四氧化三锰()是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)为原料制备高纯的工艺流程如图所示。

25℃时,相关金属离子[]形成氢氧化物沉淀的pH范围如下表,当离子浓度小于时,则认为该离子沉淀完全了。
金属离子
开始沉淀的pH
8.1
6.3
1.5
8.9
6.2
6.9
沉淀完全的pH
10.1
8.3
2.8
10.9
8.2
8.9
回答下列问题:
(1)、“氧化”步骤的主要目的是。(2)、“调pH”时溶液的pH范围应调节为4.7~6.2之间,据此可以得知:的。(3)、“滤渣3”中主要有。(4)、写出“沉锰”时的离子方程式:。(5)、在“沉锰”时,可以额外添加适量氨水促进生成碳酸锰,请你从化学平衡移动的角度解释加入氨水的目的:。(6)、Mn和O可以组成多种氧化物,其中一种氧化物的晶胞如图所示。
①该晶体中Mn的配位数为。
②已知阿伏加德罗常数的值为 , 该晶体的密度(用含a、b的代数式表示)。
-
14、二氧化氯()是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。回答下列问题:(1)、的制备:制备的常用方法有两种,分别为法、与反应法。
①法制备的原理为 , X的化学式为 , 将通入溶液中,有红褐色沉淀生成,溶液中的主要阴离子为、 , 若消耗 , 则被氧化的为。
②与反应法制备 , 生成物只有两种,参加反应的与物质的量之比为 , 与法相比,与反应法的优点是(填一条)。
(2)、的用途:除毒、除异味。①可以将剧毒的氰化物氧化成和 , 离子方程式为 , 属于(填“酸”“碱”或“两”)性氧化物,每转移 , 生成L(标准状况下)。
②能把水溶液中有异味的氧化成四价锰,使之形成不溶于水的 , 该反应的离子方程式为。
-
15、A、B、C、D、E为前20号的元素,原子序数逐渐增大。A元素的原子价层电子排布式为;A与C处于同一周期,其中C的第一电离能比同周期相邻元素的小;D、E元素的基态原子都只有一个未成对电子,其中D的电子有9种空间运动状态。下列说法正确的是A、简单氢化物键角: B、简单离子半径: C、同周期元素第一电离能小于C的有4种 D、A与D形成的化合物和C与E形成的化合物中不可能含有非极性共价键
-
16、下图是铜及部分含铜粒子的价荷图。下列推断不合理的是
 A、在酸性环境中,变成需要加氧化剂 B、转化成需要加碱 C、如果将高铜酸根离子()填入坐标,应该填在的位置 D、在酸性环境中,可以歧化成和
A、在酸性环境中,变成需要加氧化剂 B、转化成需要加碱 C、如果将高铜酸根离子()填入坐标,应该填在的位置 D、在酸性环境中,可以歧化成和 -
17、设为阿伏加德罗常数的值。下列说法不正确的是A、溶液与NaOH溶液等体积混合并加热,产生氨气的分子数为 B、标准状况下,和的混合气体总体积约为22.4L C、常温常压下,2.8gCO和的混合气体中含有的分子数为 D、与足量水完全反应,转移的电子数为
-
18、是制备有机合成的重要还原剂的反应物,氢化锂遇水蒸气剧烈反应。某小组设计如图装置制备。下列说法不正确的是
 A、装置中可通过控制盐酸的滴加速度来控制氢气的生成速率 B、装置B,C可依次盛装饱和食盐水、浓硫酸 C、装置E用于吸收尾气,避免污染环境 D、实验中,先通入 , 后点燃酒精灯
A、装置中可通过控制盐酸的滴加速度来控制氢气的生成速率 B、装置B,C可依次盛装饱和食盐水、浓硫酸 C、装置E用于吸收尾气,避免污染环境 D、实验中,先通入 , 后点燃酒精灯 -
19、马来酸(结构如图)常作食品饮料的添加剂、酸味剂。下列叙述错误的是

已知:马来酸的酸性比碳酸强。
A、马来酸有顺、反异构体 B、1mol马来酸含9molσ键 C、1mol马来酸最多能消耗 D、马来酸能使溴水、酸性溶液褪色 -
20、劳动成就梦想。下列劳动项目与所述化学知识关联不正确的是
选项
劳动项目
化学知识
A
学农活动:帮果农向储果仓库中放置酸性高锰酸钾溶液浸泡过的砖块以保鲜水果
乙烯能与酸性高锰酸钾溶液反应
B
社区服务:用白醋除去社区老年活动中心水壶中的水垢
白醋可溶解碳酸钙等沉淀
C
家务劳动:制作豆腐
胶体能发生丁达尔效应
D
志愿活动:用过氧乙酸消毒液给图书馆桌椅消毒
过氧乙酸消毒液具有强氧化性
A、A B、B C、C D、D