-
1、项目学习小组围绕铁生锈相关问题展开探究。(1)、任务一:初探铁生锈的条件
查阅资料:铁锈的主要成分是
提出猜想:基于的元素组成变化,提出铁生锈所需条件的猜想。
猜想1:只需要
猜想2:只需要
猜想3:需要和设计实验:基于猜想,分别设计实验方案如下图。将猜想与实验方案连线。
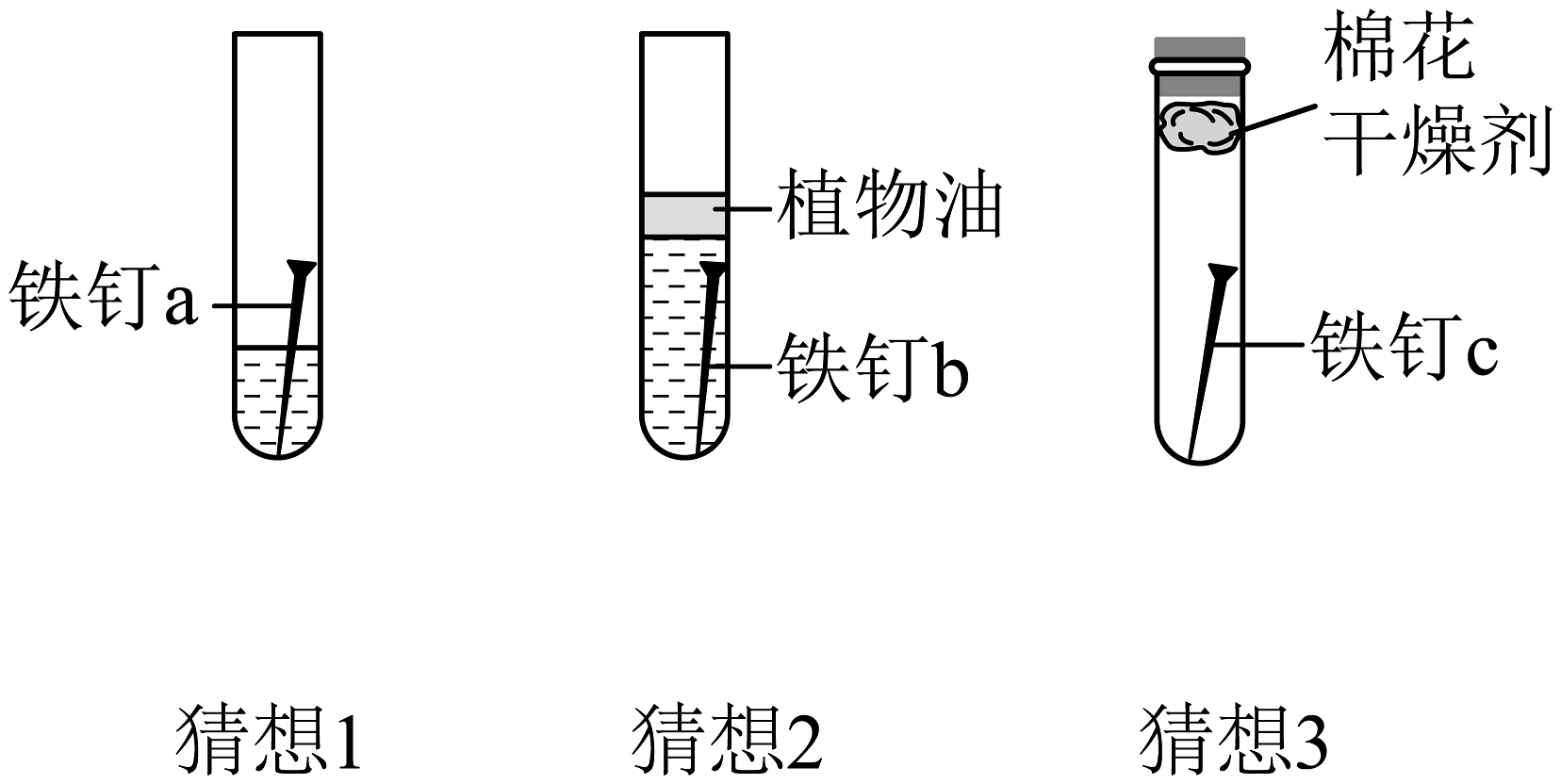
实验结论:一周后只有铁钉a生锈,即猜想成立。
反思讨论:图中植物油的作用是。
提出新问题:铁先与反应再和反应,还是与二者同时反应?
(2)、任务二:再探铁生锈的条件查阅资料:向铁粉中掺入少量炭粉,可较快观察到铁生锈。
设计实验:学习小组在老师指导下用氧气传感器设计实验如图。
进行实验:得到集气瓶中含量随时间变化的图像如图,则100s时进行的操作是。

实验结论:铁与和同时反应并生成铁锈。
(3)、任务三:再探铁生锈的正面应用补充实验:将氧气传感器换成温度传感器重复任务二中操作,100s后温度明显上升。说明铁生锈(填“吸热”或“放热”)。
客观评价:铁生锈亦有其独特的正面价值。如月饼包装袋中用铁粉做双吸剂(吸收和),起到和防腐的双重作用。
拓展应用:另举一例生活中铁生锈的正面应用。
-
2、完成下列实验(1)、任务一:的实验室制取
i.选用制取 , 化学方程式为。用图1中仪器组装发生装置,应选择E,还需补充的仪器是(填名称)。
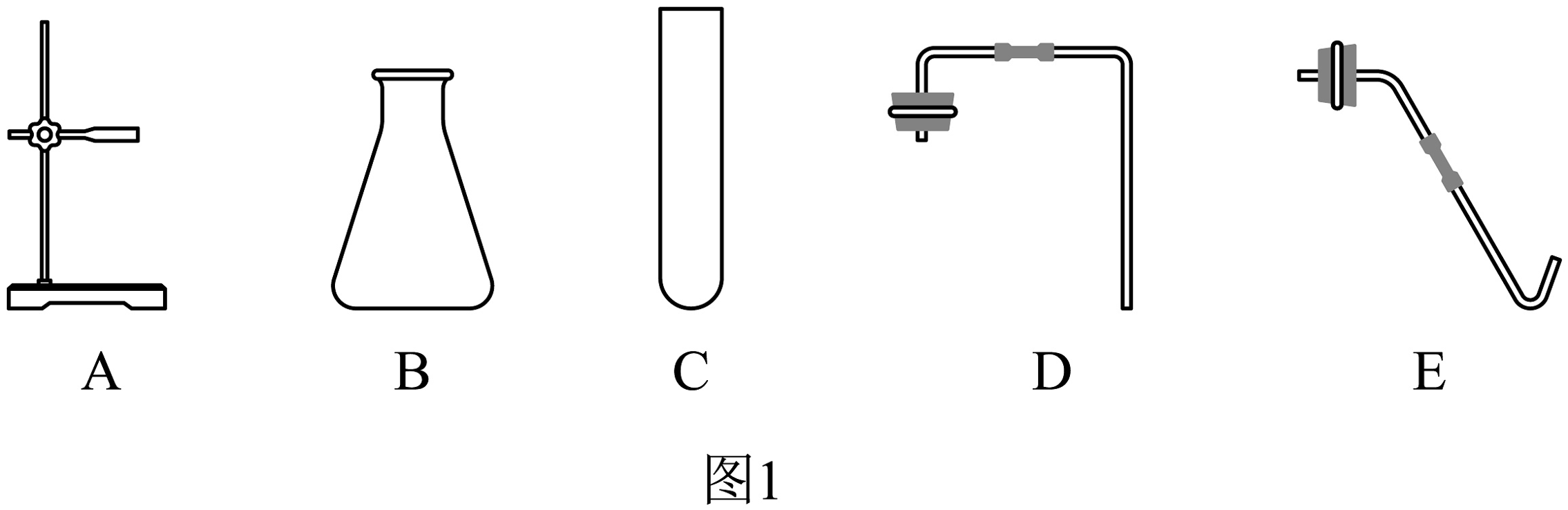
ii.检查气密性,松手后出现图2所示现象,说明该装置气密性。

iii.在图3中将收集过程的微观示意图补画完整(忽略水的蒸发)。
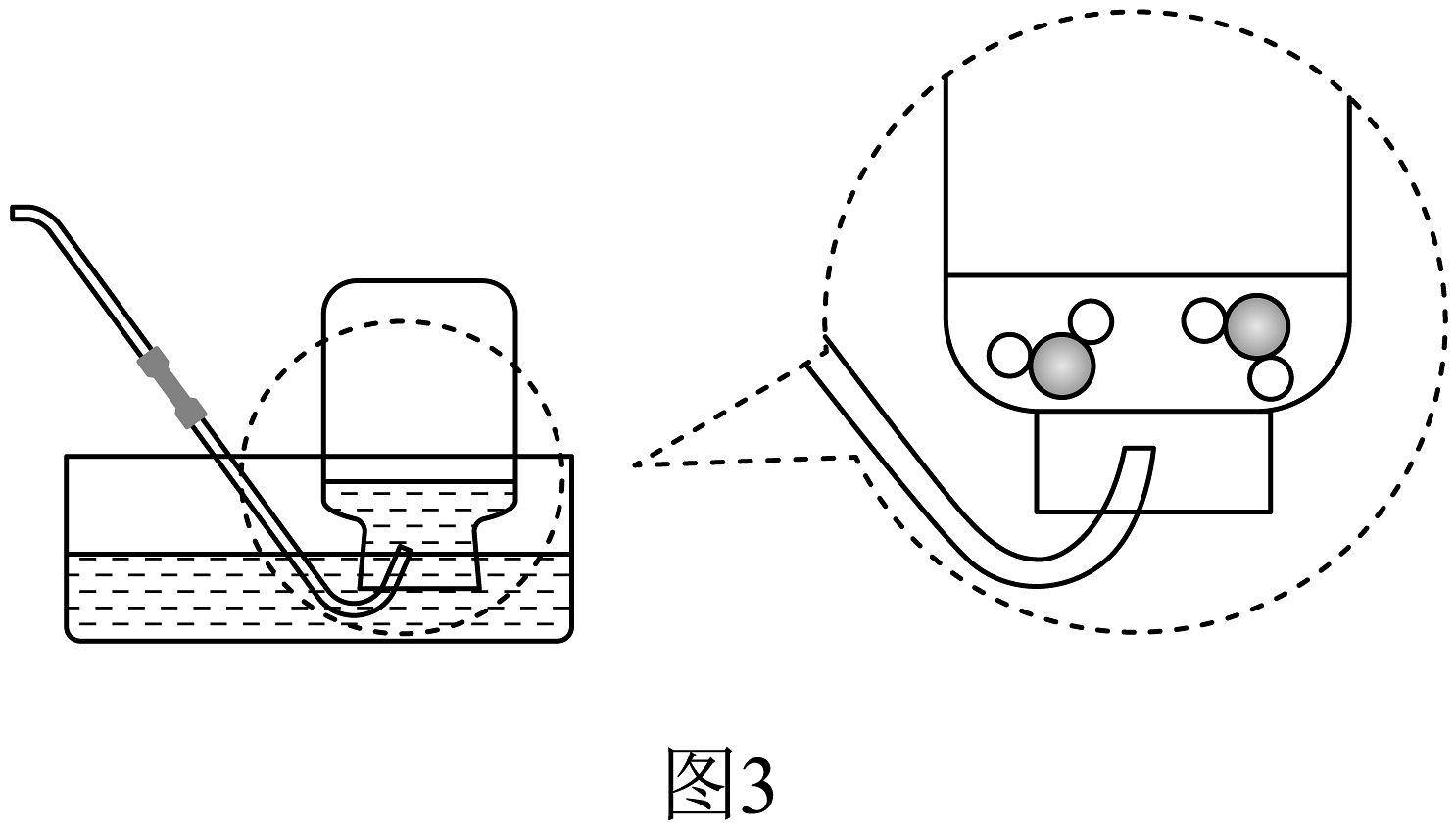 (2)、任务二:制作酸雨危害演示装置
(2)、任务二:制作酸雨危害演示装置项目学习小组利用塑料瓶和洗发水瓶等生活物品,设计制作如下装置并进行探究。
操作
现象
分析与结论

硫在空气中燃烧,(填字母),生成刺激性气味的气体a.发出白光b.发出淡蓝色火焰c.放出热量
基于环保考虑,装置可优化的一处是
燃烧结束,不断按压洗发水瓶的泵头
右侧吸管口有水喷出,大理石表面有气泡产生,一段时间后叶子变黄
溶于水后与作用生成 , 化学方程式为
-
3、同学们对干冰肯定不陌生,但你知道还有“干水”吗?干水由水和二氧化硅()组成,呈白色粉末状。拿到手上不会弄湿手,因为每颗水滴都被疏水性的纳米包围,不能聚集变大。

将纳米和水放入搅拌机中搅拌几分钟即可制得干水(如图),制备成本低且应用前景大。相同时间内干水捕获的是普通水的3倍多。干水还能快速吸收甲烷,为使用天然气的汽车提供动力。在青海、甘肃等缺水地区,埋在土壤中的干水可持续给树苗供水3个月以上。
依据上文,回答问题。
(1)、制备干水时发生的是变化(填“物理”或“化学”)。(2)、干水中水的质量分数为 , 其捕获的化学方程式为。(3)、干水可用于缺水地区抗旱造林的主要原因是。(4)、下列说法正确的是(不定项)。a.干冰、干水都是纯净物 b.纳米易溶于水
c.用力挤压干水,可能弄湿手 d.气体溶解度因溶剂分散尺度不同可能改变
-
4、“火地”是故宫中一种地下供热系统,由操作口、炉腔及烟道组成,结构剖面如图。炉腔上方置生铁架以增强支撑力,承受地砖及室内家具之重量。通过操作口向炉腔添加炭火,燃烧产生的热量沿烟道向四周扩散以加热地砖。
 (1)、“火地”系统将能转化为热能。(2)、生铁属于材料,具有较强承重能力是因为相较于纯金属,它的强度更高、硬度更。(3)、炉腔位于最低处及烟道呈坡面上升的设计是考虑到燃烧放热,烟道内空气 , 易于热量迅速扩散。(4)、故宫取暖用“红萝炭”,由山中硬木烧制而成,该过程属于(填“完全”或“不完全”)燃烧。红萝炭“气暖而耐久,灰白而不爆”,品质上乘,用其燃烧供热的化学方程式为。
(1)、“火地”系统将能转化为热能。(2)、生铁属于材料,具有较强承重能力是因为相较于纯金属,它的强度更高、硬度更。(3)、炉腔位于最低处及烟道呈坡面上升的设计是考虑到燃烧放热,烟道内空气 , 易于热量迅速扩散。(4)、故宫取暖用“红萝炭”,由山中硬木烧制而成,该过程属于(填“完全”或“不完全”)燃烧。红萝炭“气暖而耐久,灰白而不爆”,品质上乘,用其燃烧供热的化学方程式为。 -
5、控制变量是科学探究时的常用思想。下列设计应用了该思想的是


A.探究质量守恒定律
B.探究不同催化剂催化分解效果


C.探究温度对分子运动速率的影响
D.探究铁与锌的金属活动性
A、A B、B C、C D、D -
6、利用物质性质差异,可以对其进行鉴别、检验和除杂。下列实验设计合理的是
选项
实验目的
试剂或材料
A
鉴别:和
燃着的木条
B
检验:中是否含有
澄清石灰水
C
检验:溶液是否变质
足量稀盐酸
D
除杂:溶液中少量
足量铁粉
A、A B、B C、C D、D -
7、项目学习小组制作“天气瓶”。步骤如下:①将少量樟脑溶于适量酒精得溶液(樟脑难溶于水);②将和溶于水得溶液;③将、混合、加热、搅拌至澄清,冷却至室温装瓶。下列说法错误的是

 A、溶液中溶剂为酒精 B、溶液中的质量分数为 C、降温过程较先析出晶体 D、相同物质在不同溶剂中溶解性不同
A、溶液中溶剂为酒精 B、溶液中的质量分数为 C、降温过程较先析出晶体 D、相同物质在不同溶剂中溶解性不同 -
8、下列跨学科实践活动中所涉及的化学知识正确的是
选项
实践活动
化学知识
A
垃圾分类与回收利用
废报纸和易拉罐均为可回收垃圾
B
水质检测及自制简易净水器
活性炭起杀菌消毒的作用
C
探究土壤酸碱性对植物生长的影响
所测土壤越大,酸性越强
D
用微型空气质量“检测站”检测污染物
臭氧不属于空气污染物
A、A B、B C、C D、D -
9、甲烷与在催化作用下可得到合成气(和)。反应时催化剂表面同时存在积碳和消碳反应,如图。下列说法正确的是
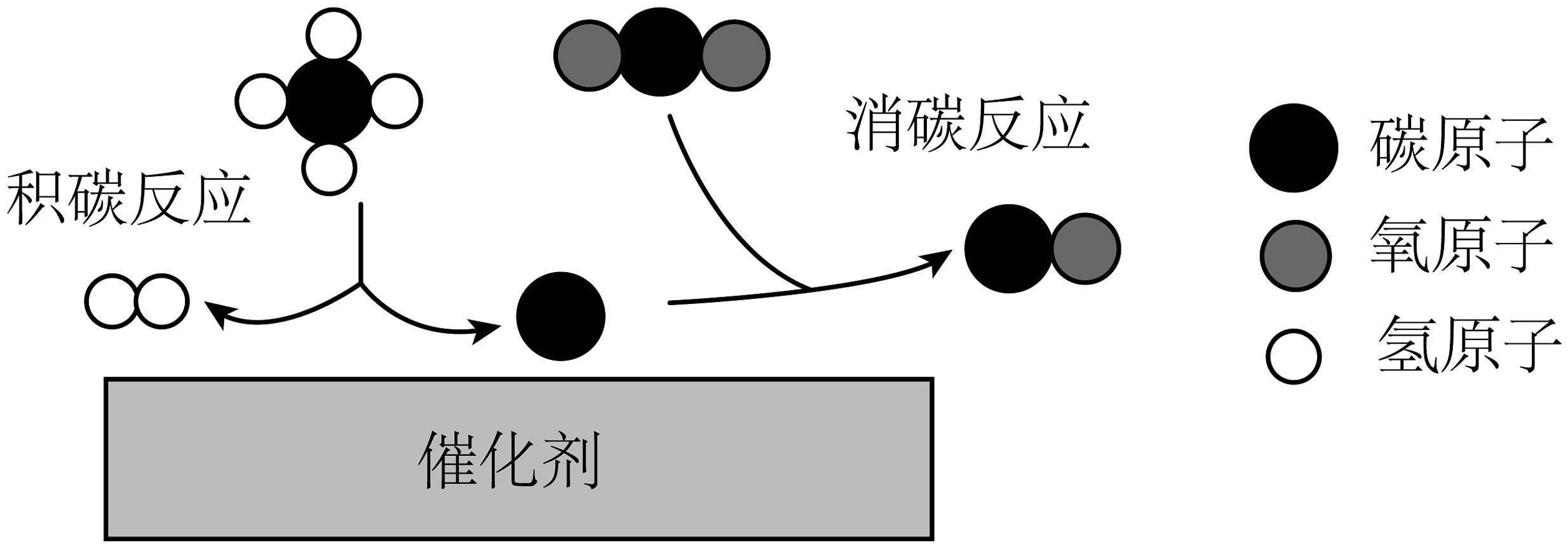 A、图中涉及的氧化物有3种 B、积碳反应为: C、为减少积碳,可加入稍过量的 D、反应结束若催化剂表面仍有积碳,则合成气中比多
A、图中涉及的氧化物有3种 B、积碳反应为: C、为减少积碳,可加入稍过量的 D、反应结束若催化剂表面仍有积碳,则合成气中比多 -
10、兴趣小组做“浮沉鸡蛋”家庭实验,现象如图。下列说法正确的是
 A、碳酸钙属于酸 B、鸡蛋表面的气泡是 C、鸡蛋上浮时所受浮力小于重力 D、实验结束玻璃杯中溶质只含有
A、碳酸钙属于酸 B、鸡蛋表面的气泡是 C、鸡蛋上浮时所受浮力小于重力 D、实验结束玻璃杯中溶质只含有 -
11、消防喷淋头及其结构如图。当喷淋头附近温度升高到设定值时,热敏球内的丙三醇()会将外层玻璃胀破,喷淋头自动喷水灭火。回答下列小题。
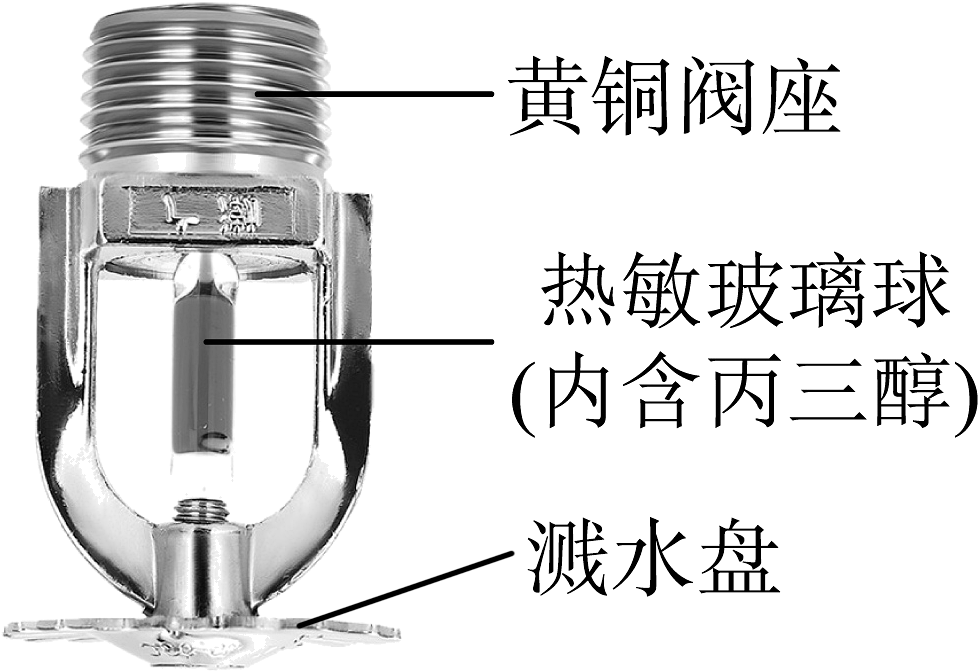 (1)、阀座使用黄铜材质(铜锌合金),下列有关黄铜的说法错误的是A、熔点较纯铜更高 B、与纯铜受热时都会变黑 C、能与稀硫酸反应 D、能承受一定的水流压力(2)、下列有关丙三醇的说法正确的是A、分子中含4个 B、由碳氢氧3种元素组成 C、碳、氢元素质量比为 D、碳元素的质量分数最小(3)、下列有关喷淋头的说法正确的是A、应安装在远离燃气灶的位置 B、灭火原理是喷水降低可燃物着火点 C、热敏球胀破是因受热时丙三醇分子间隔减小 D、溅水盘的作用是改变水流形状,增大喷淋面积
(1)、阀座使用黄铜材质(铜锌合金),下列有关黄铜的说法错误的是A、熔点较纯铜更高 B、与纯铜受热时都会变黑 C、能与稀硫酸反应 D、能承受一定的水流压力(2)、下列有关丙三醇的说法正确的是A、分子中含4个 B、由碳氢氧3种元素组成 C、碳、氢元素质量比为 D、碳元素的质量分数最小(3)、下列有关喷淋头的说法正确的是A、应安装在远离燃气灶的位置 B、灭火原理是喷水降低可燃物着火点 C、热敏球胀破是因受热时丙三醇分子间隔减小 D、溅水盘的作用是改变水流形状,增大喷淋面积 -
12、《中华人民共和国粮食安全保障法》明确国家建立粮食储备应急保障机制,以提高应对突发事件的能力。下列说法错误的是A、粮食的呼吸作用属于缓慢氧化 B、为提高粮食产量,应大量施用化肥 C、粮仓设计应密封、隔热、防潮 D、粮仓中充入氮气可延长粮食保质期
-
13、准备过滤器时,折好滤纸并放入漏斗,用少量水将其润湿。下列错误的是
 A、A B、B C、C D、D
A、A B、B C、C D、D -
14、1960年闵恩泽研制出小球硅铝裂化催化剂,确保了我国国防航空燃油的稳定供给。硅、铝元素在元素周期表中的信息如图。下列说法错误的是
 A、硅属于非金属元素 B、硅原子质子数为14 C、铝元素的相对原子质量为 D、铝和氧气反应,Al失去最外层3个电子
A、硅属于非金属元素 B、硅原子质子数为14 C、铝元素的相对原子质量为 D、铝和氧气反应,Al失去最外层3个电子 -
15、化学用语是学习和研究化学时通用的简洁语言。下列化学用语表示正确的是
2个氯原子:
2个氨分子:
1个镁离子:
碳酸钠:
A
B
C
D
A、A B、B C、C D、D -
16、科学家将水蒸气通过烧红的铁制枪管,得到“易燃空气”和黑色固体 , 证明水不是一种元素。完成下面小题。(1)、成功揭秘“水的组成”的科学家是A、拉瓦锡 B、卡文迪什 C、普里斯特利 D、阿伏加德罗(2)、上述反应的基本反应类型是A、化合反应 B、分解反应 C、置换反应 D、复分解反应
-
17、下列有关空气的说法正确的是A、空气中氮气、氧气等分子均匀地混合在一起 B、空气中氧气的体积分数最大 C、空气中氧气的化学性质不活泼 D、空气是由空气分子组成的
-
18、
露天焚烧垃圾,会对空气造成污染。某兴趣小组在实验室采用相对封闭的装置内燃烧某种含碳、氢、氧元素的垃圾,对产生的废气成分按如图所示的装置进行检验。
【查阅资料】①浓硫酸是一种常见的干燥剂。②无水硫酸铜为白色固体,遇水会变蓝色。
【提出猜想】
(1)经讨论,某小组同学认为该气体可能含有CO2、CO、H2O中的一种或几种。猜想的理论依据是________。
【实验装置】

【进行实验】拉动注射器,让废气依次通过装置。
【实验现象】
(2)A中的实验现象为________;D中的实验现象为________;B、E中澄清石灰水变浑浊。
【实验结论】废气中存在CO2、CO、H2O。
【反思评价】
(3)写出装置B中发生反应的化学方程式________。
(4)装置F处的大号注射器,除了可以引导气体流向,其另一个主要作用是________。
(5)下列可以区分二氧化碳和一氧化碳的是___________。
A. 澄清的石灰水 B. 灼热的氧化铜 C. 燃着的木条 D. 紫色石蕊溶液 (6)装置A、B是否能够交换________(填“能”或“不能”),请说出你的理由________。
-
19、如图是实验室制取气体的常用装置,请回答下列问题:
 (1)、仪器a的名称为。(2)、实验室制取二氧化碳的方程式是 , 为了随时控制反应的发生或停止,发生装置应选用(填字母)。(3)、用A装置制取O2的方程式为 , 若用E装置收集的氧气不纯,写出一种可能的原因。(4)、通常情况下,SO2是一种无色有刺激性气味的气体,密度比空气大,易溶于水。实验室里,用亚硫酸钠固体和浓硫酸反应制取SO2。则实验室制取SO2选择的发生装置是(填字母),若选择D装置收集SO2 , 气体应该从(填“b”或“c”)口进入。
(1)、仪器a的名称为。(2)、实验室制取二氧化碳的方程式是 , 为了随时控制反应的发生或停止,发生装置应选用(填字母)。(3)、用A装置制取O2的方程式为 , 若用E装置收集的氧气不纯,写出一种可能的原因。(4)、通常情况下,SO2是一种无色有刺激性气味的气体,密度比空气大,易溶于水。实验室里,用亚硫酸钠固体和浓硫酸反应制取SO2。则实验室制取SO2选择的发生装置是(填字母),若选择D装置收集SO2 , 气体应该从(填“b”或“c”)口进入。 -
20、A、B、C、D、E是初中化学常见的物质,常温下A、B、C都为无色气体,且A为单质,B有毒性,D、E都为黑色粉末,且D为化合物。物质间的转化关系如图所示(“—”表示相邻的两种物质间能发生反应,“→”表示两种物质间的转化关系,部分反应物、生成物及反应条件已略去)。请回答下列问题。
 (1)、B的化学式为。写出B物质的一种用途。(2)、A与B的反应属于反应(填基本反应类型)。(3)、B与D反应的化学方程式为。(4)、E→B的反应过程中一定放出热量,此说法( )(填“正确”或“错误”)。
(1)、B的化学式为。写出B物质的一种用途。(2)、A与B的反应属于反应(填基本反应类型)。(3)、B与D反应的化学方程式为。(4)、E→B的反应过程中一定放出热量,此说法( )(填“正确”或“错误”)。