相关试卷
-
1、深中通道的建设推动了粤港澳大湾区城市群融合发展。下列说法不正确的是A、沉管隧道对接使用的定位芯片的主要成分为 B、悬索桥主缆使用的钢丝的硬度比纯铁的大 C、桥面铺装使用的沥青可通过石油分馏获得 D、供电系统使用的太阳能电池工作时将电能转化为化学能
-
2、中国古代器皿暗藏无尽雕塑韵律之美。下列器皿主要由天然有机高分子材料制成的是




A.西周青铜盉
B.西汉玉角杯
C.元朝银槎杯
D.明朝竹根雕杯
A、A B、B C、C D、D -
3、靶向药物能够识别肿瘤细胞的特征性位点,杀灭肿瘤细胞效果好,且毒副作用小。靶向药物M的结构简式如图所示。下列说法不正确的是
 A、M的分子式为 B、M分子中含有3种官能团 C、碳原子杂化方式均为 D、1molM最多可与3molNaOH发生反应
A、M的分子式为 B、M分子中含有3种官能团 C、碳原子杂化方式均为 D、1molM最多可与3molNaOH发生反应 -
4、燕赵大地历史悠久,文化灿烂。下列有关博物馆馆藏文物的说法错误的是A、石质浮雕的主要成分是碳酸钙,碳酸钙属于钙盐 B、透雕白玉壁的主要成分是硅酸盐,常温下,易溶于水 C、青花釉里红瓷盖罐的主要成分是硅酸盐,硅酸钠的电离方程式为 D、青铜铺首的主要成分是铜锡合金,直径为50nm的铜粉形成的分散系,可产生丁达尔效应
-
5、某种可用于治疗心脏病的药物x的结构简式为
 , 下列有关X的说法正确的是 A、X的分子式是C14H24O2 B、X能溶于水,密度比水大 C、X遇酸或碱溶液都会变质 D、X是乙酸乙酯的同系物,可能有香味
, 下列有关X的说法正确的是 A、X的分子式是C14H24O2 B、X能溶于水,密度比水大 C、X遇酸或碱溶液都会变质 D、X是乙酸乙酯的同系物,可能有香味 -
6、下列方案设计、现象和结论都正确的是
编号
实验目的
方案设计
现象与结论
A
比较与的酸性强弱
分别测、两饱和溶液的
溶液小,则酸性
B
验证溶液中存在水解平衡
往含有酚酞溶液中加入少量晶体
溶液红色变浅,则溶液中存在水解平衡
C
比较与的大小
向足量溶液中先加入少量溶液,再加入溶液
先生成白色沉淀,再生成淡黄色沉淀,则
D
探究压强对化学平衡的影响
快速压缩装有、平衡混合气体的针筒活塞
平衡后气体颜色变深,则增大压强,平衡向生成的方向移动
A、A B、B C、C D、D -
7、502胶水是一种强力粘胶剂,其主要成分的结构为
 。下列有关说法正确的是 A、分子式为C6H8O2N B、含有碳碳双键、氰基和酯基三种官能团 C、分子中所有原子可能都共面 D、在微量水汽催化下发生缩聚反应固化粘着
。下列有关说法正确的是 A、分子式为C6H8O2N B、含有碳碳双键、氰基和酯基三种官能团 C、分子中所有原子可能都共面 D、在微量水汽催化下发生缩聚反应固化粘着 -
8、MgCO3和CaCO3的能量关系如图所示(M=Ca、Mg):

已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是
A、ΔH1(MgCO3)>ΔH1(CaCO3)>0 B、ΔH2(MgCO3)=ΔH2(CaCO3)>0 C、ΔH1(CaCO3)-ΔH1(MgCO3)=ΔH3(CaO)-ΔH3(MgO) D、对于MgCO3和CaCO3 , ΔH1+ΔH2>ΔH3 -
9、某同学用下列装置进行有关Cl2的实验。下列说法不正确的是
 A、Ⅰ图中:实验现象证明氯气无漂白作用,氯水有漂白作用 B、Ⅱ图中:闻Cl2的气味 C、Ⅲ图中:生成棕黄色的烟 D、Ⅳ图中:若气球干瘪,证明Cl2可与NaOH反应
A、Ⅰ图中:实验现象证明氯气无漂白作用,氯水有漂白作用 B、Ⅱ图中:闻Cl2的气味 C、Ⅲ图中:生成棕黄色的烟 D、Ⅳ图中:若气球干瘪,证明Cl2可与NaOH反应 -
10、有机太阳能电池利用有机半导体将光能转换为电能。科学家设计了一种新型有机太阳能电池材料,其部分合成路线如下:
 (1)、化合物ii的含氧官能团名称是 , 化合物iii的分子式是。(2)、化合物i的同分异构体中,能发生水解反应的芳香化合物的结构简式为。(3)、根据化合物vi的结构特征,分析预测其可能的化学性质,完成下表。
(1)、化合物ii的含氧官能团名称是 , 化合物iii的分子式是。(2)、化合物i的同分异构体中,能发生水解反应的芳香化合物的结构简式为。(3)、根据化合物vi的结构特征,分析预测其可能的化学性质,完成下表。序号
结构特征
反应试剂、条件
反应形成的新结构
反应类型
a
b
,
取代反应
(4)、由化合物生成化合物iv涉及以下转化过程(未注明反应条件),下列有关叙述正确的有___________。 A、反应②是消去反应 B、反应③中,有C-O键的断裂和生成 C、化合物x中,碳原子均采取杂化 D、化合物ix是手性分子,含有2个手性碳原子(5)、化合物v(
A、反应②是消去反应 B、反应③中,有C-O键的断裂和生成 C、化合物x中,碳原子均采取杂化 D、化合物ix是手性分子,含有2个手性碳原子(5)、化合物v( )可通过频哪醇()和联硼酸[]的脱水反应制备,频哪醇的结构简式是。 (6)、以第(4)问中化合物ii转化为化合物iv的原理为依据,设计以<>
)可通过频哪醇()和联硼酸[]的脱水反应制备,频哪醇的结构简式是。 (6)、以第(4)问中化合物ii转化为化合物iv的原理为依据,设计以<> 和化合物iii(
和化合物iii( )为原料合成化合物xi。
)为原料合成化合物xi。
基于你设计的合成路线,回答下列问题:
(a)最后一步反应中,有机反应物为(写结构简式)。
(b)第一步的化学方程式为(注明反应条件)。
-
11、铜及其合金是人类最早使用的金属材料,铜的化合物在现代生活和生产中有着广泛的应用。(1)、基态铜原子的价电子排布式是。(2)、铜和钙都是金属晶体,铜的熔点比钙的高,其原因是。(3)、如图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为。
 (4)、科学家通过X射线推测,胆矾的结构如下图所示。
(4)、科学家通过X射线推测,胆矾的结构如下图所示。
①胆矾的阳离子中心原子的配位数为 ,
胆矾的化学式用配合物的形式可表示为;
②具有对称的空间构型,中的两个被两个取代,能得到两种不同结构的产物,则的中心离子与配体形成的空间构型是。
A.三角锥形 B.正四面体 C.平面正方形 D.四角锥形
(5)、Cu与Cl构成晶体的晶胞结构如下图所示,该晶体组成的最简式为 , 已知该晶体的密度为4.14g/cm3 , 则该晶胞的边长为pm(列计算式,设为阿伏加德罗常数的值)。若将该物质气化后实验测定其蒸汽的相对分子质量为199,则其气体的分子式为。
-
12、
硼是一种用途广泛的化工原料矿物,主要用于生产硼砂、硼酸和硼的各种化合物。回答下列问题:
I.一种比事光声探针M与配位,可用于小鼠脑内铜(II)的高时空分辨率动态成像。反应如下所示:

已知:“
 ”表示的化学键伸向纸面外,“
”表示的化学键伸向纸面外,“ ”表示的化学键伸向纸面内。
”表示的化学键伸向纸面内。(1)H、C、N、F四种元素电负性由大到小的顺序为________,M中F-B-F键角________中F-B-F键角(填“>”、“<”或“=”)。
II.B的简单氢化物不能游离存在,常倾向于形成较稳定的或与其他分子结合。
(2)分子结构如图,则B原子的杂化方式为________。

Ⅲ.硼酸在电子器件工业和医疗上有重要用途。硼酸是一种片层状结构的白色晶体,层内结构如下图所示:

(3)加热时,硼酸在水中的溶解度增大,主要原因是________。
(4)硼酸在水中电离产生过程为: , 是___________酸。
A. 一元强酸 B. 一元弱酸 C. 三元强酸 D. 三元弱酸 Ⅳ.硼砂是含结晶水的四硼酸钠,请根据模型回答有关问题。
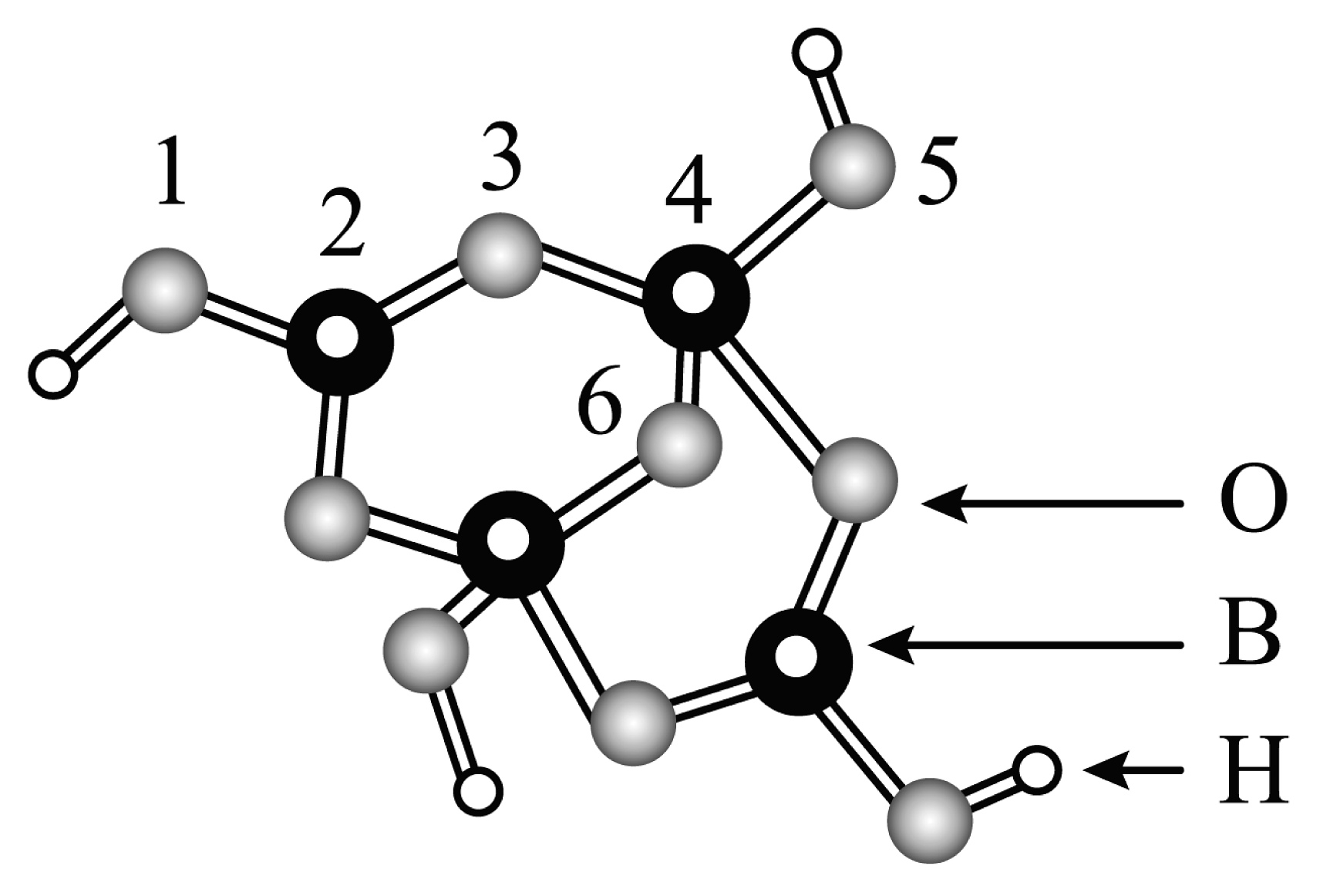
(5)硼砂中阴离子(含B、O,H三种元素)的球棍模型如图所示,则在中,2号硼原子的价层电子对数为________,m=________(填数字)。
(6)和过量NaF作用可生成 , 的空间构型为________,的电子式为________。
-
13、
1,2-二溴乙烷可作汽油抗爆剂的添加剂。某小组同学设想通过乙烯与溴水反应进行制备。已知部分有机化合物的数据如下:
物质
乙醇
1,2-二溴乙烷
2-溴乙醇
溶解性
与水任意比互溶
难溶于水
与水互溶
沸点/℃
78.5
132
149
熔点/℃
-117.3
9
-80
I.乙烯的制备
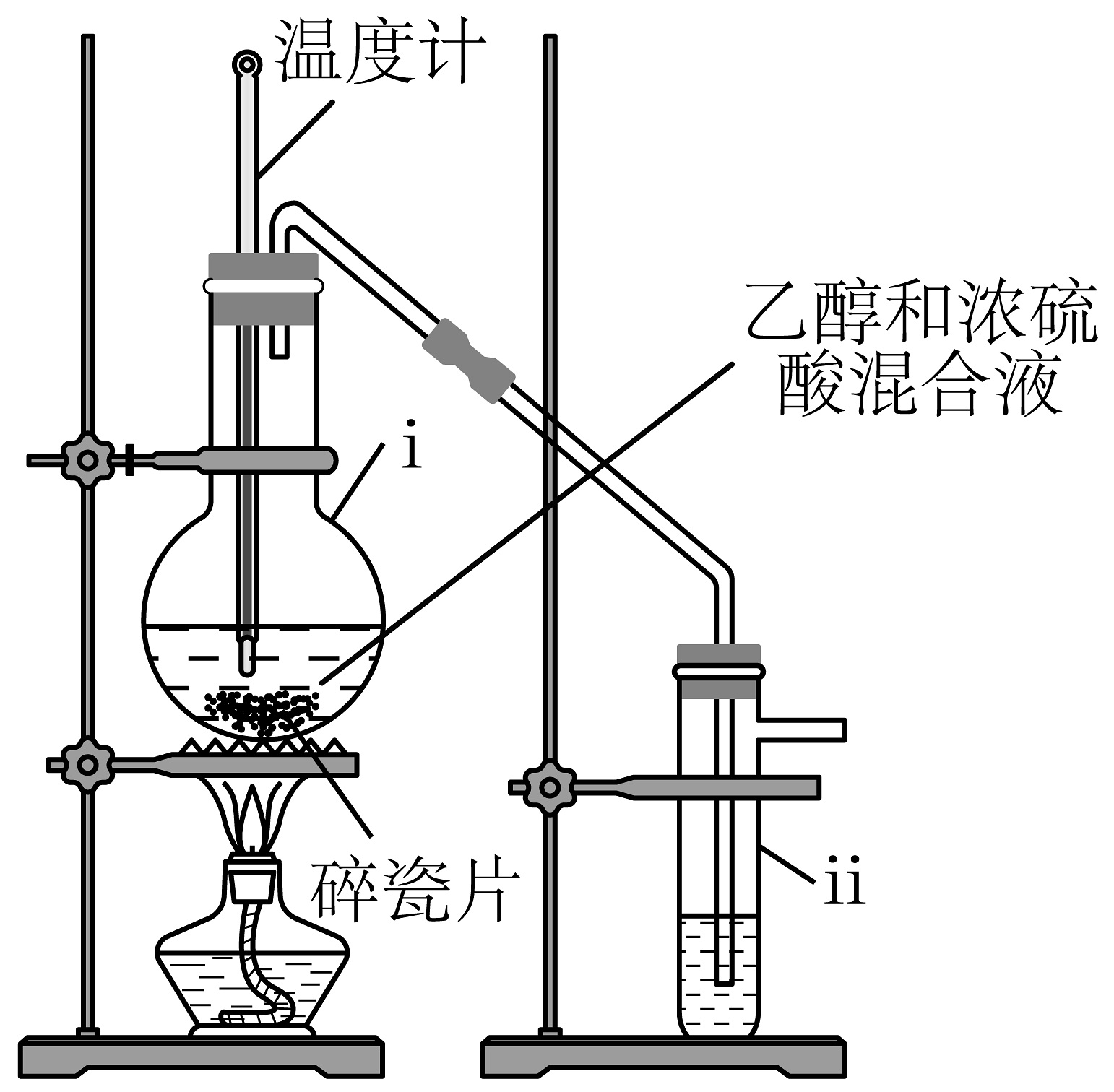
(1)仪器i的名称为;制备乙烯的化学方程式为。
(2)仪器ii的作用是除去乙烯中的和等杂质,应盛放的试剂为。
Ⅱ.1,2-二溴乙烷的制备
(3)仪器iii中是已知浓度与pH的溴水,向其中通入足量已除杂的乙烯气体,充分反应后再测定iii中溶液的pH。

预期实验现象:溴水褪色,溶液的pH变大,溶液分层。
预期产品分离方法:将仪器得到的混合物进行(填分离操作)。
(4)仪器iv中NaOH溶液的作用:。
Ⅲ.探究乙烯与溴水的反应原理
(5)如步骤Ⅱ进行实验,反应后实际观察的现象:澳水褪色,溶液的pH变小,溶液没有明显的分层现象。
查阅资料乙烯与反应生成1,2-二溴乙烷的机理如下图所示:

根据实际观察的现象,结合反应机理,写出乙烯与溴水反应的化学方程式:。
(6)实验结论
结合(5)中现象和机理,实验室制备1,2-二溴乙烷时应在无水环境中进行,可将乙烯气体通入。
(7)写出乙烯在生产生活中的一种应用。
-
14、实验室用乙酸、异戊醇、浓硫酸制备乙酸异戊酯(沸点142℃),并利用环己烷-水的共佛体系(沸点69℃)带出水分。已知体系中沸点最低的有机物是环己烷(沸点81℃),实验装置如图(夹持和水浴加热装置略去)。下列说法不正确的是
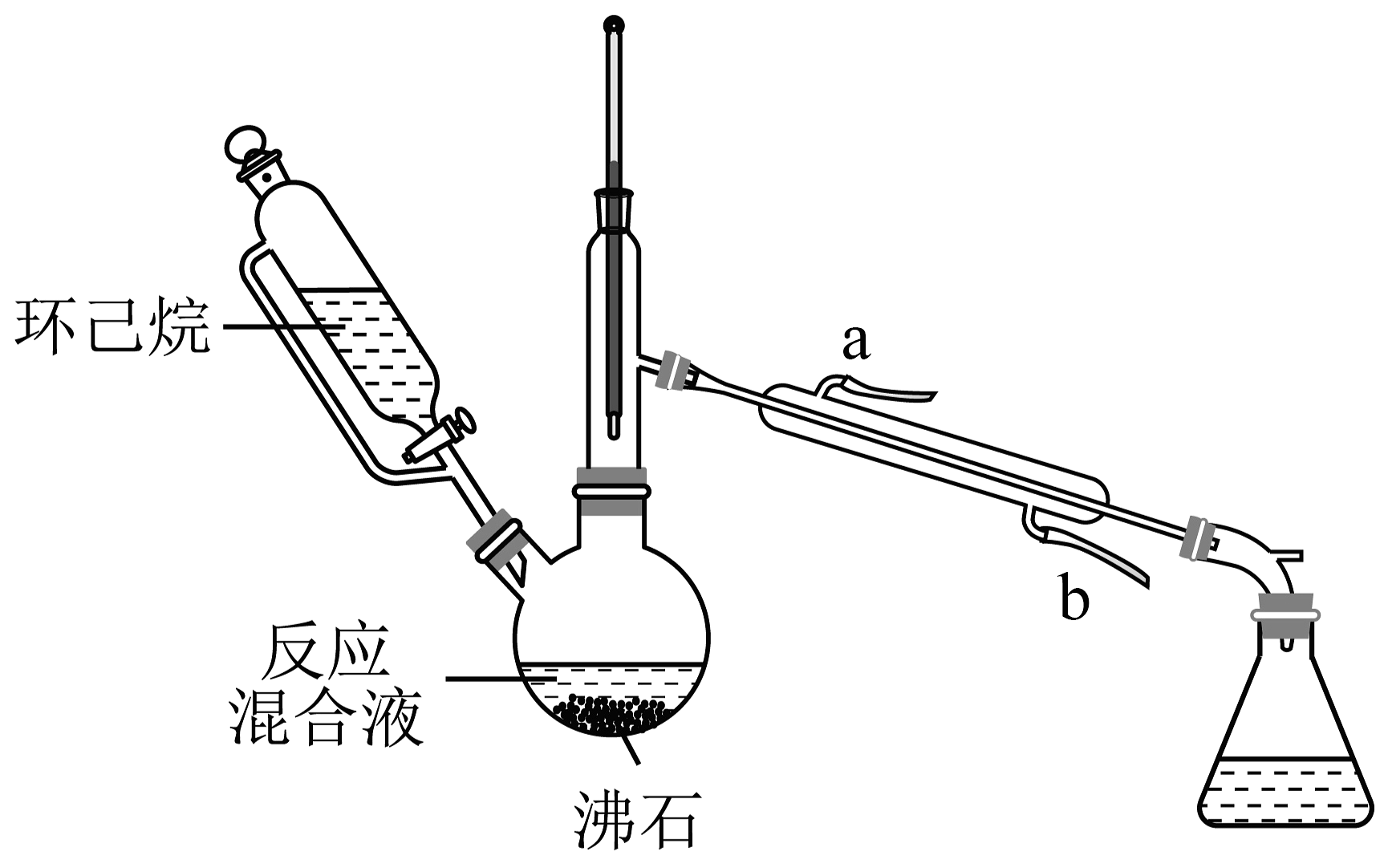 A、以共沸体系带水促使反应正向进行 B、冷凝水从b口进a口出 C、接收瓶中会出现分层现象 D、反应时水浴温度必须控制在69℃
A、以共沸体系带水促使反应正向进行 B、冷凝水从b口进a口出 C、接收瓶中会出现分层现象 D、反应时水浴温度必须控制在69℃ -
15、已知的熔点是890℃,的熔点是190℃,气态常以二聚体形式存在,其结构如下图所示。下列有关说法正确的是
 A、溶于水能导电,故为离子晶体 B、二聚体分子结构中存在配位键 C、二聚体中所有原子均在同一平面 D、和的二者熔点差异大是因为可形成分子间氢键
A、溶于水能导电,故为离子晶体 B、二聚体分子结构中存在配位键 C、二聚体中所有原子均在同一平面 D、和的二者熔点差异大是因为可形成分子间氢键 -
16、如图为甲烷晶体的晶胞结构,下列有关说法不正确的是
 A、晶体熔化时破坏了共价键 B、一个甲烷晶胞中含有4个甲烷分子 C、甲烷晶胞中的每个球体代表一个甲烷分子 D、晶体中1个甲烷分子周围有12个紧邻的甲烷分子
A、晶体熔化时破坏了共价键 B、一个甲烷晶胞中含有4个甲烷分子 C、甲烷晶胞中的每个球体代表一个甲烷分子 D、晶体中1个甲烷分子周围有12个紧邻的甲烷分子 -
17、利用有机分子模拟生物体内“醛缩酶”催化Diels-Alder反应取得重要进展,荣获2021年诺贝尔化学奖。某Diels-Alder反应以1为原料合成V,催化机理如下。下列说法错误的是
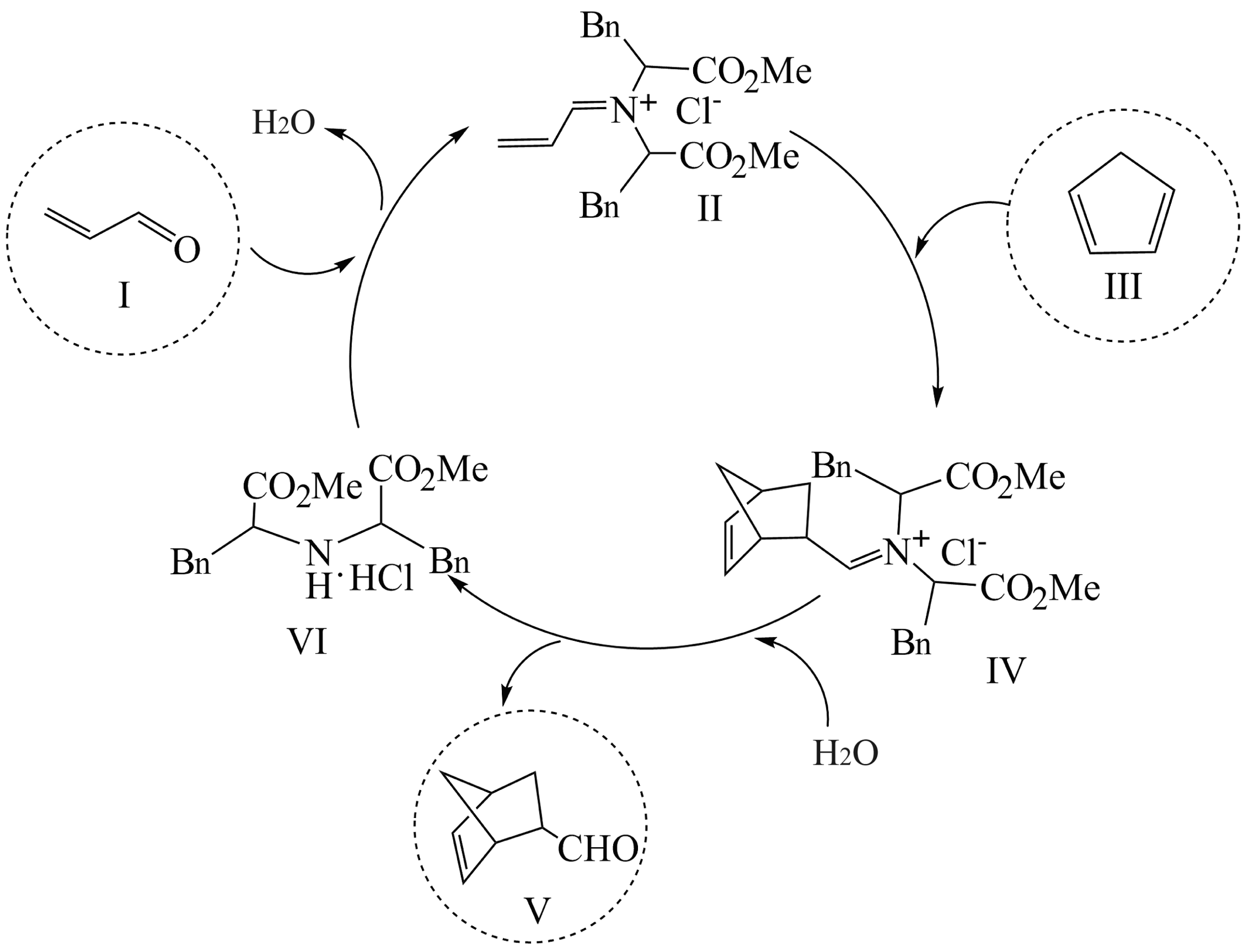 A、V的分子式为 B、总反应是:I+Ⅲ→V C、I和V互为同系物 D、Ⅵ是反应的催化剂
A、V的分子式为 B、总反应是:I+Ⅲ→V C、I和V互为同系物 D、Ⅵ是反应的催化剂 -
18、一种在航空航天、国防军工等领域具有应用前景的液晶聚芳酯G可由如下反应制备,下列说法错误的是
 A、 , 化合物X为乙酸 B、化合物E的核磁共振氢谱上共有4种H C、反应说明化合物F可发生缩聚反应 D、聚芳酯G可与NaOH溶液反应
A、 , 化合物X为乙酸 B、化合物E的核磁共振氢谱上共有4种H C、反应说明化合物F可发生缩聚反应 D、聚芳酯G可与NaOH溶液反应 -
19、下列关于实验操作与预期的现象及结论描述不合理的是
选项
实验操作
预期现象及结论
A
往盛有1mL溴乙烷的试管中滴入2滴溶液
产生浅黄色沉淀,说明溴乙烷在水中能电离出
B
向新制的中滴入少量葡萄糖溶液并加热
产生砖红色沉淀,说明葡萄糖含醛基
C
将少量乙酸乙酯加入NaOH溶液中,加热
出现分层,加热一段时间后酯层消失,说明乙酸乙酯可在碱性条件下水解
D
向盛有2mL鸡蛋清溶液的试管中加入5滴浓硝酸,加热
产生白色沉淀,加热后沉淀变黄色,说明鸡蛋清的蛋白质含有苯环
A、A B、B C、C D、D -
20、已知某多肽分子结构如图,下列说法正确的是
 A、该多肽可发生取代反应 B、该多肽含4个肽键,为四肽 C、该多肽水解后可得到5种氨基酸 D、1mol该多肽最多能与2molNaOH反应
A、该多肽可发生取代反应 B、该多肽含4个肽键,为四肽 C、该多肽水解后可得到5种氨基酸 D、1mol该多肽最多能与2molNaOH反应