相关试卷
-
1、一种补充微量元素的食品添加剂的结构式如图所示,W、X、Y、Z、Q的核电荷数依次增大,X、Y、Z同周期,Q的价层电子排布式为。下列说法不正确的是
 A、沸点: B、此结构中存在配位键 C、第一电离能:X<Y<Z D、和的空间结构均为平面三角形
A、沸点: B、此结构中存在配位键 C、第一电离能:X<Y<Z D、和的空间结构均为平面三角形 -
2、设为阿伏加德罗常数的值。下列说法正确的是A、1mol苯中含有3个π键 B、1L 1mol/L的苯酚钠溶液中含个 C、与反应生成22.4L , 转移的电子数为2 D、1mol 与混合物中含碳原子数为2
-
3、某研究性学习小组欲检验浓硫酸与蔗糖反应的产物,设计如下图所示装置(部分夹持装置已略)。下列说法不正确的是
 A、Ⅰ中蒸发皿内的白色固体变黑,体现了浓硫酸的脱水性 B、Ⅱ中溶液褪色,证明产物中有 C、Ⅲ中溶液快速变为无色且Ⅳ中产生沉淀,证明产物中有 D、Ⅴ中溶液可吸收尾气,防止污染环境
A、Ⅰ中蒸发皿内的白色固体变黑,体现了浓硫酸的脱水性 B、Ⅱ中溶液褪色,证明产物中有 C、Ⅲ中溶液快速变为无色且Ⅳ中产生沉淀,证明产物中有 D、Ⅴ中溶液可吸收尾气,防止污染环境 -
4、下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
选项
陈述Ⅰ
陈述Ⅱ
A
沸点:
 大于
大于
 存在氢键,
存在氢键, 不存在氢键
不存在氢键B
NaCl能使蛋白质变性
NaCl可用作食品防腐剂
C
键键能比键高
的沸点比高
D
对X射线透过率低且难溶于酸
医学上常用作X射线检查的内服药剂
A、A B、B C、C D、D -
5、新颖的曲面屏手机和折叠屏手机采用OLED显示技术,OLED是有机发光二极管的简称,如图有机物可用作OLED显示屏的发光材料。下列关于该有机物说法正确的是
 A、属于芳香烃 B、分子式为 C、分子中所有原子共面 D、分子中的碳原子均采用杂化
A、属于芳香烃 B、分子式为 C、分子中所有原子共面 D、分子中的碳原子均采用杂化 -
6、合成氨是人类科学技术发展史上一项重大成就。某兴趣小组利用以下装置进行氨气相关实验,其中难以达到预期目的的是


A.制备
B.干燥


C.收集
D.验证的溶解性
A、A B、B C、C D、D -
7、劳动铸就辉煌,汗水谱写华章。下列劳动项目与所述化学知识没有关联的是
选项
劳动项目
化学知识
A
环保工程师:监测大气中二氧化硫的浓度
二氧化硫有漂白性,可用于杀菌消毒
B
科研工作者:探索石墨转化成金刚石的条件
C
电池研发员:研发丙烷燃料电池
电池总反应:
D
营养师:建议炖排骨时加入适量的醋
醋酸可以溶解骨头中的含钙物质,利于人体吸收钙元素
A、A B、B C、C D、D -
8、提纯粗溴苯(含少量溴和苯)的过程如下。其中,操作X为
 A、冷却结晶 B、分液 C、蒸馏 D、过滤
A、冷却结晶 B、分液 C、蒸馏 D、过滤 -
9、中科院牵头研制的新概念潜水器——“鹿岭号”深海多位点着陆器,使用了镁,海水燃料电池,其总反应为:。下列有关说法正确的是A、金属镁作负极材料 B、放电时电解质溶液中向正极移动 C、可使用金属钠代替镁作钠—海水燃料电池电极材料 D、氧气在电极表面发生反应:
-
10、“为生活加速,为品质加码!”汽车已走入千家万户。关于汽车的下列说法不正确的是A、真皮座垫含蛋白质,蛋白质水解的最终产物是氨基酸 B、发动机由合金材料制成,合金都具有熔点高、硬度低的特性 C、车漆的成分之一是有机高分子,可通过单体的加聚或缩聚反应合成有机高分子 D、排气管中的催化剂提高了NO和CO的转化效率,催化剂可降低反应的活化能
-
11、深中通道是集“桥、岛、隧、地下互通”一体的跨海集群工程。下列说法不正确的是A、桥面中心位置,隐藏着一道抗强台风的玻璃墙,玻璃是非晶态固体 B、悬索主缆使用的中国自主研发2060兆帕镀锌铝钢丝,具有强抗腐蚀性 C、桥面铺装了耐高温的环氧沥青,沥青可通过石油裂化获得 D、用于密封沉管接头的可反复折叠M形橡胶止水带属于有机高分子材料
-
12、实验室分析仪器是探索微观世界的眼睛。下列对分析仪器重要部件的推测不正确的是A、X射线衍射仪的氧化铝X射线管:是两性氧化物 B、分光光度计的分光棱镜:可使用Si单质制作 C、核磁共振分析仪的铌钛线圈:属于金属材料 D、红外光谱仪的高压氦氖激光源:产生激光与电子跃迁有关
-
13、传统工艺承古韵,非遗文化见风采。下列非遗文化产品中,主要材质为无机非金属材料的是


A.开平灰塑
B.新会葵扇


C.新会陈皮
D.白沙茅龙笔
A、A B、B C、C D、D -
14、有机化合物 G 可用于治疗神经系统疾病,人工合成路线如下:
 (1)、H 中官能团的名称为。(2)、B→D 的反应类型为。(3)、的另一种产物的分子式为C7H8O,则结构简式为。(4)、G(填“存在”或“不存在”)顺反异构现象。(5)、C 的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:。
(1)、H 中官能团的名称为。(2)、B→D 的反应类型为。(3)、的另一种产物的分子式为C7H8O,则结构简式为。(4)、G(填“存在”或“不存在”)顺反异构现象。(5)、C 的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:。①能发生银镜反应
②分子中含有3个甲基
③分子中含有4种不同化学环境的氢原子
(6)、写出以CH3CH2OH和 为原料制备
为原料制备 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。 -
15、以芳香烃 A(C7H8)为原料合成某中间体 H 的路线如下:

已知:①
②
(1)、与 A 反应的反应物及反应条件是。(2)、②③④的反应类型分别是、、。(3)、反应⑤的化学方程式:。(4)、反应⑥的化学方程式:。 -
16、醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:

可能用到的有关数据如下:
相对分子质量
密度()
沸点/℃
溶解性
环己醇
100
0.9618
161
微溶于水
环己烯
82
0.8102
83
难溶于水
合成反应:
在 a 中加入 20 g 环己醇和 2 小片碎瓷片,冷却搅动下慢慢加入 1 mL 浓硫酸。b 中通入冷却水后,开始缓慢加热 a,控制馏出物的温度不超过90℃。
分离提纯:
反应粗产物倒入分液漏斗中,分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯 10 g。
回答下列问题:
(1)、装置 b 的名称是。(2)、加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是(填正确答案标号)。A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)、本实验中最容易产生的副产物的结构简式为。(4)、分液漏斗在使用前须清洗干净并;在本实验分离过程中,产物应该从分液漏斗的(填“上口倒出”或“下口放出”)。(5)、分离提纯过程中加入无水氯化钙的目的是。(6)、在环己烯粗产物蒸馏过程中,不可能用到的仪器有(填正确答案标号)。A.蒸馏烧瓶 B.温度计 C.分液漏斗 D.坩埚 E.锥形瓶
(7)、本实验所得到的环己烯产率是___________(填正确答案标号)。A、41% B、50% C、61% D、70% -
17、有机化合物A是一种重要的化工中间体,在一定条件下的转化关系如图所示。

回答下列问题:
(1)、A→B反应的试剂及条件为。(2)、C的含氧官能团的名称是。(3)、A→D的过程中,可生成一种高分子副产物,该副产物的结构简式为。(4)、写出E在碱性条件下与新制氢氧化铜反应的化学方程式:。(5)、通常条件下,向F中加入酸性高锰酸钾溶液可转化为A,你认为这种方法是否正确(填“是”或“否”),请说明理由。 -
18、化合物 Z 是合成平喘药沙丁胺醇的中间体,可通过下列路线制得:

下列说法正确的是
A、等物质的量 X、Y、Z 最多消耗的 NaOH 的物质的量之比为1:2:2 B、等物质的量 X、Y、Z 最多消耗H2的量是相同的 C、X 与苯甲酸互为同分异构体,都能与碳酸氢钠溶液反应生成CO2 D、Y 能发生的反应类型:加成反应、消去反应、取代反应、氧化反应 -
19、化合物Y能用于高性能光学树脂的合成,可由化合物X与2-甲基丙烯酰氯在一定条件下反应制得:

下列有关化合物X、Y的说法正确的是
A、X分子中所有原子一定在同一平面上 B、Y中含有三种官能团,其中能与H2加成的官能团只有一种 C、X、Y均不能使酸性KMnO4溶液褪色 D、X→Y的反应为加成反应 -
20、我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下:
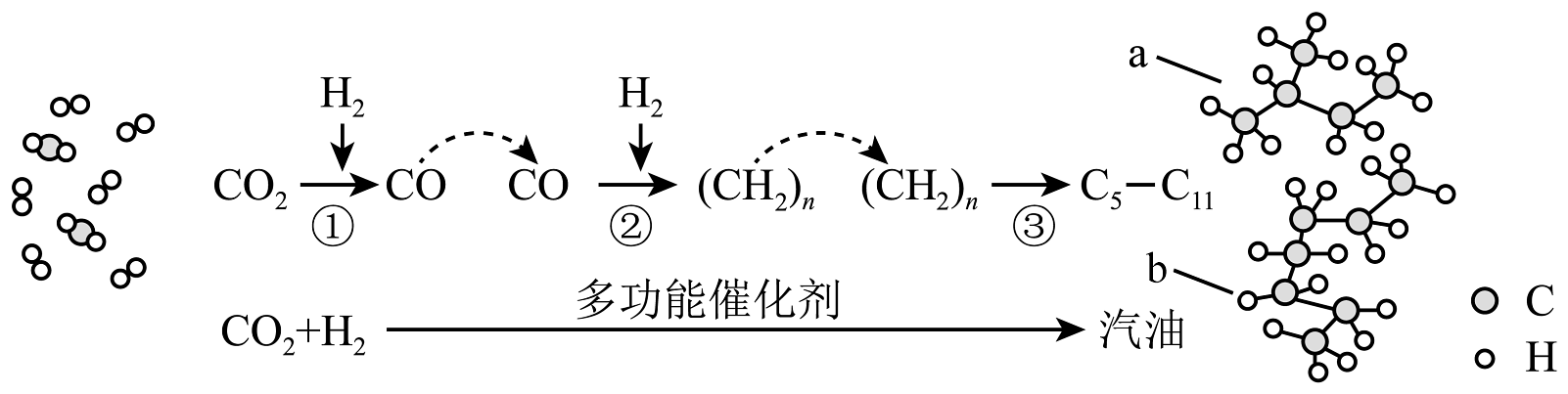
下列说法不正确的是
A、反应①的产物中含有水 B、反应②中只有碳碳键形成 C、汽油主要是的烃类混合物 D、相同情况下 a 比 b 的沸点低