相关试卷
-
1、下列化学用语或图示不正确的是A、2-丁烯的实验式:CH2 B、SO的VSEPR模型:
 C、基态Cr原子的价层电子排布式:3d54s1
D、HF分子中σ键的形成:
C、基态Cr原子的价层电子排布式:3d54s1
D、HF分子中σ键的形成:
-
2、化学研究应当注重宏观与微观相结合。下列宏观现象与微观解释不符的是
选项
宏观现象
微观解释
A
氮气稳定存在于自然界中
氮分子中存在氮氮三键,断开该共价键需要较多的能量
B
苯不能使溴的溶液褪色
苯分子中碳原子形成了稳定的大键
C
天然水晶呈现多面体外形
原子在三维空间里呈周期性有序排列
D
氯化钠晶体熔点高于氯化铝晶体
离子晶体中离子所带电荷数越少,离子半径越大,离子晶体熔点越低
A、A B、B C、C D、D -
3、制作食醋的传统方法是发酵谷物中的淀粉,其过程包括淀粉水解、发酵制醇和发酵制酸等三个阶段,食醋风味的产生与其制作过程中生成的酯类物质有关。下列说法不正确的是A、淀粉水解阶段有葡萄糖产生 B、发酵制醇阶段有CO2产生 C、发酵制酸阶段有酯类物质产生 D、上述三个阶段均应在无氧条件下进行
-
4、为缓解温室效应与能源供应之间的冲突,的资源化利用已成为研究的热点。(1)、、重整能获得氢能,同时能高效转化温室气体。
①已知:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
反应Ⅳ:
②其他条件相同,、混合气体在催化剂a、b作用下分别发生重整反应,催化剂表面均产生积碳。对附着积碳的催化剂a、b在空气中加热以除去积碳(该过程催化剂不发生反应),剩余固体的质量变化如图所示。则重整反应中能保持较长时间催化活性的是(填“催化剂a”或“催化剂b”),判断的理由是。
 (2)、利用制备甲酸。
(2)、利用制备甲酸。①我国科学家利用在Ru(与Fe同族)基催化剂上加氢成功制得甲酸。催化过程如图所示。

与吸附了H原子的催化剂通过配位键形成中间体X,X的结构式为。该催化过程的总反应为。
②一种利用电催化反应器合成甲酸的工作原理如图所示。

阴极主要发生的电极反应式:。
③/HCOOH循环在氢能的贮存释放、燃料电池等方面具有重要应用。其他条件不变,催化加氢转化为的转化率随温度的变化如图所示。反应温度在40~80℃范围内,催化加氢的转化率迅速上升,但是在80~100℃范围内,催化加氢的转化率下降,两段变化的主要原因是。

-
5、
某兴趣小组利用废旧铂镍催化剂回收金属铂,实验步骤如下:
步骤Ⅰ 利用如图所示装置边搅拌边持续加热8h。

(1)为提高盐酸利用率,图中三颈烧瓶a口处还需要添加的仪器为。
步骤Ⅱ 取出步骤Ⅰ中所得固体,洗涤后加至浓硝酸和浓盐酸的混合液中发生氧化反应,得到含的溶液。
(2)写出Pt发生反应的化学方程式:。
(3)该过程需控制在40℃左右的原因是。
步骤Ⅲ 向的溶液中加入等体积的NH4Cl溶液,生成沉淀。反应原理: , 。
(4)为使铂沉淀完全,即 , 所加溶液浓度最小为(忽略混合时溶液体积变化)。
步骤Ⅳ 向溶液中加入溶液,充分反应后得到金属铂,同时有逸出。
(5)还原0.5mol , 参加反应的物质的量为mol。
(6)铂镍合金在低温下形成的超导结构有序相,其立方晶胞结构如图所示,化学式为 , 图中“○”代表金属原子Pt或Ni,请在答题卡上将Pt原子所在位置涂黑。

-
6、有机物F是合成药物泊沙康唑的重要中间体,其合成路线如下:
 (1)、A分子中碳原子杂化方式为。(2)、B→C的反应类型为。(3)、反应D→E中,的作用是。E→F中有副产物()生成,其结构简式为。(4)、W是组成比F少“”的有机物。写出同时满足下列条件的W的一种同分异构体的结构简式:。
(1)、A分子中碳原子杂化方式为。(2)、B→C的反应类型为。(3)、反应D→E中,的作用是。E→F中有副产物()生成,其结构简式为。(4)、W是组成比F少“”的有机物。写出同时满足下列条件的W的一种同分异构体的结构简式:。①能与溶液发生显色反应,也能发生银镜反应;
②分子中有4种化学环境的氢。
(5)、写出以 和为原料制备化合物
和为原料制备化合物 的合成路线流程图(题中有机试剂可选用,其它无机试剂和有机溶剂仟用,合成路线流程图示例见本题题干)。
的合成路线流程图(题中有机试剂可选用,其它无机试剂和有机溶剂仟用,合成路线流程图示例见本题题干)。 -
7、某废弃锂离子电池正极材料(含、及少量Al、Fe、等杂质)的湿法回收流程如下:

已知:
①常温下,溶液中部分金属离子完全转化为氢氧化物沉淀时的pH如下:Al3+:4.7 Fe2+:8.6 Fe3+:3.2
②微溶于水,在冷水中的溶解度比在热水中的大。
(1)、“酸浸”①将正极活性材料进行破碎处理的目的是。
②在浸取过程中发生反应的化学方程式为。
(2)、“调pH=5”①加入NaOH调pH之前要检验是否含有 , 其操作为:。
②滤渣2的主要成分是(填化学式)。
(3)、“沉钴”称取沉钴后所得固体5.49 g高温灼烧,残留固体的质量随温度变化关系如图所示。500℃时所得钴的氧化物化学式为(写出计算过程)。 (4)、“沉锂”
(4)、“沉锂”在10mL 0.1溶液中逐滴加入0.1 HCl溶液,溶液中含碳元素微粒的物质的量随pH变化的图像如图所示(逸出未画出)

补充由“沉钴”后的母液制备的操作方案:向母液中加入(须使用的试剂:NaOH溶液,饱和溶液,乙醇溶液),得到。
-
8、与重整制氢的主要反应为
反应Ⅰ:
反应Ⅱ:
在一定条件下,将混合气体通入反应器中。平衡时,各组分的物质的量分数与温度的关系如下图所示。下列说法正确的是
 A、反应Ⅰ的 B、曲线a为CO的物质的量分数 C、通过提高投料比或增大压强方式可提高平衡转化率 D、450~550℃,浓度对反应Ⅱ的影响大于温度对反应Ⅱ的影响
A、反应Ⅰ的 B、曲线a为CO的物质的量分数 C、通过提高投料比或增大压强方式可提高平衡转化率 D、450~550℃,浓度对反应Ⅱ的影响大于温度对反应Ⅱ的影响 -
9、在给定条件下,下列制备过程涉及的物质转化均可实现的是A、工业制硝酸: B、工业制硫酸: C、工业制漂白粉: D、工业制金属镁:溶液
-
10、化合物Z是一种药物合成中间体,其合成路线如下:

下列说法正确的是
A、X分子的含氧官能团为羰基、酯基 B、1 mol Y可以与5 mol完全加成 C、Z分子中没有手性碳原子 D、Y、Z可以用溶液鉴别 -
11、阅读下列材料,完成下面小题:
碳族元素及其化合物在自然界广泛存在且具有重要应用。甲烷是一种清洁能源,燃烧热较大;反应可用于提纯Ni;工业上用氢气还原三氯硅烷制得高纯度的硅,硅是重要的半导体材料;是一种弱酸,在水中缓慢生成 , 是一种杀菌剂;四氯化锗()水解可得到;醋酸铅[]易溶于水,难电离,醋酸铅溶液可用于吸收气体。
(1)、下列说法正确的是A、Ge原子基态核外电子排布式为[Ar] B、1 mol中含有键数为3 mol C、的空间构型为平面四边形 D、配合物中含离子键、共价键(2)、下列化学反应表示错误的是A、氢气还原三氯硅烷的反应: B、与水反应: C、水解制: D、醋酸铅溶液吸收气体:(3)、下列物质结构与性质或性质与用途具有对应关系的是A、燃烧热较大,可作为燃料 B、溶液呈弱碱性,可用作农业杀菌剂 C、晶体硅熔点高,可用作半导体材料 D、CO具有氧化性,可用于冶炼铁等金属 -
12、“丹砂能化为汞”出自《神农本草经》,该过程涉及化学反应:。下列说法正确的是A、的结构示意图为
 B、O2属于非极性分子
C、HgS中S元素的化合价为-1
D、SO2的VSEPR模型为直线形
B、O2属于非极性分子
C、HgS中S元素的化合价为-1
D、SO2的VSEPR模型为直线形
-
13、《厉害了,我的国》“中国名片”中航天、军事、天文等领域的发展受到世界瞩目。下列说法正确的是A、“中国天眼”的“眼眶”圈梁使用的钢铁属于合金 B、“复兴号”车厢连接处使用的聚四氟乙烯属于烃类 C、“神舟十一号”推进系统材料中的氮化硼属于分子晶体 D、“天宫二号”存储器中的石墨烯和金刚石属于同位素
-
14、有机物G是合成一种重要疱疹药物的中间体,其合成路线如图所示:

回答下列问题:
(1)、化合物A的名称为。(2)、化合物D中官能团的名称为 , 的反应类型为。(3)、化合物F的结构简式为。(4)、的反应方程式为。(5)、芳香族化合物M是C的同分异构体,M能与溶液发生显色反应,满足下列条件的M的同分异构体有种。①苯环上只有两个取代基 ②催化氧化后的产物能发生银镜反应
写出其中苯环上一溴代物只有两种的结构简式(任写一种)。
(6)、参照上述路线,以苯甲醇( )和
)和 为原料设计合成路线合成
为原料设计合成路线合成 (无机试剂任选,注明反应试剂和条件)。
(无机试剂任选,注明反应试剂和条件)。 -
15、
铜及其化合物在日常生产、生活中有着广泛的应用。回答下列问题:
I.将氨水逐滴加入到溶液中,形成难溶物,继续添加氨水后沉淀溶解,得到深蓝色透明溶液,向上述溶液中加入乙醇,并用玻璃棒摩擦试管内壁,最终析出深蓝色晶体。
(1)Cu位于周期表________区,基态的价层电子排布式为________。
(2)形成难溶物的离子反应方程式为________。
(3)具有对称的空间结构,中的两个被两个取代,能得到两种不同结构的产物,则中心离子与配体形成的空间结构是_______。
A. 三角锥形 B. 正四面体 C. 平面三角形 D. 平面正方形 II.科学家通过X射线衍射法推测胆矾的结构如下图所示。

(4)胆矾的阳离子中心原子的配位数为________;胆矾的化学式用配合物的形式可表示为________。
III.溴化亚铜(CuBr)晶胞结构如图所示。已知①、②号铜原子坐标依次为。

(5)③号溴原子的坐标为________。
(6)CuBr的晶体密度为 , 为阿伏加德罗常数,则Cu原子与Br原子的核间距离为________pm(用含和的代数式表示)。
-
16、
硼有“金属材料的维生素”之称,其化合物如硼酸、硼砂等在工业生产中应用广泛。请回答下列问题:
I.与可形成 , 硼的化合物中氢元素化合价为-1价。
(1)基态硼原子的核外电子轨道表示式为。
(2)的电子式为 , 中硼原子的杂化方式为。
(3)中所含元素电负性由大到小的顺序为。
II.硼酸是一种片层状结构的白色晶体,层内氧原子通过氢键连结,结构如下图所示,层与层之间以微弱的分子间作用力相结合构成整个硼酸晶体。

(4)若HF中氢键表示为“”,则硼酸中氢键表示为;1mol硼酸中含有氢键的数目为。
(5)温度升高,硼酸在水中的溶解度增大,主要原因是。
III.硼砂是含结晶水的四硼酸钠,其阴离子(含三种元素)的球棍模型如图:
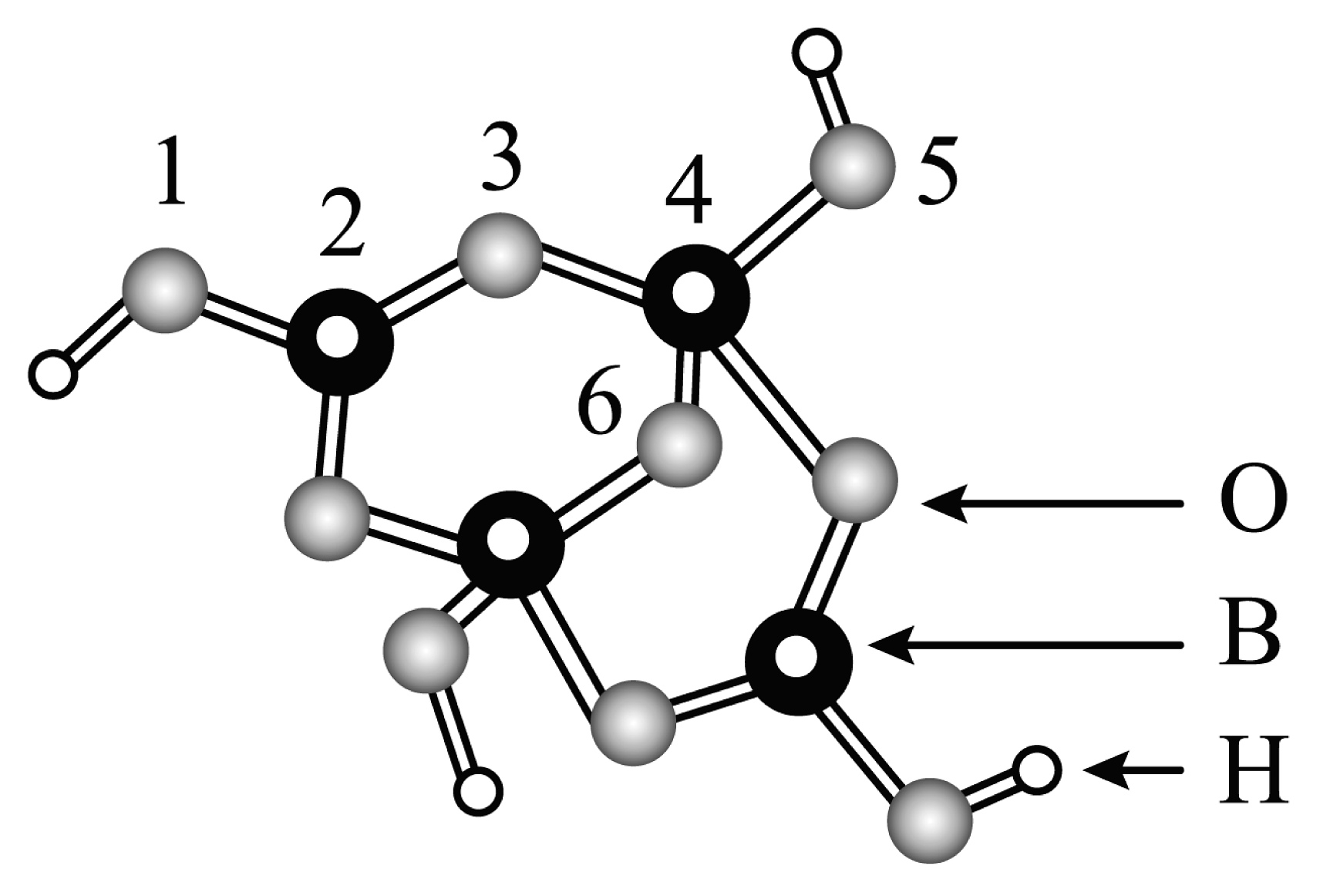
(6)在中,1号氧原子的价层电子对数为 , (填数字)。
-
17、
某种含三种元素的有机物A是我国批准使用的香料,其沸点为。某小组从粗品中分离纯化得到纯品A,然后运用李比希元素定量分析法、现代科学仪器测定有机物A的分子组成和结构,并预测其性质,具体实验过程如下。
步骤一:将粗品用蒸馏法进行纯化。
(1)蒸馏装置如图1所示,仪器a的名称是________,图中虚线框内应选用右侧的仪器________(填“x”或“y”),该实验________(填“能”或“不能”)改用水浴加热,原因是________。

步骤二:确定A的实验式和分子式。
(2)利用元素分析仪测得A中碳的质量分数为 , 氢的质量分数为 , 则A的实验式为________;测得A的蒸汽对二氧化碳的相对密度为2,则A的分子式为________。
步骤三:确定A的结构简式。
(3)A的核磁共振氢谱如图2,图中峰面积之比为1:3:1:3,A的红外光谱如图3。

根据上述信息推断A的结构简式为________。
步骤四:预测A可能的性质。
(4)某小组对A的结构和可能具有的化学性质进行了如下描述,其中正确的是_______。
A. 分子中含有一个手性碳原子 B. A分子中含有键和键的数目之比为12:1 C. 在氢氧化钠的乙醇溶液中加热可发生消去反应 D. 在一定条件下与氢气发生反应生成 -
18、已知几种物质的结构或晶胞如下图所示,下列说法正确的是
 A、在金刚石晶体中,碳原子与碳碳键个数的比为1:4 B、E和F形成的气态团簇分子的分子式为EF或FE C、在NaCl晶体中,距离最近的形成正六面体形 D、在晶体中,与距离最近且紧邻的共有12个
A、在金刚石晶体中,碳原子与碳碳键个数的比为1:4 B、E和F形成的气态团簇分子的分子式为EF或FE C、在NaCl晶体中,距离最近的形成正六面体形 D、在晶体中,与距离最近且紧邻的共有12个 -
19、高分子修饰指对高分子进行处理,接上不同取代基改变其性能。我国高分子科学家对聚乙烯进行胺化修饰,并用来制备新材料,合成路线如图所示。下列说法正确的是
 A、a分子的核磁共振氢谱图中有4组峰 B、高分子b能使溴的四氯化碳溶液褪色 C、高分子c的水溶性比聚乙烯的水溶性好 D、聚乙烯进行胺化修饰后,其化学性质没有改变
A、a分子的核磁共振氢谱图中有4组峰 B、高分子b能使溴的四氯化碳溶液褪色 C、高分子c的水溶性比聚乙烯的水溶性好 D、聚乙烯进行胺化修饰后,其化学性质没有改变 -
20、汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述不正确的是
 A、汉黄芩素的分子式为 B、1mol该物质与溴水反应,最多消耗 C、1mol该物质与NaOH反应,最多消耗2molNaOH D、与足量发生加成反应后,该分子中官能团的种类减少2种
A、汉黄芩素的分子式为 B、1mol该物质与溴水反应,最多消耗 C、1mol该物质与NaOH反应,最多消耗2molNaOH D、与足量发生加成反应后,该分子中官能团的种类减少2种