相关试卷
-
1、中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物()。回答下列问题:(1)、基态原子的价电子排布式为。橄榄石中,各元素电负性大小顺序为 , 铁的化合价为。(2)、已知一些物质的熔点数据如下表:
物质
熔点/℃
800.7
与均为第三周期元素,熔点明显高于 , 原因是。分析同族元素的氯化物、、熔点变化趋势及其原因。的空间结构为 , 其中的轨道杂化形式为。
(3)、一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有个。该物质化学式为 , B-B最近距离为。
-
2、请回答以下问题:(1)、载人航天器中,通过以下两个反应实现氧的循环:
Ⅰ.
Ⅱ.
写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式。
(2)、在分子中,与N原子相连的H呈正电性 , 与B原子相连的H呈负电性 , 这三种元素电负性从大到小的顺序是。(用元素符号作答)(3)、的溶液中水电离出的物质的量为mol。(4)、下图为相互串联的三个装置,试回答:
①写出甲池负极的电极反应式:。
②若利用乙池在铁片上镀银,则B是(填电极材料)。
③向丙池溶液中滴加几滴酚酞试液,电极(填“石墨”或“Fe”)周围先出现红色,该电极的电极反应式为:;电解中,若丙池仅产生两种气体,要使丙池溶液恢复原浓度,可向溶液中加入。(填化学式)
-
3、某晶体的晶胞结构如图所示,已知晶胞参数分别为a nm、b nm、c nm,A、B原子的坐标分别为、 , 阿伏加德罗常数的值为。下列说法不正确的是( )
 A、Cu位于元素周期表ds区 B、C原子的坐标为 C、该晶体的化学式为 D、该晶体的密度为
A、Cu位于元素周期表ds区 B、C原子的坐标为 C、该晶体的化学式为 D、该晶体的密度为 -
4、某立方晶系的锑钾(Sb—K)合金可作为钾离子电池的电极材料,图a为该合金的晶胞结构图,图b表示晶胞的一部分。下列说法正确的是( )
 A、该晶胞的体积为a3×10-36cm-3 B、K和Sb原子数之比为3∶1 C、与Sb最邻近的K原子数为4 D、K和Sb之间的最短距离为apm
A、该晶胞的体积为a3×10-36cm-3 B、K和Sb原子数之比为3∶1 C、与Sb最邻近的K原子数为4 D、K和Sb之间的最短距离为apm -
5、化合物是分析化学中重要的基准物质。X、Y、Z、W、T均为36号以前的元素,原子序数依次增加,X原子的电子只有一种自旋取向,Y原子的最外层电子排布式为 , W、Z同主族,且W的原子序数是Z的两倍,T元素基态原子的正三价离子的3d轨道为半充满。下列说法错误的是( )A、电负性:Y>W>X B、化合物中Y和W原子的杂化方式不同 C、简单氢化物的沸点:Z>Y D、是工业制备的原料
-
6、下列反应的离子方程式错误的是( )A、过量铁粉与稀硝酸反应: B、溶于烧碱溶液: C、向溶液通入足量: D、溶液滴入溶液中:
-
7、日光中用到的某种荧光粉的主要成分为。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为。下列说法错误的是( )A、电负性:Y>X>Z>W B、原子半径:Y>X>Z>W C、Y和W的单质都能与水反应生成气体 D、Z元素最高价氧化物对应的水化物具有强氧化性
-
8、下列有关物质结构或性质的说法不正确的是( )A、凡是中心原子采取杂化的分子,其空间结构都是正四面体 B、盐碱地可以通过施加适量的石膏降低土壤碱性 C、从虾蟹壳中提取的甲壳质可制成全降解的手术缝合线 D、等离子体是由电子、阳离子和电中性粒子组成的混合物
-
9、价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是( )A、与的键角相等 B、和均为非极性分子 C、和的空间构型均为平面三角形 D、和的VSEPR模型均为四面体
-
10、下列化学用语表述正确的是( )A、的电子式:
 B、中子数为10的氧原子:
C、分子的VSEPR模型:
B、中子数为10的氧原子:
C、分子的VSEPR模型: D、基态原子的价层电子轨道表示式为
D、基态原子的价层电子轨道表示式为
-
11、近年来甲醇用途日益广泛,越来越引起商家的关注。工业上甲醇的合成途径多种多样。现在实验室中模拟甲醇合成反应,在2L密闭容器内,400℃时发生反应CO(g)+2H2(g)CH3OH(g),体系中n(CO)随时间的变化如表:
时间/s
0
1
2
3
5
n(CO)/mol
0.020
0.011
0.008
0.007
0.007
(1)、图甲中表示CH3OH的变化的曲线是(填字母)。 (2)、下列措施不能提高反应速率的有(填字母,下同)。
(2)、下列措施不能提高反应速率的有(填字母,下同)。a.升高温度 b.加入催化剂
c.减小压强 d.及时分离出CH3OH
(3)、下列叙述能说明反应达到平衡状态的是。a.CO和H2的浓度保持不变
b.v(H2)=2v(CO)
c.CO的物质的量分数保持不变
d.容器内气体密度保持不变
e.每生成1molCH3OH的同时有2molH-H断裂
(4)、现有如下两个反应:A.NaOH+HCl=NaCl+H2O,B.Cu+2Ag+=2Ag+Cu2+。①根据上述两反应的本质,能设计成原电池的是(填字母)。
②将上述反应中能设计成原电池的反应设计成原电池。
I.写出负极的电极反应式 , 反应类型为。
II.画出装置图并标明电极材料与名称、电解质溶液、电子流向。

-
12、现有金属A、B、C,化合物D、E、F、G、H和气体甲、乙、丙,其转化关系如图所示。
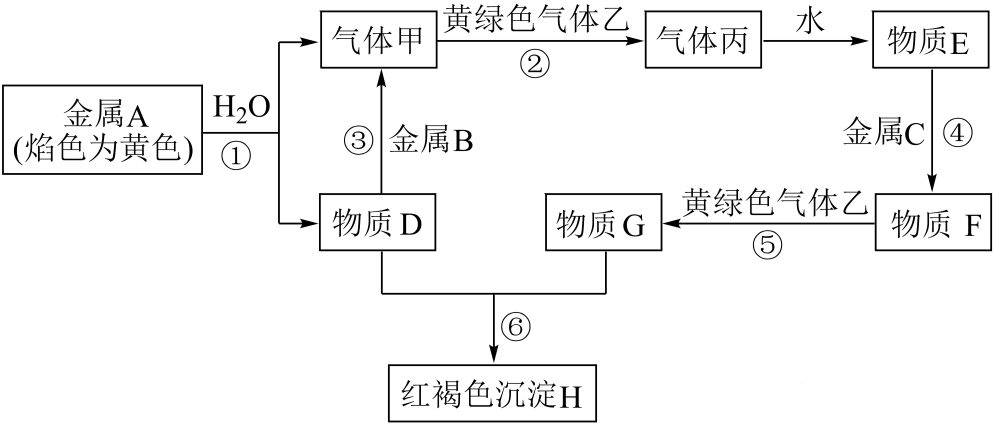
请回答下列问题:
(1)、丙的电子式为。(2)、反应①的离子方程式为 , 每生成0.5mol的甲时,转移电子数为。(3)、向F溶液中滴加NaOH溶液的现象是 , 写出其中属于氧化还原反应的化学方程式。(4)、G溶液常用于腐蚀覆盖同印刷电路板,请写出相关反应的离子方程式。 -
13、如表列出了9种元素在元素周期表(元素周期表中给出部分)中的位置。

请回答下列问题:
(1)、考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的符号是。(2)、画出元素⑧形成的简单离子的结构示意图:。(3)、元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物反应的离子方程式为。(4)、元素②③④⑤⑧⑨与元素①形成的最简单化合物中稳定性最强的是(填化学式)。(5)、元素⑦和⑧形成化合物的化学键类型为。(6)、用电子式表示元素⑥和⑨形成化合物的过程。 -
14、某学习小组在实验室制备氯化铁并配制其溶液,过程如下。
【制备无水FeCl3】无水FeCl3是一种常见的化工原料,易升华,在空气中极易吸水,可利用以下实验装置制备。
 (1)、按气流方向,连接顺序为a→→j→k→f→g→b→c(填仪器连接口的字母编号)。(2)、装置B的作用是。(3)、A中发生的离子反应为。(4)、【配制FeCl3溶液】
(1)、按气流方向,连接顺序为a→→j→k→f→g→b→c(填仪器连接口的字母编号)。(2)、装置B的作用是。(3)、A中发生的离子反应为。(4)、【配制FeCl3溶液】配置100mL0.5mol/LFeCl3溶液,需用量筒量取5.0mol/LFeCl3溶液mL,还需要的仪器有烧杯、玻璃棒、。
(5)、下列实验操作对所配制的FeCl3溶液物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)①定容时,俯视刻度线:。
②未洗涤烧杯及玻璃棒:。
-
15、下列实验中,对应的操作、现象以及结论都正确的是( )
选项
操作
现象
结论
A
干燥氯气通入装有鲜花的集气瓶中
鲜花褪色
氯气有漂白性
B
将KI溶液滴加到酸性KMnO4溶液中,边加边振荡
溶液褪色
KI具有还原性
C
向某溶液中先加入BaCl2溶液,再加入稀硝酸
产生白色沉淀
该溶液中一定含有SO
D
向某溶液中加入NaOH溶液
产生气泡
该溶液中一定含有NH
A、A B、B C、C D、D -
16、下列离子方程式不正确的是( )A、Cl2与H2O反应:Cl2+H2OH++Cl-+HClO B、Na2O2溶于足量水中:2Na2O2+2H2O=4Na++4OH-+O2↑ C、Cu与FeCl3反应:Cu+2Fe3+=2Fe2++Cu2+ D、稀HNO3与过量Fe反应:Fe+4H++NO=Fe3++NO↑+2H2O
-
17、硅是带来人类文明的重要元素之一,科学家也提出硅是“21世纪的能源”。这主要是由于硅及其化合物对社会发展所起的巨大促进作用。下列关于硅及其化合物的说法中错误的是( )A、传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料 B、高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” C、陶瓷、玻璃、水泥容器均不能贮存氢氟酸 D、传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐
-
18、室温下,下列各组离子在指定溶液中能大量共存的是( )A、使酚酞试液变红的溶液:Na+、Cl-、SO、Fe3+ B、碳酸氢钠溶液:K+、SO、Cl-、H+ C、加入铝粉放出H2的溶液:K+、Na+、SO、Cl- D、硫酸溶液:NH、Na+、MnO、Cl-
-
19、下列各组气体中均能用如图装置进行喷泉实验的是( )
 A、HCl和CO2 B、NH3和CO C、O2和CO2 D、NO2和NO
A、HCl和CO2 B、NH3和CO C、O2和CO2 D、NO2和NO -
20、设NA为阿伏加德罗常数的值,则下列说法正确的是( )A、0.2mol•L-1的Na2SO4溶液中含Na+数目为0.4NA B、在氧化还原反应中,反应掉1molCl2时转移电子数目一定为2NA C、标况下,2.24L水中含有的电子数目为NA D、常温常压下,22g二氧化碳中含有的原子数目为1.5NA