相关试卷
-
1、某含锰废料中主要含MnCO3及少量的FeCO3、SiO2、Cu2(OH)2CO3 , 以此为原料制备MnO2的流程如下:
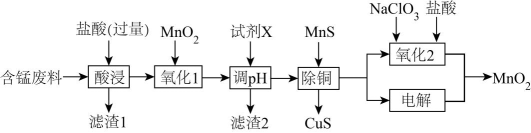
Ⅰ.氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物
Mn(OH)2
Fe(OH)2
Fe(OH)3
Cu(OH)2
开始沉淀时pH
8.3
6.3
2.7
4.7
完全沉淀时pH
9.8
8.3
3.7
6.7
Ⅱ.常温下Ksp(MnS)=2.0×10-10、Ksp(CuS)=6.0×10-36。
回答下列问题:
(1)、滤渣1的主要成分是(填化学式)。(2)、“氧化1”的目的是(用离子方程式表示)。(3)、“调pH”时,试剂X为(任写一种),pH的调节范围为。(4)、“除铜”时,当溶液中c(Mn2+)=12mol·L-1 , 溶液中c(Cu2+)=。(5)、“氧化2”制备MnO2 (恰好完全反应)时,n(Mn2+):n(ClO)=( ClO→Cl-);“电解”制备MnO2的阳极电极反应式为。 -
2、是存在于燃气中的一种有害气体,脱除的方法有多种。回答下列问题:(1)、Claus氧化回收硫的反应原理为:
① ;
② ;
③ 。
则。
(2)、化学反应的焓变与反应物和生成物的键能(气态分子中化学键解离成气态原子所吸收的能量)有关。已知某些化学键的键能如下表所示:共价键
键能
339
246
120
结合(1)中反应原理,。
(3)、电解法治理是先用溶液吸收含的工业废气,所得溶液用情性电极电解,阳极区所得溶液循环利用。
①进入电解池的溶液中,溶质是(填化学式)。
②阳极的电极反应式为。
(4)、工业上采用高温热分解的方法制取 , 在膜反应器中分离出。下,分解:。保持压强不变,反应达到平衡时,气体的体积分数随温度的变化曲线如图:
①在密闭容器中,关于上述反应的说法正确的是 (填字母)。
A.随温度的升高而增大
B.低压有利于提高的平衡分解率
C.维持温度、气体总压强不变时,向平衡体系中通入氩气,则v(正)<v(逆)
D.在恒容密闭容器中进行反应,当气体密度不再变化时,反应达到平衡状态
②图中点:的平衡转化率为;时,反应的(为以分压表示的平衡常数,分压=总压×物质的量分数)。
-
3、已知A、B、C、D、E为原子序数依次增大的短周期主族元素。其中A元素的一种同位素中没有中子,B元素原子的L层电子数是K层电子数的2倍,D元素是地壳中含量最多的元素,E的原子序数是A、C原子序数之和的2倍。回答下列问题:(1)、分子中键和键数目比为;是由极性键和非极性键形成的(填“极性”或“非极性”)分子。(2)、A与C可形成一种原子个数比为的六原子分子,其结构式为 , 其中C原子的杂化方式为。(3)、的VSEPR模型名称为 , 其属于(填“极性”或“非极性”)分子。(4)、基态E原子的价层电子排布式为 , 其最高价氧化物对应的水化物的化学式为。(5)、的沸点比的沸点低,其主要原因是。
-
4、化学是一门以实验为基础的学科。回答下列问题:(1)、Ⅰ.某同学设计如图所示实验,探究反应中的能量变化。
()所涉及的反应为(填“放”或“吸”)热反应,将实验()中的铝片更换为等质量的铝粉后,释放出的热量(填“增加”“减少”或“不变”)。 (2)、从实验装置()上看,图中尚缺少的一种仪器是。实验()为稀盐酸和氢氧化钠稀溶液反应测定反应热,反应物的用量理论上对中和反应反应热的测定(填“有”或“无”)影响;用相同浓度和体积的氨水代替溶液进行上述实验,测得的中和反应反应热的数值()会(填“偏大”“偏小”或“无影响”)。(3)、Ⅱ.用广谱高效的二氧化氯()替代液氯进行消毒,可避免产生对人体健康有害的有机氯代物。化学小组欲对用消毒过的自来水进行氯元素含量的测定(假设全部转化为),进行如下实验:向水样中加几滴溶液,用的溶液滴定(已知和可反应生成砖红色沉淀)。
(2)、从实验装置()上看,图中尚缺少的一种仪器是。实验()为稀盐酸和氢氧化钠稀溶液反应测定反应热,反应物的用量理论上对中和反应反应热的测定(填“有”或“无”)影响;用相同浓度和体积的氨水代替溶液进行上述实验,测得的中和反应反应热的数值()会(填“偏大”“偏小”或“无影响”)。(3)、Ⅱ.用广谱高效的二氧化氯()替代液氯进行消毒,可避免产生对人体健康有害的有机氯代物。化学小组欲对用消毒过的自来水进行氯元素含量的测定(假设全部转化为),进行如下实验:向水样中加几滴溶液,用的溶液滴定(已知和可反应生成砖红色沉淀)。在规格为的滴定管中,若溶液的起始读数是 , 则此时滴定管中溶液的实际体积为____(填字母)。
A、 B、小于 C、 D、大于(4)、如图所示,排去碱式滴定管中气泡的方法应采用操作(填“甲”“乙”或“丙”),然后轻轻挤压玻璃球使尖嘴部分充满碱液。 (5)、滴定过程如下:
(5)、滴定过程如下:①在清水洗涤后,用标准溶液润洗滴定管次
②取标准液注入滴定管至刻度线0处,并固定在铁架台上
③排气泡后,记下读数
④移取待测水样注入洁净的锥形瓶中,并加入滴试液
⑤把锥形瓶放在滴定管的下面,垫上白纸
⑥时,停止滴定,并记下滴定管液面的刻度
(6)、重复实验2次将操作⑥补充完整:。
下列操作或误差判断不正确的是(填字母)。
A.滴定过程中,眼睛始终注视锥形瓶中溶液颜色的变化
B.锥形瓶清洗后需要用待测水样润洗次
C.滴定完成后,俯视滴定管读数,会造成滴定结果偏高
D.若滴定结束发现滴定管中出现气泡,则使结果偏低
-
5、常温下,用某未知浓度的溶液滴定溶液,滴定曲线如图所示,c点溶液中,。下列说法错误的是( )
 A、c点为反应终点 B、该溶液的物质的量浓度为 C、b点溶液中, D、a点溶液中,
A、c点为反应终点 B、该溶液的物质的量浓度为 C、b点溶液中, D、a点溶液中, -
6、某温度下,2L容积不变的密闭容器中与反应生成 , 反应过程中X、Y、Z的物质的量变化如图1所示。保持其他条件不变,温度分别为和时,Z的体积百分含量与时间的关系如图2所示。下列结论错误的是( )
 A、反应的前3min内,用X表示的反应速率 B、容器中发生的反应可表示为: C、保持其他条件不变,升高温度,化学平衡向正反应方向移动 D、若改变反应条件,反应进程如图3所示,则改变的条件是使用催化剂
A、反应的前3min内,用X表示的反应速率 B、容器中发生的反应可表示为: C、保持其他条件不变,升高温度,化学平衡向正反应方向移动 D、若改变反应条件,反应进程如图3所示,则改变的条件是使用催化剂 -
7、如图为阳离子交换膜法以石墨为电极电解饱和溶液的原理示意图。已知溶液从A口进料,含少量的水从B口进料,下列说法错误的是( )
 A、阳极发生氧化反应,有氧气生成 B、电路中转移电子时,阳极区有生成 C、从D出口流出的是较浓的溶液 D、从E出口逸出的气体是
A、阳极发生氧化反应,有氧气生成 B、电路中转移电子时,阳极区有生成 C、从D出口流出的是较浓的溶液 D、从E出口逸出的气体是 -
8、磷化氢()是一种无色剧毒,有类似大蒜气味的气体,微溶于冷水。下列关于的叙述错误的是( )A、分子中有未成键的电子对 B、是非极性分子 C、分子结构为三角锥形 D、不能与水形成分子间氢键
-
9、常温下,在水中的沉淀溶解平衡曲线如图所示,已知常温下。下列说法正确的是( )
 A、升高温度曲线会往右上方移动 B、d点表示的过饱和溶液,b点表示的不饱和溶液 C、b点加水可以变到如图的曲线上,且此时的 D、加入 , 可以使溶液由c点变到a点
A、升高温度曲线会往右上方移动 B、d点表示的过饱和溶液,b点表示的不饱和溶液 C、b点加水可以变到如图的曲线上,且此时的 D、加入 , 可以使溶液由c点变到a点 -
10、室温下,下列实验探究方案不能达到探究目的的是( )
选项
探究方案
探究目的
A
向较浓的FeCl2溶液中滴入少量酸性KMnO4溶液,观察KMnO4溶液紫色是否褪去
Fe2+具有还原性
B
Na2O2用棉花包裹放在石棉网上,向棉花上滴几滴水,观察棉花是否燃烧
Na2O2与H2O反应放热
C
向2mL1mol•L-1CH3COOH溶液中滴加1mol•L-1Na2CO3溶液,观察是否产生气泡
比较Ka(CH3COOH)和Ka1(H2CO3)的大小
D
向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化
Br2的氧化性强于I2
A、A B、B C、C D、D -
11、下列各组元素中,彼此的化学性质一定相似的是( )
选项
(Ⅰ)基态原子结构信息
(Ⅱ)基态原子结构信息
A
最外层电子排布式:1s2
最外层电子排布式:2s2
B
核外有12个电子
K、L层电子数之和与M、N层电子数之和相等
C
2p能级上有1个未成对电子
核外电子共有17种运动状态
D
L层上只有一个空轨道
M层上有3个p电子
A、A B、B C、C D、D -
12、下列说法错误的是( )A、合成氨反应采取循环操作主要是为了提高化学反应速率 B、 、 , 则 C、反应 , 能自发进行的原因是 D、一定温度下,对平衡体系缩小体积,再次达到平衡时不变
-
13、下列实验设计或装置能达到实验目的的是( )
 A、按图甲的电路连接对反应塔进行防腐保护 B、用图乙装置在铁制品表面镀一层锌 C、用图丙验证铝和稀盐酸反应是放热反应 D、按图丁装置设计锌铜“双液原电池”实现化学能→电能
A、按图甲的电路连接对反应塔进行防腐保护 B、用图乙装置在铁制品表面镀一层锌 C、用图丙验证铝和稀盐酸反应是放热反应 D、按图丁装置设计锌铜“双液原电池”实现化学能→电能 -
14、以下是一些基态原子能级上的电子排布图及电子排布式:①
 ②
② ③碳原子:④钾原子:。对上述表示方法的评价中,正确的是( ) A、①违背泡利原理 B、②正确 C、③违背能量最低原理 D、④违背洪特规则
③碳原子:④钾原子:。对上述表示方法的评价中,正确的是( ) A、①违背泡利原理 B、②正确 C、③违背能量最低原理 D、④违背洪特规则 -
15、在一刚性密闭容器内发生反应 , 若内B减少了 , 则下列说法正确的是( )A、反应达到平衡时 B、容器内气体总密度不再政变是该反应达到平衡的标志之一 C、内用B表示反应速率为 D、升高温度能加快反应速率主要是其使活化分子的能量明显增加
-
16、工业上通常利用反应来获得单质铝,该反应还需要添加(冰晶石)以降低氧化铝的熔化温度。下列表示相关微粒的化学用语错误的是( )A、质子数与中子数相等的氟原子: B、的结构示意图:
 C、基态钠原子外围电子排布式:
D、基态氧原子的轨道表示式:
C、基态钠原子外围电子排布式:
D、基态氧原子的轨道表示式:
-
17、下列工业上金属的制备方法正确的是( )A、焦炭还原氧化铁制备金属铁 B、电解氯化钠溶液制备金属钠 C、氢气还原氧化镁制备金属镁 D、铝热反应制备金属钙
-
18、下列现象不能用“相似相溶”规律解释的是( )A、硫磺易溶于 B、氯气易溶于溶液 C、碘易溶于 D、二氧化硫易溶于水
-
19、很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。
 (1)、基态硫原子电子排布式为。(2)、、、的沸点由高到低顺序为。(3)、汞的原子序数为80,位于元素周期表第周期第ⅡB族。(4)、化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有____。A、在Ⅰ中S原子采取杂化 B、在Ⅱ中S元素的电负性最大 C、在Ⅲ中C—C—C键角是 D、在Ⅲ中存在离子键与共价键 E、在Ⅳ中硫氧键的键能均相等(5)、汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水溶性较好的是。(6)、理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb取代后形成。
(1)、基态硫原子电子排布式为。(2)、、、的沸点由高到低顺序为。(3)、汞的原子序数为80,位于元素周期表第周期第ⅡB族。(4)、化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有____。A、在Ⅰ中S原子采取杂化 B、在Ⅱ中S元素的电负性最大 C、在Ⅲ中C—C—C键角是 D、在Ⅲ中存在离子键与共价键 E、在Ⅳ中硫氧键的键能均相等(5)、汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水溶性较好的是。(6)、理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb取代后形成。
①图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是。
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为;该晶胞中粒子个数比。
③设X的最简式的式量为Mr,则X晶体的密度为(列出算式)。
-
20、2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯与四氟乙烯的共聚物(ETFE)制成。回答下列问题:(1)、基态F原子的价电子排布图(轨道表示式)为。(2)、图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图是(填标号),判断的根据是;第三电离能的变化图是(填标号)。
 (3)、氟化氢的沸点高于氯化氢的原因是。(4)、聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因。(5)、萤石是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是;若该立方晶胞参数为a pm,正负离子的核间距最小为pm。
(3)、氟化氢的沸点高于氯化氢的原因是。(4)、聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因。(5)、萤石是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是;若该立方晶胞参数为a pm,正负离子的核间距最小为pm。