相关试卷
-
1、下列物质的熔、沸点高低顺序中,正确的是A、金刚石>石墨>碳-60 B、
 C、
D、金刚石>生铁>纯铁>钠
C、
D、金刚石>生铁>纯铁>钠
-
2、物质的结构决定其性质。下列实例与解释不相符的是
选项
实例
解释
A
键角:
O的电负性大于N
B
加热稀溶液,溶液变色
升温促进与形成
C
的碱性强于
中N的电子云密度比大
D
离子液体常温下呈液态
原因之一是离子液体的阴阳离子半径较大
A、A B、B C、C D、D -
3、氨基酸是构成蛋白质的结构单元,某氨基酸的结构简式如图所示。下列有关说法正确的是
 A、第一电离能: B、该分子结构中不存在手性碳原子 C、该分子中碳原子的杂化轨道类型有和 D、键的极性强弱:
A、第一电离能: B、该分子结构中不存在手性碳原子 C、该分子中碳原子的杂化轨道类型有和 D、键的极性强弱: -
4、我国力争2030年前实现碳达峰,2060年前实现碳中和,这体现了中国对解决气候问题的大国担当。在实际生产中,可利用反应:CO2+NaOH=NaHCO3来捕捉废气中的CO2 , 下列有关化学用语表示正确的是A、的空间填充模型:
 B、H2O2的电子式:
B、H2O2的电子式: C、钠原子2py电子云图为
C、钠原子2py电子云图为 D、Na+的电子排布式:
D、Na+的电子排布式:
-
5、文物记载体现中华文明灿烂成就,科技发展体现国家繁荣强盛,下列说法错误的是
 A、宋蕉叶形水晶杯,水晶属于晶体 B、天和核心舱的主要材料SiC是共价晶体 C、“奋斗者”潜水艇的46Ti与47Ti互为同素异形体 D、北斗卫星太阳能电池使用了砷化镓器件,砷是p区元素
A、宋蕉叶形水晶杯,水晶属于晶体 B、天和核心舱的主要材料SiC是共价晶体 C、“奋斗者”潜水艇的46Ti与47Ti互为同素异形体 D、北斗卫星太阳能电池使用了砷化镓器件,砷是p区元素 -
6、硫氰化物是重要的分析试剂和合成中间体。(1)、基态的价电子轨道表示式为。(2)、配制溶液时,常将晶体溶于较浓的盐酸中,再加水稀释到所需浓度,其目的是。(3)、向10mL 0.005溶液中加入10mL 0.015KSCN溶液,反应达平衡后,得到红色溶液M。
①取红色溶液M,分别对其进行如下操作,相关描述正确的有(填标号)。
A.加入少量铁粉,溶液红色变浅
B.加入少量水,溶液中离子总数减小
C.加入几滴1KSCN溶液,溶液红色变深
D.加入几滴0.05 溶液,的值减小
②取红色溶液M,向其中滴加饱和溶液,体系中主要存在以下平衡:
Ⅰ:
Ⅱ:
Ⅲ:
平衡总浓度随滴入饱和溶液滴数的变化曲线如图(忽略溶液体积变化)。
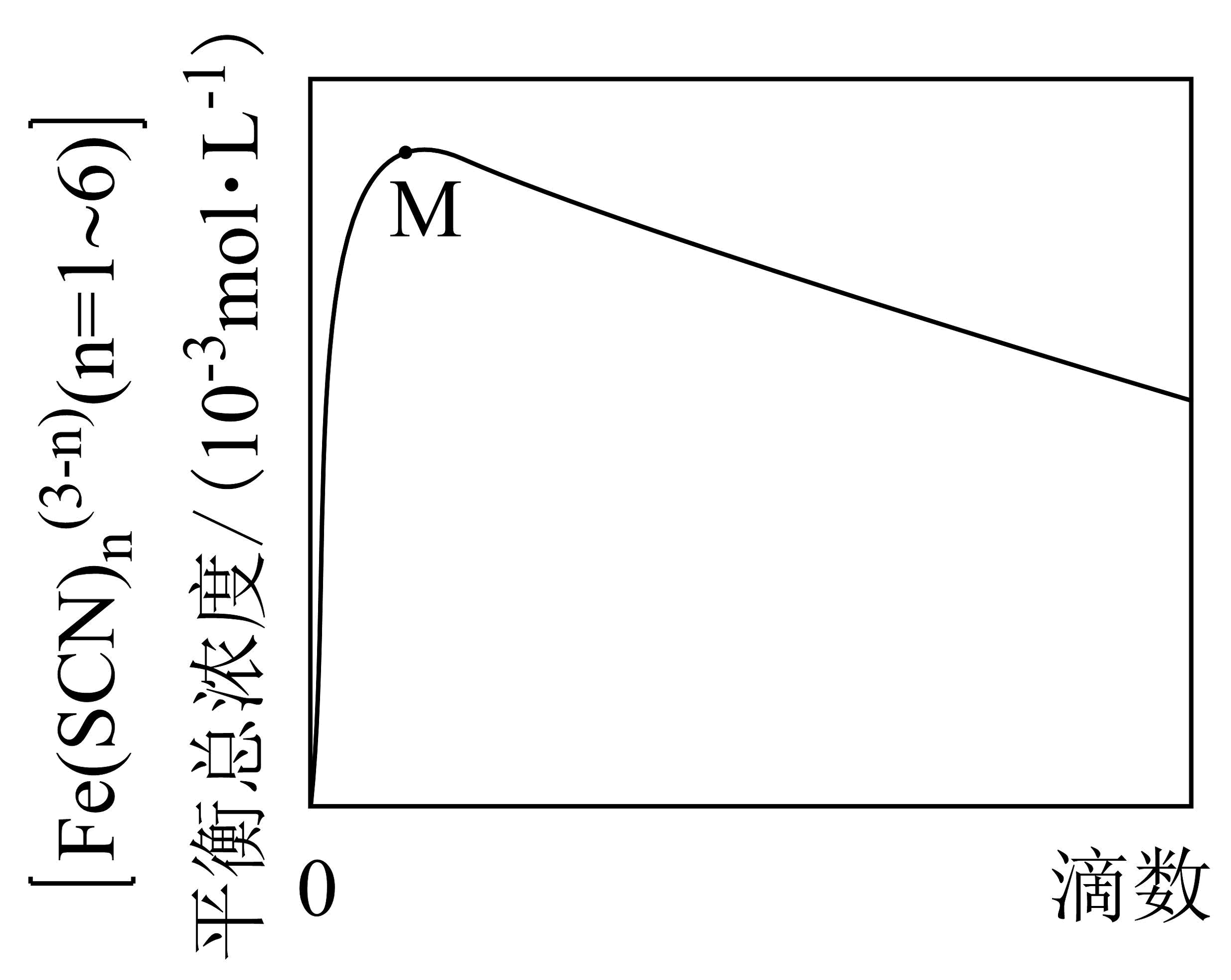
ⅰ.M点前,(填“Ⅰ”“Ⅱ”或“Ⅲ”)的平衡移动,是导致曲线上升的主要原因。
ⅱ.运用平衡移动原理,分析M点后曲线下降的主要原因:。
(4)、某浸金废水中含0.5 , 在相同条件下研究催化剂a、b对该废水中氧化处理过程的影响(氧化处理过程中溶液体积保持不变),的残留率随时间t的变化曲线如图: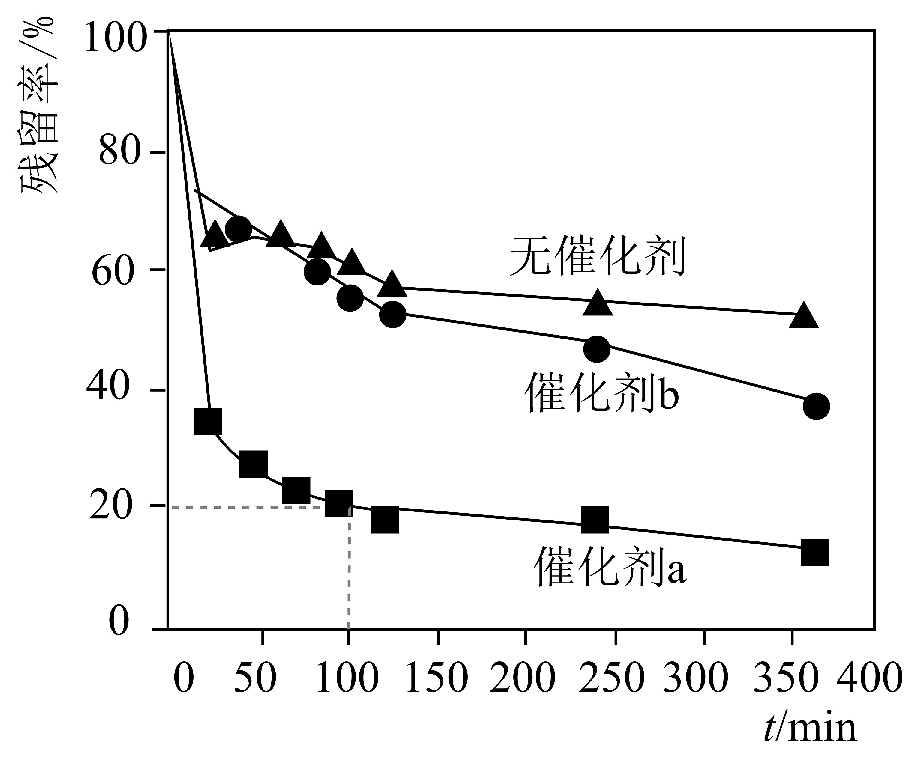
①使用(填“催化剂a”或“催化剂b”)时,的氧化反应活化能更低。
②使用催化剂a时,0~100 min内,的平均反应速率。
(5)、TBP(磷酸三丁酯)难溶于水,对水溶液中HSCN有萃取作用,主要存在的萃取平衡为(o代表有机相)。分别向pH不同的的水溶液中,加入等体积0.2TBP的有机溶液进行萃取(有机溶剂不参与平衡)。、随平衡体系pH的变化如图(分配比D为萃取达平衡时,被萃物在有机相和水相的浓度之比;分析该体系时,需考虑被萃物在水相中的所有存在形式)。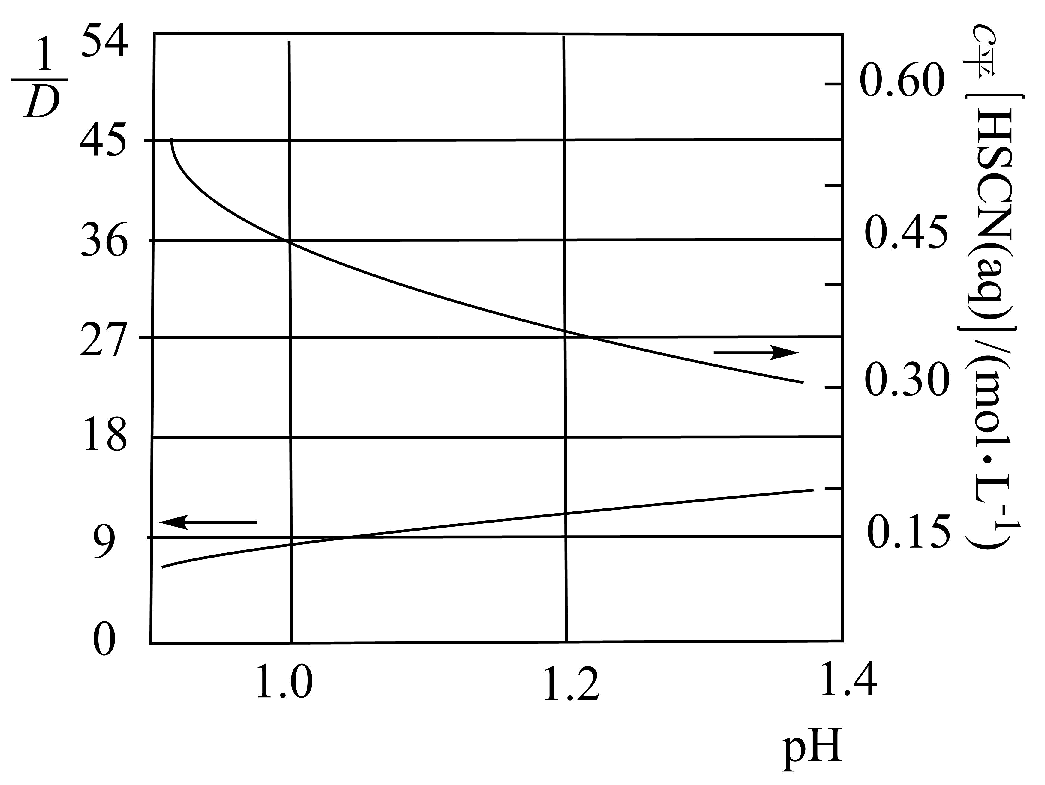
计算上述萃取平衡的平衡常数K=(写出计算过程,保留三位有效数字)。
-
7、利用多膜装置通过电解法可以制备 , 同时获得一定的副产品,其电解装置如图所示。下列说法正确的是
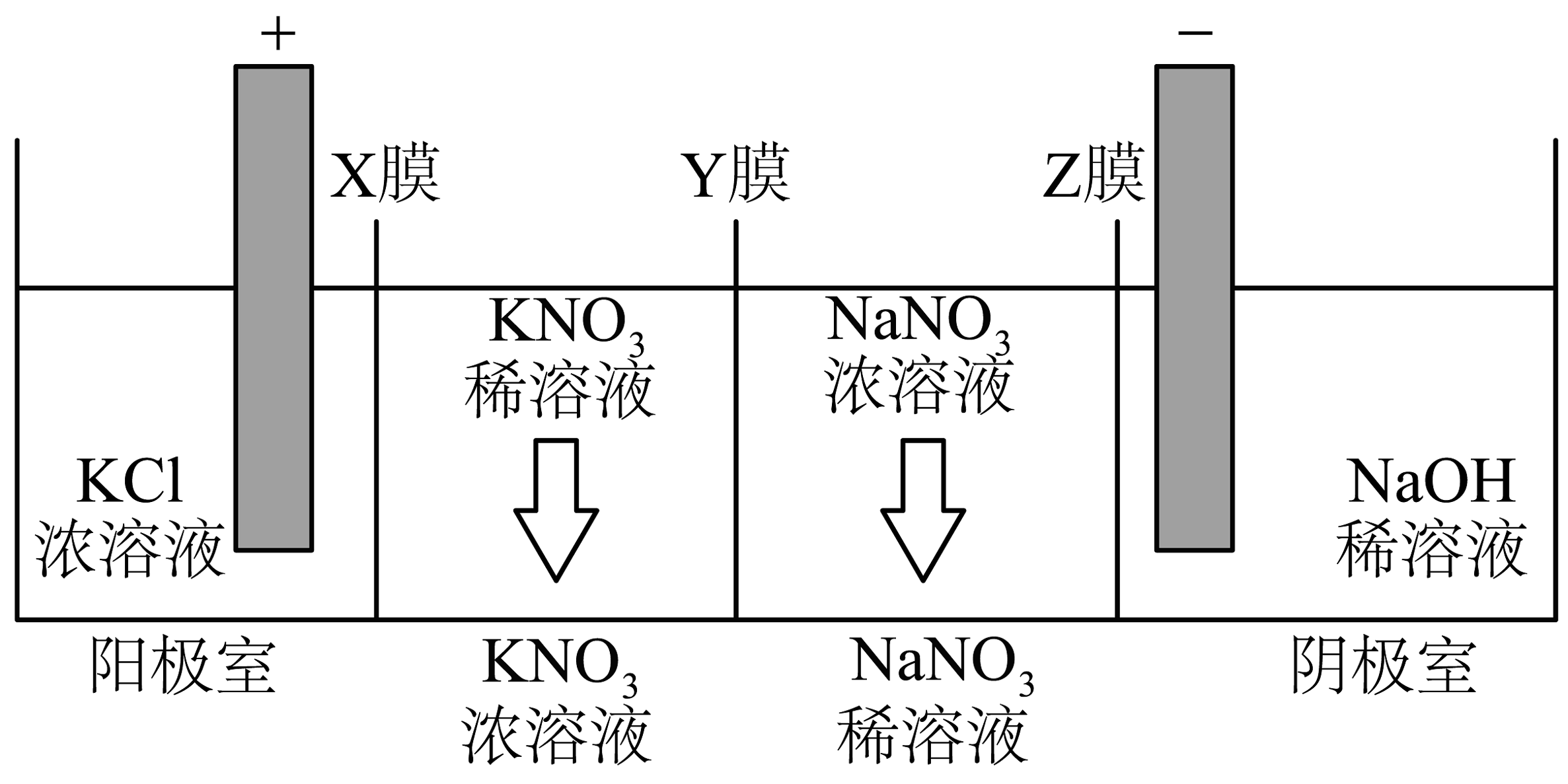 A、Y膜为阳离子交换膜 B、阴极室溶液中浓度逐渐降低 C、理论上每生成标准状况下 , 阳极室内溶液质量减少 D、理论上每生成 , 阴极室溶液质量增加
A、Y膜为阳离子交换膜 B、阴极室溶液中浓度逐渐降低 C、理论上每生成标准状况下 , 阳极室内溶液质量减少 D、理论上每生成 , 阴极室溶液质量增加 -
8、一种杀菌剂的结构式如图所示,元素X、Y、Z、W、T、Q原子序数依次增大且在前四周期均有分布,Y、Z、W在同一周期,和在同一主族,的价层电子排布式为 , 下列说法正确的是
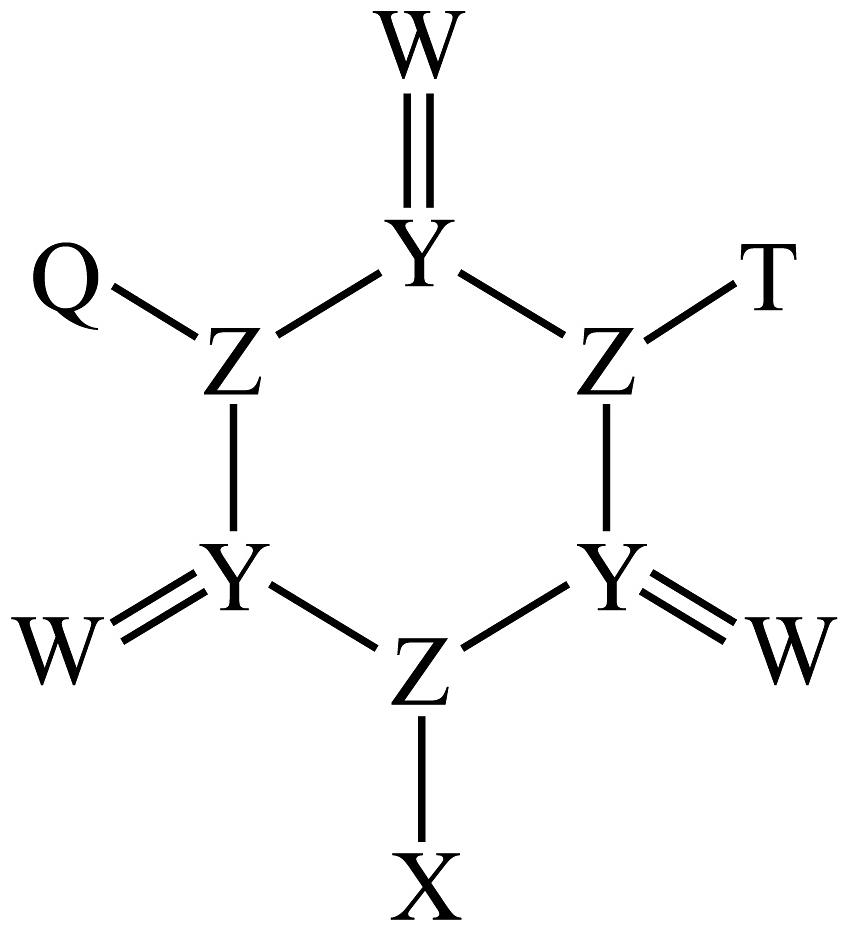 A、的空间结构为平面三角形 B、元素的电负性大小: C、元素的第一电离能: D、最高价氧化物的水化物的酸性:
A、的空间结构为平面三角形 B、元素的电负性大小: C、元素的第一电离能: D、最高价氧化物的水化物的酸性: -
9、下列陈述I、II均正确且存在因果关系的是
选项
陈述I
陈述II
A
酸性:
吸电子效应:
B
金属钠具有强还原性
钠可置换出溶液中的铁单质
C
次氯酸具有漂白性
漂白液在空气中久置易变质
D
往氯乙烷中加入浓溶液后共热,冷却后加入少量溶液,有白色沉淀生成
可证明氯乙烷中含有氯原子
A、A B、B C、C D、D -
10、某实验小组利用下图装置探究浓硫酸与葡萄糖反应生成的气体成分。下列说法正确的是
 A、本实验只体现浓硫酸的脱水性 B、装置b中出现的白色沉淀,可能是BaCO3或BaSO3 C、装置d中出现浑浊,证明产生的气体中含有CO2 D、装置e中可以盛放NaOH溶液
A、本实验只体现浓硫酸的脱水性 B、装置b中出现的白色沉淀,可能是BaCO3或BaSO3 C、装置d中出现浑浊,证明产生的气体中含有CO2 D、装置e中可以盛放NaOH溶液 -
11、为阿伏加德罗常数的值,下列说法正确的是A、分别与足量氯气和硫完全反应时转移的电子数均为 B、中含有的阴、阳离子数共 C、醋酸铵溶液呈中性,则的醋酸铵溶液中数为 D、中键数为
-
12、《哪吒2之魔童闹海》中太乙真人使用藕粉为哪吒和敖丙重塑肉身。尼克酸是藕的主要成分之一,其结构如图所示
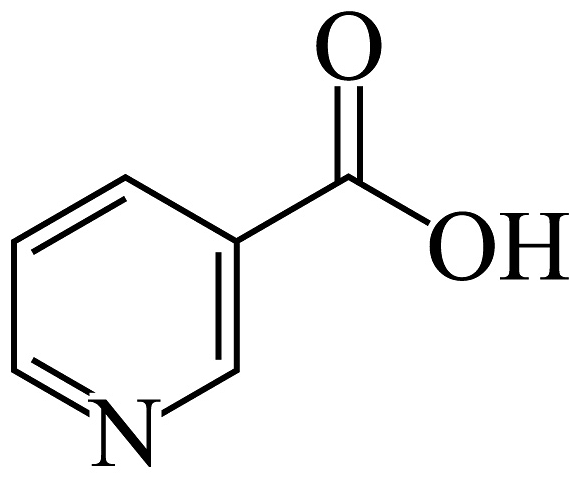 (
( 与苯环相似)。下列说法错误的是 A、尼克酸分子中有两个手性碳原子 B、尼克酸的分子式为 C、尼克酸的所有原子可能共平面 D、尼克酸能发生取代、加成和氧化反应
与苯环相似)。下列说法错误的是 A、尼克酸分子中有两个手性碳原子 B、尼克酸的分子式为 C、尼克酸的所有原子可能共平面 D、尼克酸能发生取代、加成和氧化反应 -
13、1727年,英国的化学家哈尔斯用氯化铵与石灰的混合物合成了氨气。以下实验难以达到预期目的的是


A.制备
B.干燥


C.尾气处理
D.喷泉实验
A、A B、B C、C D、D -
14、从海带中提取碘的过程如下,其中操作为
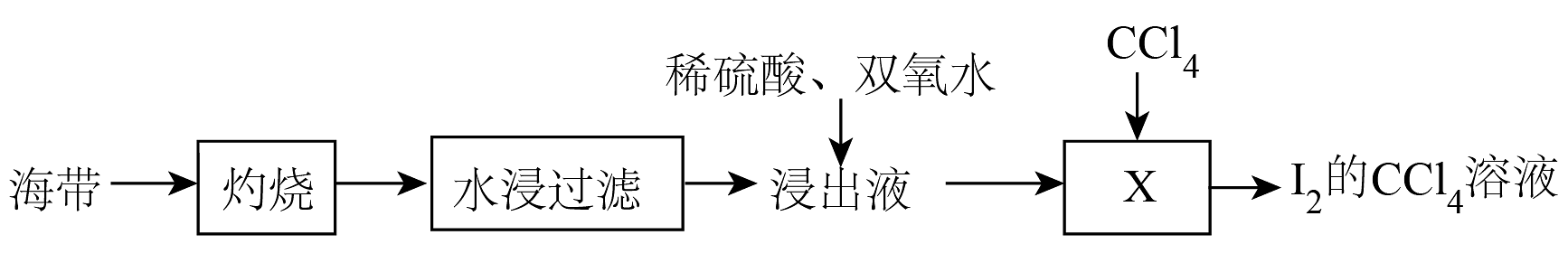 A、过滤 B、蒸馏 C、结晶 D、萃取
A、过滤 B、蒸馏 C、结晶 D、萃取 -
15、“华龙一号”标志着中国进入核电技术先进国家行列。下列说法正确的是A、蒸汽发生器中水吸收热量变成蒸汽:共价键被破坏 B、碳化硼用作核反应堆的控制棒:碳化硼含极性共价键 C、用低浓缩铀()制成燃料棒:的中子数为92 D、汽轮机高速运转使发电机发电:该过程机械能转化为化学能
-
16、中国是农业大国,粮食安全是国家安全的重要部分。下列说法不正确的是A、水稻种子中含有淀粉,淀粉属于高分子 B、收割机的割刀为铁合金,该合金比纯铁硬度大 C、“秸秆炭化,草灰还田”,草木灰可以用作钾肥 D、CuSO4可制备杀菌剂波尔多液,因为SO能使蛋白质变性
-
17、蛇是十二生肖之一,下列有关蛇的历史文物中,主要材质为金属材料的是


A.商周石蛇
B.春秋蛇纹铜提链罐

C.唐彩绘生肖蛇陶俑
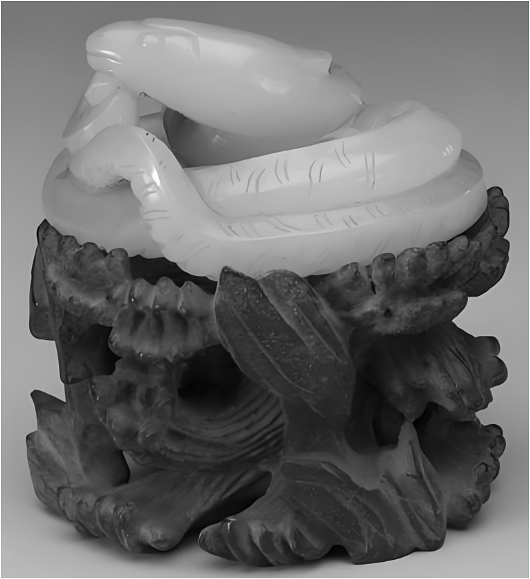
D.清青玉十二辰-蛇
A、A B、B C、C D、D -
18、化合物A仅含碳、硫两种元素。为测定化合物A中碳、硫元素的含量,某化学兴趣小组进行了如下实验:
步骤Ⅰ:取10.00 g化合物A固体,充分加热至完全分解,得到混合气体X;
步骤Ⅱ:为除去混合气体X中的SO2 , 将混合气体X通入足量酸性高锰酸钾溶液充分反应;
步骤Ⅲ:再将剩余气体通入足量Ca(OH)2溶液充分反应,测得质量增加了1.32 g。
已知SO2与Mn的反应如下:5SO2+2Mn+2H2O=5S+2Mn2++4H+。
请计算:
(1)、混合气体中CO2的物质的量为mol。(2)、物质A中碳元素的质量分数为。(3)、下列实验方案中,能测定化合物A中硫的质量分数的是。A.将混合气体通入Ba(OH)2溶液充分反应,过滤、洗涤、干燥,得a g固体。经计算,测得化合物A中硫的质量分数w(S)=
B.将混合气体通入H2O2和BaCl2混合溶液充分反应,过滤、洗涤、干燥,得b g固体。经计算,测得化合物A中硫的质量分数w(S)=
C.将混合气体通入酸性KMnO4溶液充分反应,共消耗c mol的酸性KMnO4溶液。经计算,测得化合物A中硫的质量分数w(S)=
-
19、某种石头块的有效成分为碳酸钙,测得其中碳酸钙含量的操作加下(设该岩石中的其他成分不与盐酸或氢氧化钠反应):
①将一粒研碎过后的石头块(0.10 g)放置烧杯中;
②配制0.10 mol·L-1稀盐酸和 0.10 mol·L-1 NaOH溶液;
③用0.10 mol·L-1 NaOH溶液中和过量的稀盐酸,记录所消耗氢氧化钠溶液的体积;
④加入25 mL 0.10 mol·L-1稀盐酸,使石头完全溶解。
请回答下列问题:
(1)、“步骤④”中发生反应的离子方程式为。(2)、正确的操作顺序为(填序号)①→___________→___________→___________。
(3)、在“配制0.10 mol·L-1稀盐酸”时,下列实验仪器不需要用到的是___________。A、 B、
B、 C、
C、 D、
D、 (4)、该测定实验共进行了4次。实验室现有50 mL、100 mL、250 mL、500 mL 4种规格的容量瓶,则配制盐酸选用的容量瓶规格为。(5)、某同学用容量瓶配制盐酸,其他操作均正确,仅定容时仰视容量瓶上的刻度线,会导致最终测得岩石中碳酸钙的质量分数(填“偏大”“偏小”或“不变”)。
(4)、该测定实验共进行了4次。实验室现有50 mL、100 mL、250 mL、500 mL 4种规格的容量瓶,则配制盐酸选用的容量瓶规格为。(5)、某同学用容量瓶配制盐酸,其他操作均正确,仅定容时仰视容量瓶上的刻度线,会导致最终测得岩石中碳酸钙的质量分数(填“偏大”“偏小”或“不变”)。 -
20、氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。

请回答:
(1)、工业生成中为了盛装大量浓硝酸,可选择___________作为罐体材料。A、铁 B、铜 C、镁 D、铝(2)、氧化炉中发生反应的化学方程式为。(3)、下列说法正确的是___________。A、工业上可增加“合成塔”中催化剂用量,使H2的转化率提升到100% B、“氨分离器”中主要应用了氨气易液化的性质 C、向吸收塔里通入A的目的是将NO转化为NO2 D、为避免硝酸生成尾气中的氮氧化物污染空气,可将其点燃处理(4)、NH3可将氮氧化物还原成N2 , 该过程中氮氧化物体现的性质是性。