相关试卷
-
1、 乙二醇是一种重要化工原料,以合成气为原料合成乙二醇具有重要意义。
Ⅰ.直接合成法: , 不同温度下平衡常数如下表所示。
温度
298K
355K
400K
平衡常数
10
(1)、该反应的0(填“>”或“<”)。(2)、已知的燃烧热分别为 , 则上述合成反应的(用a、b和c表示)。(3)、实验表明,在500K时,即使压强(34MPa)很高乙二醇产率(7%)也很低,可能的原因是(答出1条即可)。Ⅱ.间接合成法:用合成气和制备的DMO合成乙二醇,发生如下3个均放热的连续反应,其中MG生成乙二醇的反应为可逆反应。
 (4)、在2MPa、催化、固定流速条件下,发生上述反应,初始氢酯比 , 出口处检测到DMO的实际转化率及MG、乙二醇、乙醇的选择性随温度的变化曲线如图所示[某物质的选择性]。
(4)、在2MPa、催化、固定流速条件下,发生上述反应,初始氢酯比 , 出口处检测到DMO的实际转化率及MG、乙二醇、乙醇的选择性随温度的变化曲线如图所示[某物质的选择性]。
①已知曲线Ⅱ表示乙二醇的选择性,则曲线(填图中标号,下同)表示DMO的转化率,曲线表示MG的选择性。
②有利于提高A点DMO转化率的措施有(填标号)。
A.降低温度 B.增大压强
C.减小初始氢酯比 D.延长原料与催化剂的接触时间
③483K时,出口处的值为(精确至0.01)。
④A点反应的浓度商(用物质的量分数代替浓度计算,精确至0.001)。
-
2、 某实验小组采用如下方案实现了对甲基苯甲酸的绿色制备。
反应:

步骤:
Ⅰ.向反应管中加入0.12g对甲基苯甲醛和1.0mL丙酮,光照,连续监测反应进程。
Ⅱ.5h时,监测结果显示反应基本结束,蒸去溶剂丙酮,加入过量稀NaOH溶液,充分反应后,用乙酸乙酯洗涤,弃去有机层。
Ⅲ.用稀盐酸调节水层后,再用乙酸乙酯萃取。
Ⅳ.用饱和食盐水洗涤有机层,无水干燥,过滤,蒸去溶剂,得目标产物。
回答下列问题:
(1)、相比作氧化剂,该制备反应的优点为、(答出2条即可)。(2)、根据反应液的核磁共振氢谱(已去除溶剂H的吸收峰,谱图中无羧基H的吸收峰)监测反应进程如下图。已知峰面积比 , 。反应2h时,对甲基苯甲醛转化率约为%。 (3)、步骤Ⅱ中使用乙酸乙酯洗涤的目的是。(4)、步骤Ⅲ中反应的离子方程式为、。(5)、用同位素示踪法确定产物羧基O的来源。丙酮易挥发,为保证气氛,通前,需先使用“循环冷冻脱气法”排出装置中(空气中和溶剂中)的 , 操作顺序为:①→②→→→(填标号),重复后四步操作数次。
(3)、步骤Ⅱ中使用乙酸乙酯洗涤的目的是。(4)、步骤Ⅲ中反应的离子方程式为、。(5)、用同位素示踪法确定产物羧基O的来源。丙酮易挥发,为保证气氛,通前,需先使用“循环冷冻脱气法”排出装置中(空气中和溶剂中)的 , 操作顺序为:①→②→→→(填标号),重复后四步操作数次。
同位素示踪结果如下表所示,则目标产物中羧基O来源于醛基和。
反应条件
质谱检测目标产物相对分子质量
太阳光, , 室温, , 5h
138
太阳光,空气,室温, , 5h
136
-
3、 某工厂采用如下工艺回收废渣(含有ZnS、、FeS和CuCl)中的Zn、Pb元素。

已知:①“氧化浸出”时,不发生变化,ZnS转变为;
②;
③酒石酸(记作)结构简式为。
回答下列问题:
(1)、分子中手性碳原子数目为。(2)、“氧化浸出”时,过二硫酸根转变为(填离子符号)。(3)、“氧化浸出”时,浸出率随温度升高先增大后减小的原因为。(4)、“除铜”步骤中发生反应的离子方程式为。(5)、滤渣2中的金属元素为(填元素符号)。(6)、“浸铅”步骤,和反应生成PbA。PbA产率随体系pH升高先增大的原因为 , pH过高可能生成(填化学式)。(7)、290℃“真空热解”生成2种气态氧化物,该反应的化学方程式为。 -
4、 室温下,将置于溶液中,保持溶液体积和N元素总物质的量不变,pX-pH曲线如图,和的平衡常数分别为和:的水解常数。下列说法错误的是( )
 A、Ⅲ为的变化曲线 B、D点: C、 D、C点:
A、Ⅲ为的变化曲线 B、D点: C、 D、C点: -
5、 一定条件下,“”4种原料按固定流速不断注入连续流动反应器中,体系pH-t振荡图像及涉及反应如下。其中AB段发生反应①~④,①②为快速反应。下列说法错误的是( )

①
②
③
④
⑤
A、原料中不影响振幅和周期 B、反应④: C、反应①~④中,对的氧化起催化作用 D、利用pH响应变色材料,可将pH振荡可视化 -
6、 一种基于的储氯电池装置如图,放电过程中a、b极均增重。若将b极换成Ag/AgCl电极,b极仍增重。关于图中装置所示电池,下列说法错误的是( )
 A、放电时向b极迁移 B、该电池可用于海水脱盐 C、a极反应: D、若以Ag/AgCl电极代替a极,电池将失去储氯能力
A、放电时向b极迁移 B、该电池可用于海水脱盐 C、a极反应: D、若以Ag/AgCl电极代替a极,电池将失去储氯能力 -
7、 化学需氧量(COD)是衡量水体中有机物污染程度的指标之一,以水样消耗氧化剂的量折算成消耗的量(单位为)来表示。碱性不与反应,可用于测定含Cl-水样的COD,流程如图。

下列说法错误的是( )
A、Ⅱ中发生的反应有 B、Ⅱ中避光、加盖可抑制被氧化及的挥发 C、Ⅲ中消耗的越多,水样的COD值越高 D、若Ⅰ中为酸性条件,测得含水样的COD值偏高 -
8、 某工厂利用生物质(稻草)从高锰钴矿(含和少量)中提取金属元素,流程如图。已知“沉钴”温度下 , 下列说法错误的是( )
 A、硫酸用作催化剂和浸取剂 B、使用生物质的优点是其来源广泛且可再生 C、“浸出”时,3种金属元素均被还原 D、“沉钴”后上层清液中
A、硫酸用作催化剂和浸取剂 B、使用生物质的优点是其来源广泛且可再生 C、“浸出”时,3种金属元素均被还原 D、“沉钴”后上层清液中 -
9、 人体皮肤细胞受到紫外线(UV)照射可能造成DNA损伤,原因之一是脱氧核苷上的碱基发生了如下反应。下列说法错误的是( )
 A、该反应为取代反应 B、Ⅰ和Ⅱ均可发生酯化反应 C、Ⅰ和Ⅱ均可发生水解反应 D、乙烯在UV下能生成环丁烷
A、该反应为取代反应 B、Ⅰ和Ⅱ均可发生酯化反应 C、Ⅰ和Ⅱ均可发生水解反应 D、乙烯在UV下能生成环丁烷 -
10、 晶体因x变化形成空位而导致颜色各异,当时,其立方晶胞结构如图。设为阿伏加德罗常数的值,下列说法错误的是( )
 A、与W最近且等距的O有6个 B、x增大时,W的平均价态升高 C、密度为时, D、空位数不同,吸收的可见光波长不同
A、与W最近且等距的O有6个 B、x增大时,W的平均价态升高 C、密度为时, D、空位数不同,吸收的可见光波长不同 -
11、 巧设实验,方得真知。下列实验设计合理的是( )
A.除去中的HCl
B.制备少量NO避免其被氧化


C.用乙醇萃取中的S
D.制作简易氢氧燃料电池

 A、A B、B C、C D、D
A、A B、B C、C D、D -
12、 化学家用无机物甲成功制备了有机物乙 , 开创了有机化学人工合成的新纪元。其中W、X、Y、Z原子序数依次增大,X、Y、Z同周期,基态X、Z原子均有2个单电子。下列说法正确的是( )A、第一电离能:Z>Y>X B、甲中不存在配位键 C、乙中键和键的数目比为 D、甲和乙中X杂化方式分别为和
-
13、 微粒邂逅时的色彩变化是化学馈赠的视觉浪漫。下列对颜色变化的解释错误的是( )
选项
颜色变化
解释
A
空气中灼烧过的铜丝伸入乙醇中,黑色铜丝恢复光亮的紫红色
=
B
悬浊液中加入溶液,固体由白色变为红褐色
=
C
溶液中加入 , 浅绿色溶液出现蓝色浑浊
=
D
溶液中加入NaOH溶液,溶液由橙色变为黄色
A、A B、B C、C D、D -
14、 一种强力胶的黏合原理如下图所示。下列说法正确的是( )
 A、Ⅰ有2种官能团 B、Ⅱ可遇水溶解使黏合物分离 C、常温下Ⅱ为固态 D、该反应为缩聚反应
A、Ⅰ有2种官能团 B、Ⅱ可遇水溶解使黏合物分离 C、常温下Ⅱ为固态 D、该反应为缩聚反应 -
15、 钠及其化合物的部分转化关系如图。设为阿伏加德罗常数的值,下列说法正确的是( )
 A、反应①生成的气体,每11.2L(标准状况)含原子的数目为 B、反应②中2.3gNa完全反应生成的产物中含非极性键的数目为 C、反应③中与足量反应转移电子的数目为 D、溶液中,的数目为
A、反应①生成的气体,每11.2L(标准状况)含原子的数目为 B、反应②中2.3gNa完全反应生成的产物中含非极性键的数目为 C、反应③中与足量反应转移电子的数目为 D、溶液中,的数目为 -
16、 可用于水的杀菌消毒,遇水发生反应:。下列说法正确的是( )A、反应中各分子的键均为键 B、反应中各分子的VSEPR模型均为四面体形 C、键长小于H—O键长 D、HClO分子中Cl的价电子层有2个孤电子对
-
17、 侯氏制碱法突破西方技术垄断,推动了世界制碱技术的发展,其主要反应为NaCl+。下列有关化学用语或说法正确的是( )A、的电子式:
 B、的空间结构:直线形
C、的晶体类型:离子晶体
D、溶解度:
B、的空间结构:直线形
C、的晶体类型:离子晶体
D、溶解度:
-
18、 东北三省及内蒙古资源丰富,下列资源转化的主要过程不属于化学变化的是( )A、石灰石煅烧 B、磁铁矿炼铁 C、煤的液化 D、石油分馏
-
19、巴洛沙韦酯K(
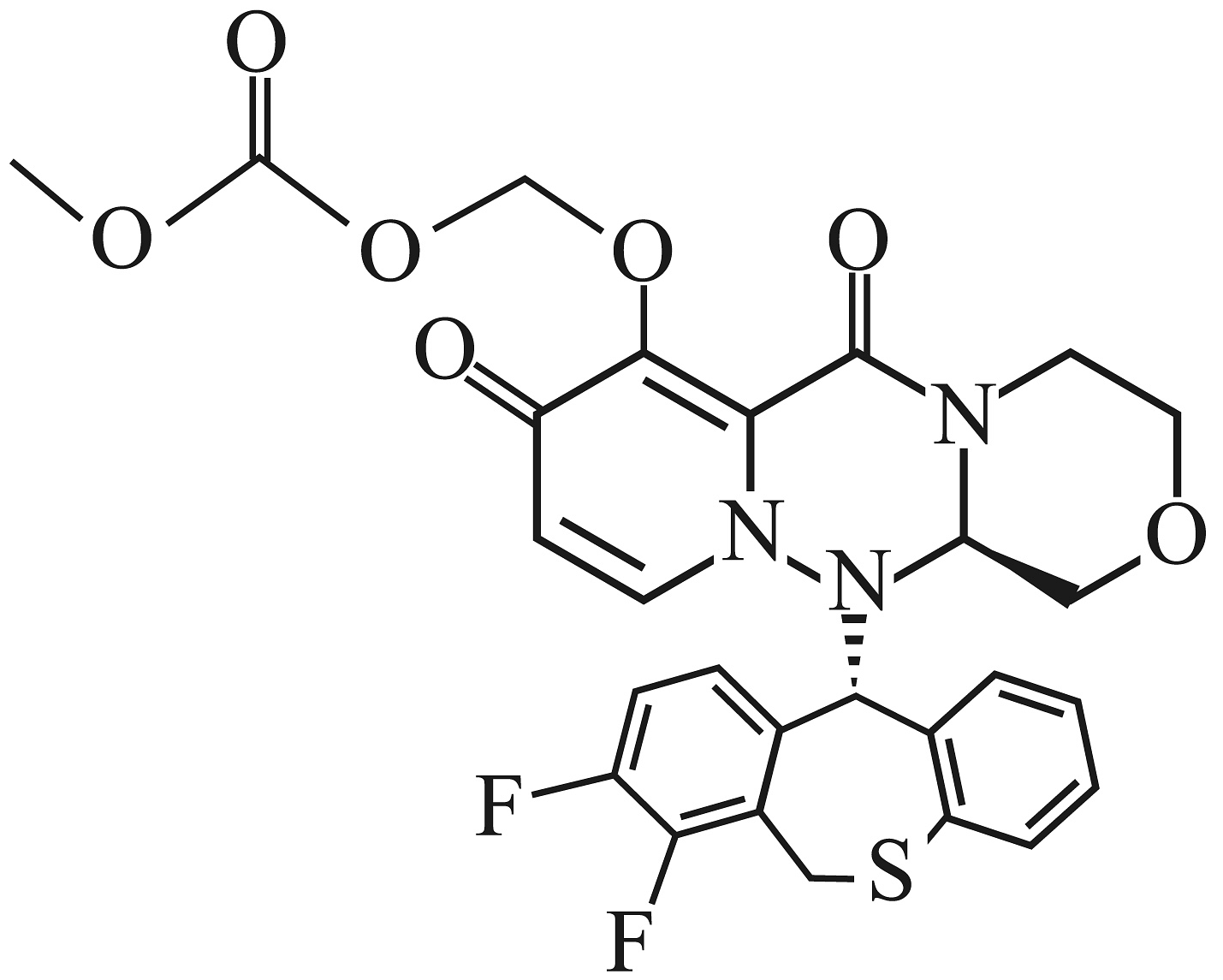 )能抑制流感病毒帽状依赖型核酸内切酶,从而抑制病毒的合成。其部分优化路线如下:
)能抑制流感病毒帽状依赖型核酸内切酶,从而抑制病毒的合成。其部分优化路线如下: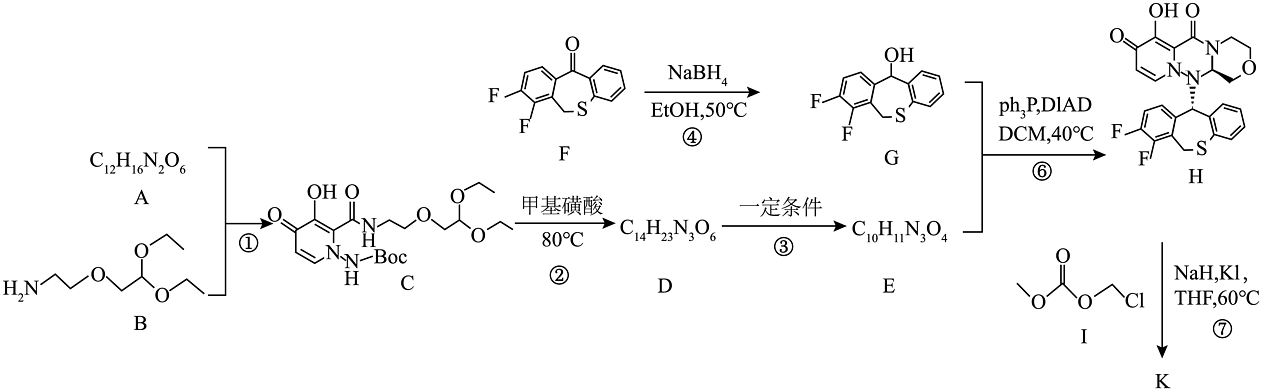
已知:①是叔丁氧羰基的缩写,甲基磺酸条件下容易脱去。
②
 。
。③
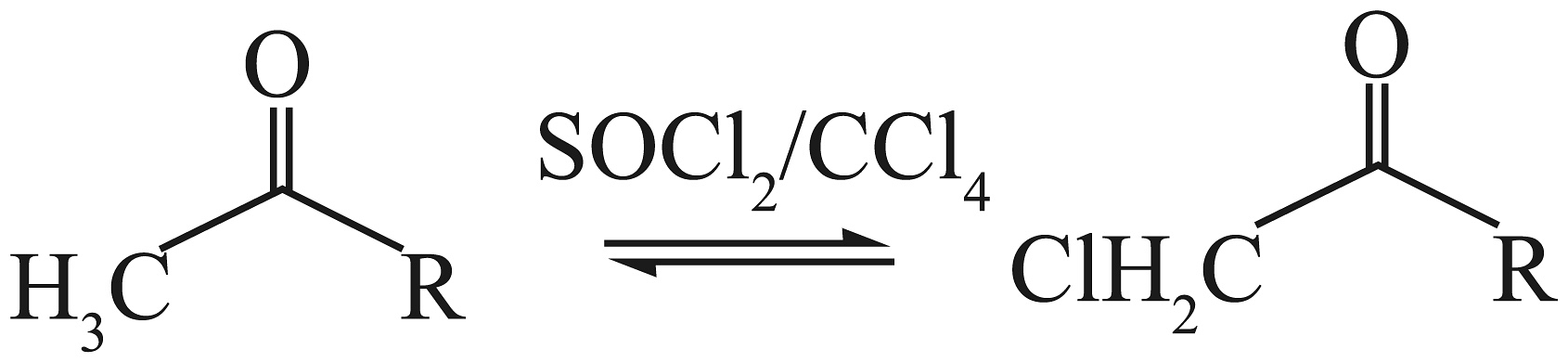 。(1)、化合物B中的官能团名称是。(2)、化合物A的结构简式为。(3)、写出过程③的化学方程式。(4)、下列说法正确的是____________。A、化合物G可发生水解、消去反应 B、过程②可能会生成 C、过程④为还原反应,产生手性碳原子 D、K的分子式为(5)、写出同时符合下列条件的化合物G的4种同分异构体的结构简式。
。(1)、化合物B中的官能团名称是。(2)、化合物A的结构简式为。(3)、写出过程③的化学方程式。(4)、下列说法正确的是____________。A、化合物G可发生水解、消去反应 B、过程②可能会生成 C、过程④为还原反应,产生手性碳原子 D、K的分子式为(5)、写出同时符合下列条件的化合物G的4种同分异构体的结构简式。①含有结构
②能发生银镜反应的芳香族化合物,苯环上有4个取代基,不直接与F原子相连,且含
 基团
基团③核磁共振氢谱显示含4种不同环境的H原子
(6)、乙醛和L( )为原料可合成化合物B,利用已知信息和流程路线中的相关信息,设计合成路线(用流程图表示,无机试剂任选)。
)为原料可合成化合物B,利用已知信息和流程路线中的相关信息,设计合成路线(用流程图表示,无机试剂任选)。 -
20、甘氨酸亚铁是一种新型的铁营养强化剂。实验室制备甘氨酸亚铁部分装置如下图(夹持和加热、搅拌仪器已省略)。
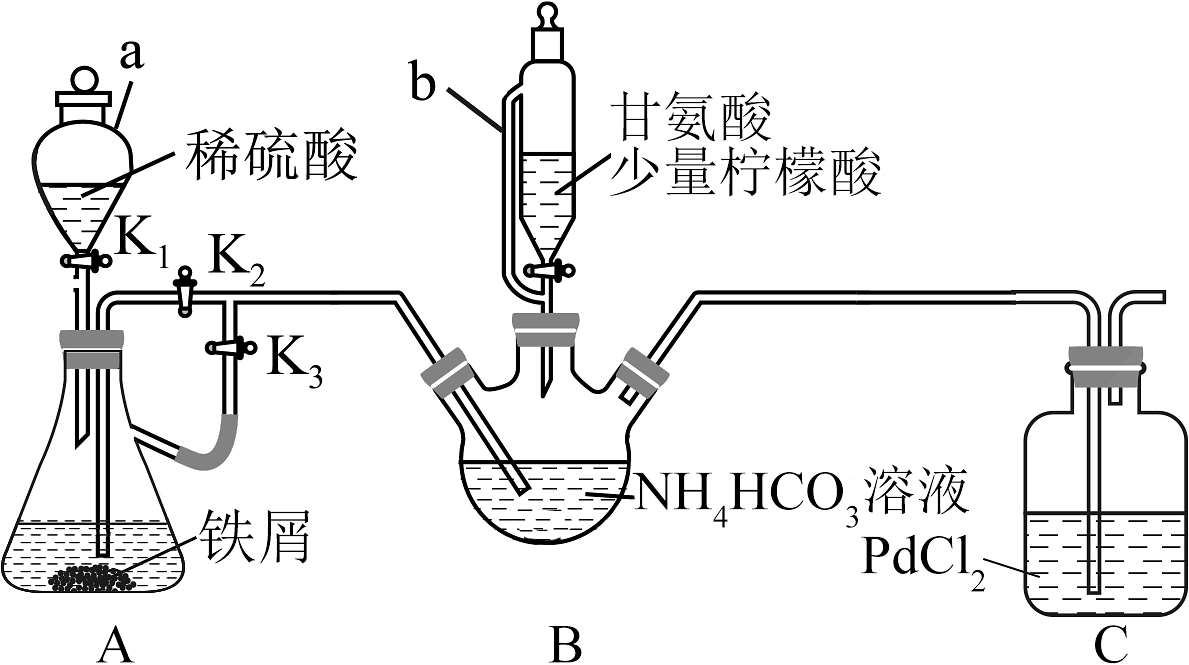
已知:
i.柠檬酸易溶于水和乙醇,有弱酸性和还原性。
ii.易溶于水,难溶于乙醇。
iii.通入溶液中的反应:(黑色)
实验步骤:
Ⅰ.关闭活塞 , 打开活塞和 , 加入适量稀硫酸(铁屑足量),当出现____________现象后关闭活塞。
Ⅱ.____________,磁力搅拌器不断搅拌,B中生成沉淀。
Ⅲ.在恒温条件下继续磁力搅拌,然后向B中滴加甘氨酸和柠檬酸溶液,调节溶液至5.5左右,使反应物充分反应。
Ⅳ.反应完成后,向B的反应混合物中加入无水乙醇,生成白色沉淀,将沉淀过滤、洗涤得到粗产品,将粗产品纯化后得精品。
回答下列问题:
(1)、仪器b的名称为。(2)、步骤Ⅰ中横线处的现象是。(3)、下列说法正确的是____________。A、步骤Ⅰ中的铁屑可以改为铁粉,从而加快反应速率 B、步骤Ⅱ横线处操作为:关闭 , 打开 , 将A中溶液压入到B中 C、步骤Ⅲ可以用水浴加热 D、步骤Ⅳ中洗涤剂可以用冰水(4)、写出B中生成甘氨酸亚铁的化学方程式。(5)、步骤Ⅲ中加入少量柠檬酸的一个作用是能调节溶液促进溶解,另一个作用是。(6)、已知甘氨酸亚铁的结构为: , 请分析,等浓度溶液导电能力远弱于溶液的原因。
, 请分析,等浓度溶液导电能力远弱于溶液的原因。