相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、氮及其化合物的转化过程和能量变化如图,下列分析错误的是
 A、过程I中,发生反应的化学方程式为 B、由图可知,过程I发生的总反应为放热反应 C、过程Ⅱ中,没有伴随着能变化 D、使用催化剂是为了增大反应速率,提高生产效率
A、过程I中,发生反应的化学方程式为 B、由图可知,过程I发生的总反应为放热反应 C、过程Ⅱ中,没有伴随着能变化 D、使用催化剂是为了增大反应速率,提高生产效率 -
2、我国在科技领域取得重大成就。下列说法错误的是A、墨子巡天望远镜主镜上面银色的铝反射膜属于金属材料 B、制造中国天眼使用的碳化硅陶瓷属于新型无机非金属材料 C、新能源汽车领域使用的高导热率氮化铝陶瓷属于金属材料 D、高纯可制成芯片,广泛运用于信息技术和新能源技术领域
-
3、氯及其化合物在生产、生活中都有重要的用途,下列说法正确的是A、新制氯水光照下容易分解产生 , 需用棕色瓶密封保存 B、电解氯化钠溶液可以得到金属钠和氯气 C、漂白粉比稳定,可露置在空气中长期保存 D、由和直接化合可制得
-
4、物质类别与元素价态是学习元素及其化合物性质的重要认识视角。下图是硫元素的“价类二维图”,其中焰色反应均显黄色。有关叙述错误的是
 A、a分别与反应,都可以生成b B、e的浓溶液和稀溶液均具有氧化性 C、f溶液久置于空气中会生成g D、将d的稀溶液滴入紫色石蕊溶液中,溶液先变红后褪色
A、a分别与反应,都可以生成b B、e的浓溶液和稀溶液均具有氧化性 C、f溶液久置于空气中会生成g D、将d的稀溶液滴入紫色石蕊溶液中,溶液先变红后褪色 -
5、某同学整理铁及其化合物的有关知识,其中错误的是A、可用溶液检验溶液是否变质 B、红热的铁能与水蒸气发生反应,生成铁红和氢气 C、氯化铁溶液可以和铜反应,可利用该反应来制作印刷电路板 D、常温下,铁制容器盛放浓硝酸,原因是表面被浓硝酸氧化
-
6、如图是某硫酸试剂标签上的部分内容。某学生用该试剂配制溶液,下列说法正确的是
硫酸化学纯(级)
品名:硫酸
化学式:
相对分子质量:98
密度:
质量分数:
A、容量瓶用蒸馏水洗涤,干燥后才能使用 B、定容时俯视刻度线,则所配溶液浓度偏低 C、该试剂瓶中硫酸溶液的物质的量浓度为 D、向容量瓶转移液体时,玻璃棒下端应在容量瓶刻度线以下 -
7、为阿伏加德罗常数的值,下列说法正确的是A、中含有的中子数为 B、任何物质都含有个原子 C、标准状况下,水中含有分子个数为 D、变为时失去的电子数为
-
8、能正确表示下列反应的离子方程式的是A、钠与水反应: B、石灰石中加入稀盐酸: C、铜溶于浓硝酸中: D、将通入足量的氢氧化钠溶液中:
-
9、劳动创造幸福,实干成就伟业。下列劳动项目与所涉及化学知识不相符的是
选项
劳动项目
化学知识
A
科研人员研发用于汽车的氢气燃料电池
电池驱动汽车是化学能直接转变为动能
B
蒸制糕点加小苏打粉作膨松剂
小苏打受热分解产生
C
利用豆科植物作绿肥进行施肥
豆科植物可以实现自然固氮
D
家庭里用“84消毒液”杀菌消毒
具有强氧化性
A、A B、B C、C D、D -
10、化学与人类社会的生产、生活有着密切联系。下列叙述错误的是A、不溶于水,可用作医疗上检查肠胃的钡餐 B、人类通过物质的燃烧获取热能,燃烧是放热反应 C、铝锅不易生锈,可用来长时间存放酸性、碱性食物 D、葡萄酒中添加适量 , 可以起到杀菌和抗氧化作用
-
11、分类观和价态观是研究物质性质的两个重要维度,氮元素的价类二维图如图所示,下列说法错误的是
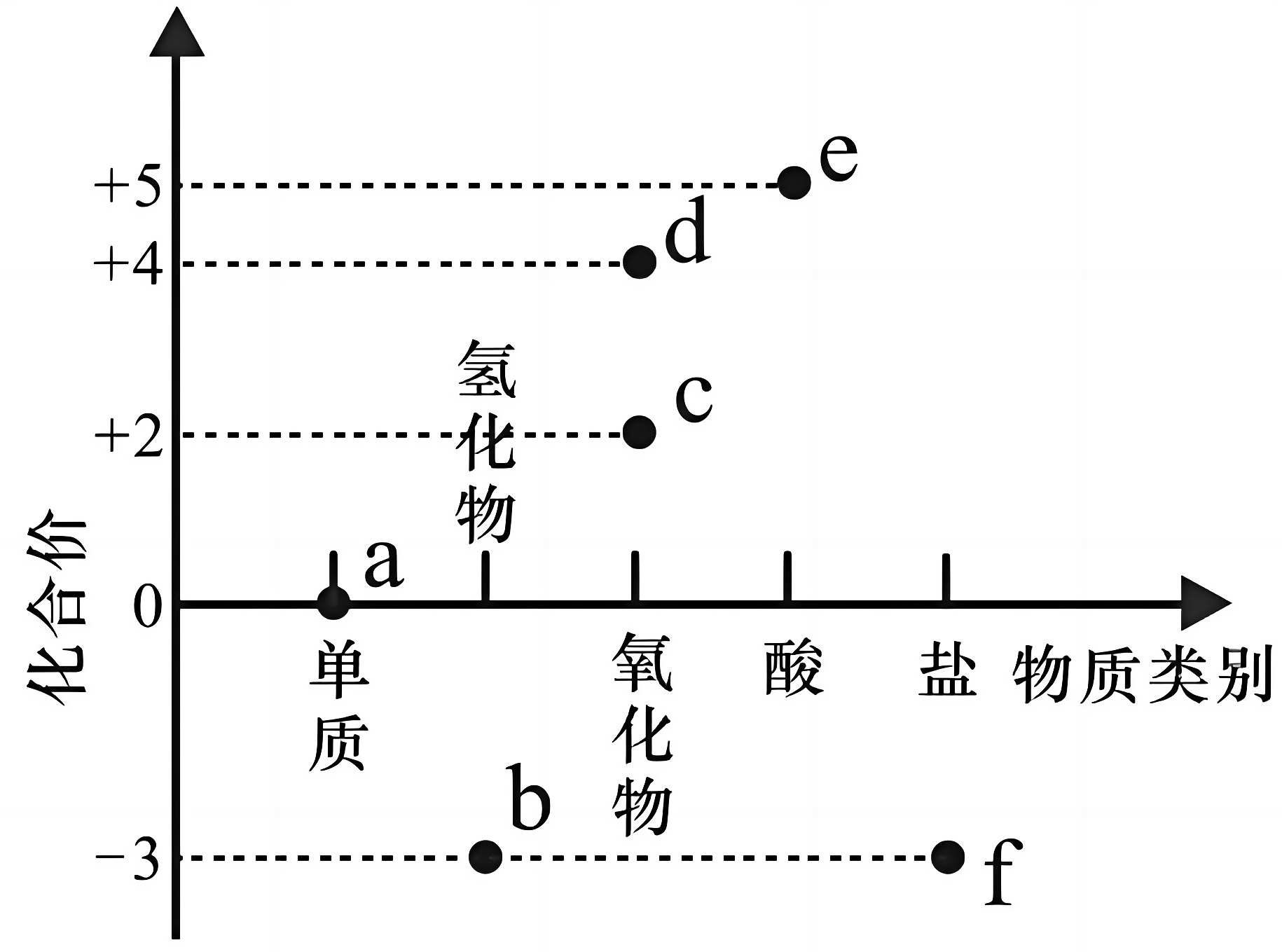 A、c、d都不是酸性氧化物 B、“雷雨发庄稼”转化过程:a→c→d→e C、b与e反应生成f的过程属于固氮反应 D、绝大多数f易溶于水,受热易分解
A、c、d都不是酸性氧化物 B、“雷雨发庄稼”转化过程:a→c→d→e C、b与e反应生成f的过程属于固氮反应 D、绝大多数f易溶于水,受热易分解 -
12、某澄清透明溶液中可能含有K+ , Na+ , H+ , , 、Cl﹣中的若干种,且各离子数目相等。为了确定溶液的组成,设计了如图检验流程:

下列说法错误的是
A、原溶液中一定存在Na+、K+ B、原溶液中可能存在 C、气体W为CO2 , 白色沉淀X为AgCl D、向原溶液中滴加澄清石灰水溶液变浑浊 -
13、下列相关反应的离子方程式书写错误的是A、盐酸除铁锈: B、碳酸氢钠溶液与氢氧化钠溶液混合: C、向氯化钠溶液中加入盐酸除去含有的 D、向硝酸银溶液中滴加盐酸:
-
14、以铅精矿(含 , 等)为主要原料提取金属和的工艺流程如下:

回答下列问题:
(1)、“热浸”时,难溶的和转化为和及单质硫。溶解等物质的量的和时,消耗物质的量之比为;溶液中盐酸浓度不宜过大,除防止“热浸”时挥发外,另一目的是防止产生(填化学式)。(2)、将“过滤Ⅱ”得到的沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属 , “电解I”阳极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为。(3)、“还原”中加入铅精矿的目的是。(4)、“置换”中可选用的试剂X为(填标号)。A. B. C. D.
“置换”反应的离子方程式为。
(5)、“电解II”中将富银铅泥制成电极板,用作(填“阴极”或“阳极”)。 -
15、部分含或或物质的分类与相应化合价关系如图。下列推断合理的是
 A、若a在沸水中可生成e,则a→f的反应一定是化合反应 B、在g→f→e→d转化过程中,一定存在物质颜色的变化 C、加热c的饱和溶液,一定会形成能产生丁达尔效应的红棕色分散系 D、若b和d均能与同一物质反应生成c,则组成a的元素一定位于周期表p区
A、若a在沸水中可生成e,则a→f的反应一定是化合反应 B、在g→f→e→d转化过程中,一定存在物质颜色的变化 C、加热c的饱和溶液,一定会形成能产生丁达尔效应的红棕色分散系 D、若b和d均能与同一物质反应生成c,则组成a的元素一定位于周期表p区 -
16、中国载人登月初步飞行方案公布,计划2030年前实现登月。登月发射使用的火箭是长征9号火箭,火箭采用煤油、液氢、液氧等无毒无污染推进剂。分解水可以制取氢气,分解时的能量变化如图所示。下列有关该反应的说法正确的是
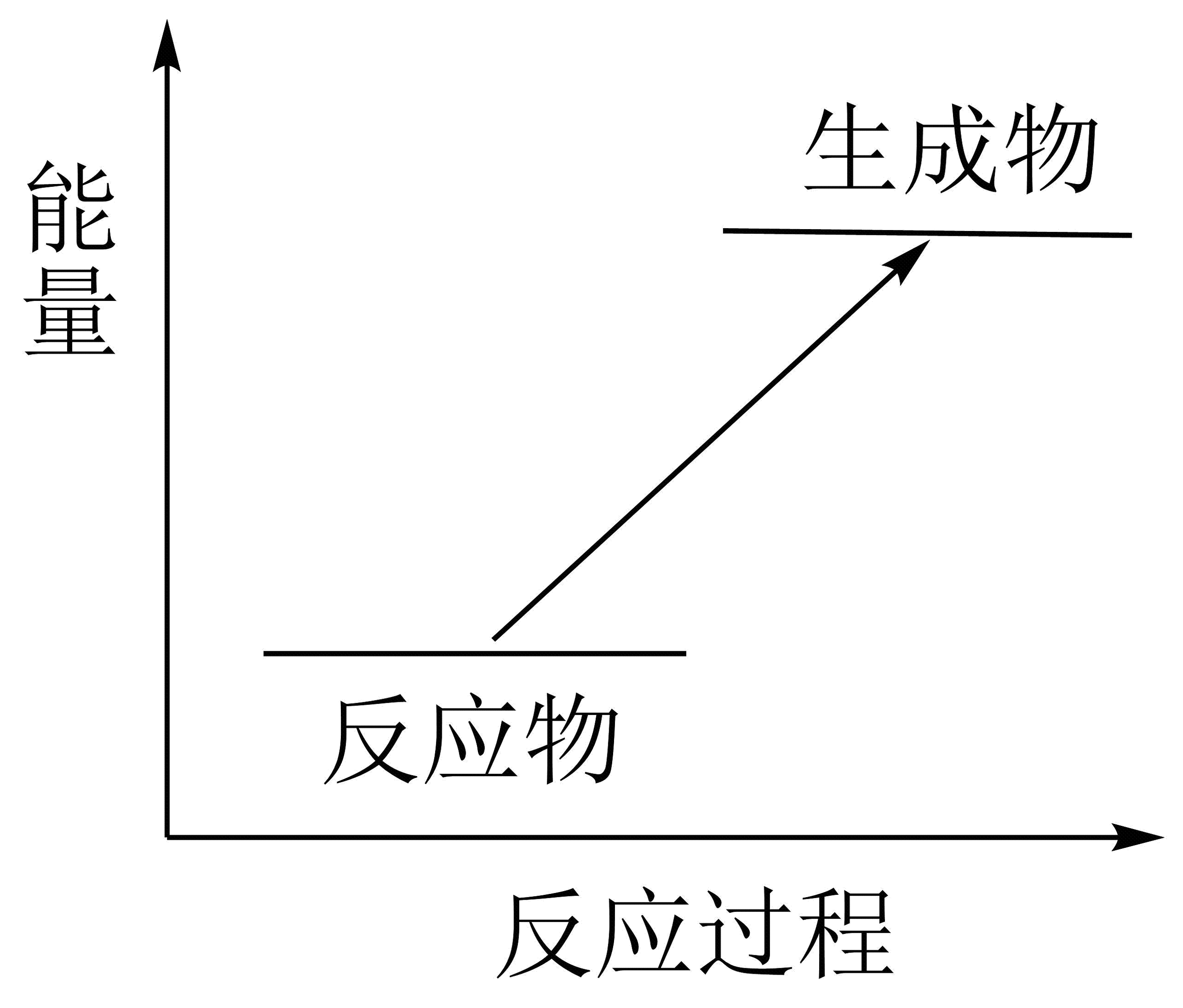 A、断开H-O键放出能量 B、反应物的总键能大于生成物的总键能 C、该条件下生成物比反应物更为稳定 D、寻找合适催化剂可不需要额外提供能量实现分解水
A、断开H-O键放出能量 B、反应物的总键能大于生成物的总键能 C、该条件下生成物比反应物更为稳定 D、寻找合适催化剂可不需要额外提供能量实现分解水 -
17、物质微观结构决定宏观性质,进而影响用途。下列结构或性质不能解释其用途的是
结构或性质
用途
A
具有还原性
可用作自来水的消毒剂
B
甘油结构中含能与水形成氢键的羟基
甘油可用作保湿类护肤品
C
中N≡N键能大
可用作反应的保护气
D
聚乳酸具有生物相溶性和可降解性
聚乳酸可用作手术缝合线
A、A B、B C、C D、D -
18、G是合成一种治疗胃食管反流疾病药物的关键中间体,其合成过程如下。
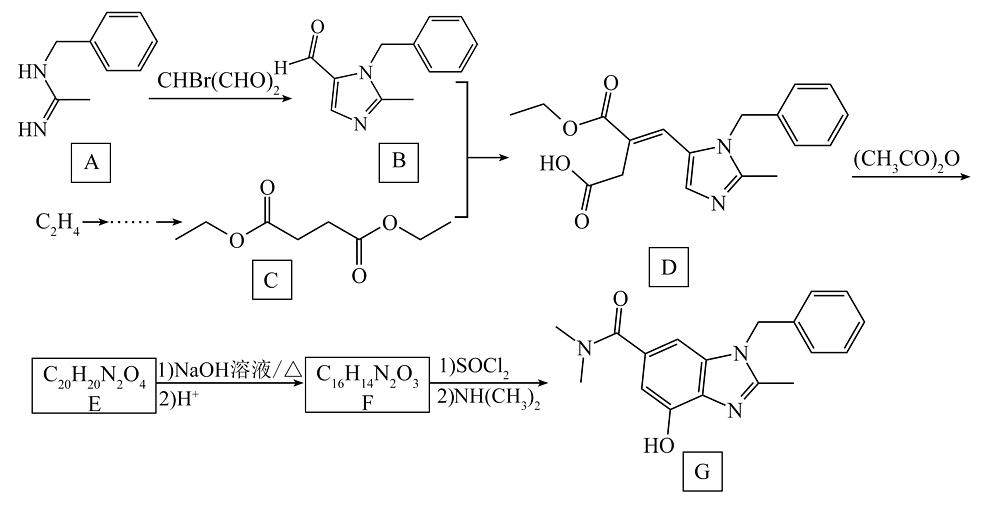
已知:①

②
 不稳定,能快速异构化为
不稳定,能快速异构化为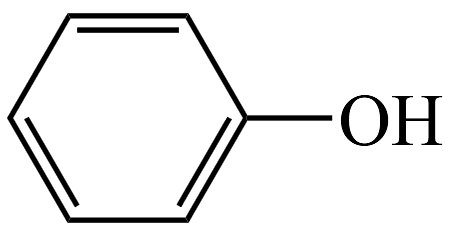
③
请回答:
(1)、中含氧官能团的名称是。(2)、写出B+C→D的化学方程式。(3)、下列说法不正确的是_______。A、在气态下,的碱性强于 B、A→B的过程只有取代反应 C、F→G中的作用是将变为 , 更易与反应 D、G的分子式为(4)、化合物E的结构简式为。(5)、设计以乙烯为原料合成C的路线(用流程图表示,无机试剂任选)。(6)、写出4种同时符合下列条件的化合物A的同分异构体的结构简式。①核磁共振氢谱图显示有5组峰;红外光谱图显示没有氮氮单键。
②除苯环外没有其他环且苯环上有三个取代基。
-
19、利用和生成进而制备连二硫酸钠晶体。相关物质性质见下表。
物质(化学式)
摩尔质量
215
242
主要性质
空气中易分解
空气中不易变质
均可溶于水,时会释放出气体
操作流程如下:
 (1)、实验室采用如图装置制备 , 仪器a的名称为 , 写出步骤II中反应的离于方程式。
(1)、实验室采用如图装置制备 , 仪器a的名称为 , 写出步骤II中反应的离于方程式。 (2)、下列说法不正确的是_______。A、步骤I冰水浴的作用是提高反应液中的浓度 B、为防止反应过于剧烈,步骤II反应分数次缓慢加入 C、步骤III中滴加饱和溶液的目的主要是除去 D、步骤IV的依据是的溶解度大于(3)、将步骤V中正确的仪器或操作的标号填入相应横线上:
(2)、下列说法不正确的是_______。A、步骤I冰水浴的作用是提高反应液中的浓度 B、为防止反应过于剧烈,步骤II反应分数次缓慢加入 C、步骤III中滴加饱和溶液的目的主要是除去 D、步骤IV的依据是的溶解度大于(3)、将步骤V中正确的仪器或操作的标号填入相应横线上:将滤液转移入中,用酒精灯加热,并用玻璃棒不断搅拌→→→洗涤、干燥。
a.坩埚
b.蒸发皿
c.蒸发溶剂至有大量晶体析出
d.浓缩溶液至有少量小晶体析出
e.停止加热,自然冷却,过滤
f.停止加热,利用余热蒸干
(4)、一定条件下,连二硫酸钠可与发生以下反应:某连二硫酸钠晶体的标定纯度(质量分数)为92.0%,为检测其实际纯度,称取样品溶于冷水,配成溶液,移取于锥形瓶中,用的酸性溶液滴定(杂质不参加反应),重复操作3次,消耗酸性溶液的体积见表。
实验次数
第1次
第2次
第3次
消耗溶液体积(mL)
19.92
20.00
20.08
根据以上数据计算该样品的纯度为;若操作无误,所测纯度与标定纯度存在较大差异的原因可能是。
-
20、工业制丙烯的方法有多种,回答下列问题:(1)、直接脱氢反应I: 。压强分别为和时,丙烷平衡转化率与温度的关系如图所示。该反应自发进行的条件是(填“高温”“低温”或“任意温度”),图中表示的关系曲线是(填“a”或“b”)。520℃时,条件下丙烷的平衡转化率Y=%(计算结果保留一位小数)。

[对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平街常数,记作(类似于浓度平衡常数K),如 , p为平衡总压强,x(B)为平衡体系中B的物质的量分数]。
(2)、氧气氧化反应II:①已知: , 则(用含、的式子表示)。
②研究发现丙烷和可在表面通过吸附、断键、成键及脱附等过程进行反应,某研究小组为探究反应II的机理,对进料和过程产品成分进行监测,记录见表。由此推测丙烷催化氧化反应过程的机理可能是(用文字描述)。
实验
进料成分
检测记录
实验I
和
初期气态产物无
实验II
、和
反应过程中无分子
(3)、电化学法制丙烯工作原理如图所示,生成丙烯的电极反应式是。产生丙烯,理论上需电流强度为的铅蓄电池至少工作秒。
已知:电荷量电流时间(s);;。