相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、硫化氢是二元弱酸。某小组做如下两组实验:
实验Ⅰ:往溶液中滴加溶液;
实验Ⅱ:往溶液中滴加溶液。
[已知:的电离平衡常数; , 溶液混合后体积变化忽略不计]。
下列说法正确的是
A、实验I可选用甲基橙(变色的范围)作指示剂,指示反应终点 B、实验I中时,存在 C、实验Ⅱ中发生的主要反应为 D、往实验Ⅱ反应产生的黑色沉淀中加入氨水,黑色沉淀溶解,产生 -
2、2023年诺贝尔化学奖颁发给量子点的发现与研究。其中巯基乙酸是量子点合成过程中的一种保护剂。下列说法不正确的是A、亲水性:羧基巯基 B、酸性:巯基乙酸乙酸 C、与量子点上的过渡金属离子配位的原子是S,结合后水溶性降低 D、与水分子形成的氢键强度:
-
3、根据图示,下列判断不正确的是
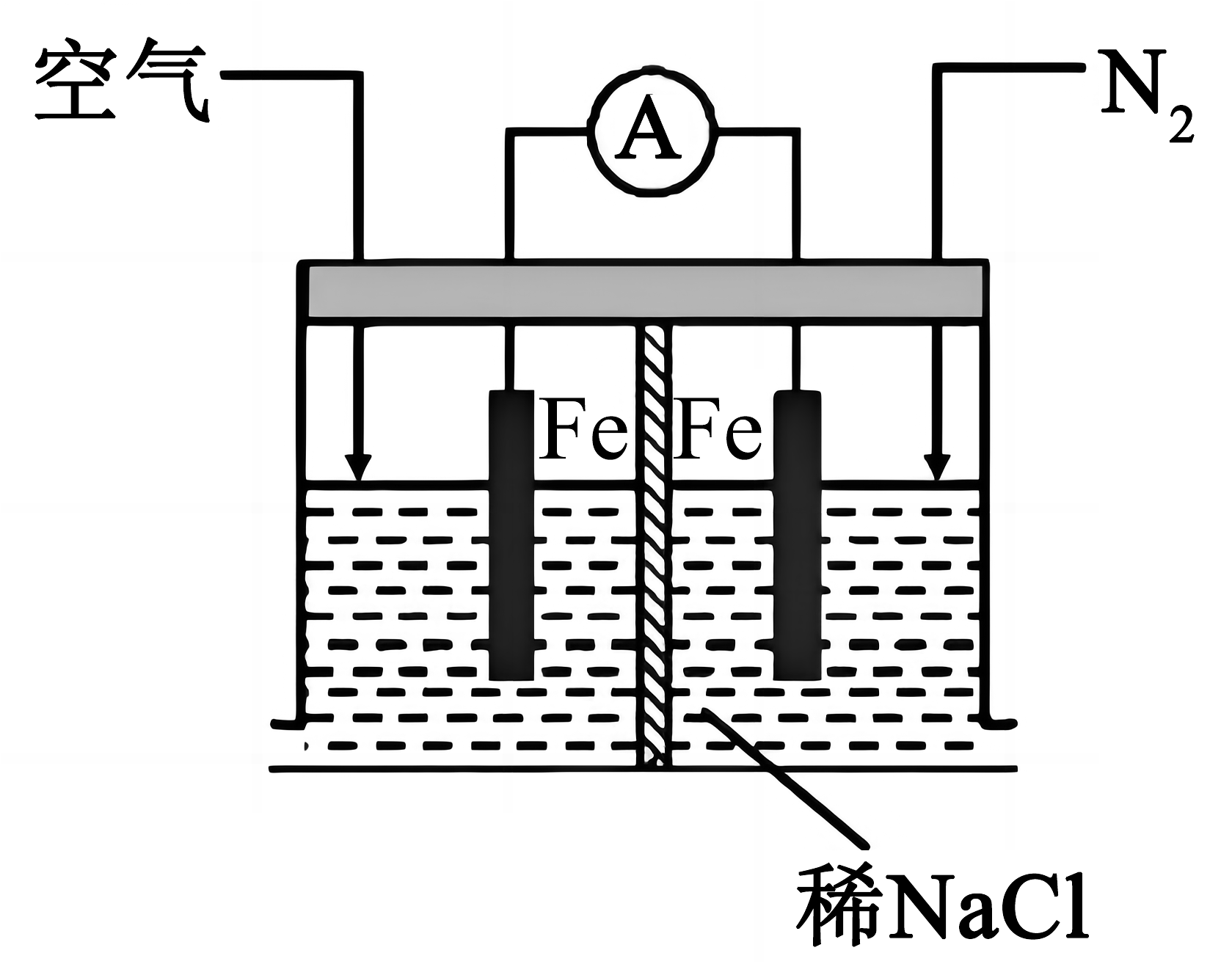 A、该装置为原电池模型 B、过一段时间,左侧溶液的升高 C、该体系中,优先于参与反应 D、腐蚀速率:左侧电极>右侧电极
A、该装置为原电池模型 B、过一段时间,左侧溶液的升高 C、该体系中,优先于参与反应 D、腐蚀速率:左侧电极>右侧电极 -
4、氢是清洁能源,硼氢化钠是一种环境友好的固体储氢材料,其水解生氢反应机理如图所示。

下列说法正确的是
A、此过程的反应说明B的电负性大于H的电负性 B、若用代替 , 至多生成3种气体产物 C、已知反应过程中会发出大量的热,可推测出该反应需在低温条件才可自发进行 D、该反应比较缓慢,可通过升高溶液温度、加入硼酸溶液来加快反应速率 -
5、下列化学反应表示不正确的是A、黄铁矿的燃烧: B、十水碳酸钠与硝酸铵反应: C、酸性溶液测定空气中含量: D、氟磺酸与足量溶液反应:
-
6、有机物A经元素分析仪测得只含碳、氢、氧3种元素,红外光谱显示A分子中存在醚键,质谱和核磁共振氢谱示意图如下。下列关于A的说法正确的是
 A、不能使酸性溶液褪色 B、能与反应生成1-丁醛 C、能与发生酯化反应 D、能与反应生成
A、不能使酸性溶液褪色 B、能与反应生成1-丁醛 C、能与发生酯化反应 D、能与反应生成 -
7、根据材料的组成和结构变化可推测其性能变化,下列推测不合理的是
材料
组成和结构变化
性能变化
A
硫化橡胶
添加炭黑
耐磨性提高
B
用、O取代部分、N
用于制作发光材料
C
石墨
掺杂
电池稳定性增强
D
水泥
加入石膏
调节硬化速率
A、A B、B C、C D、D -
8、为阿伏加德罗常数的值。下列说法不正确的是A、(其分子结构为
 )中共价键的数目为
B、中的的数目为
C、与在密闭容器中充分反应后的分子数小于
D、中存在键
)中共价键的数目为
B、中的的数目为
C、与在密闭容器中充分反应后的分子数小于
D、中存在键
-
9、下列有关实验说法正确的是A、对于含重金属(如铅、汞或镉等)离子的废液,可用或进行沉淀化处理 B、如果不慎将苯酚沾到皮肤上,应立即用大量水冲洗,再用的溶液冲洗 C、向溶液中滴加氨水至难溶物溶解得深蓝色溶液,再加入乙醇,无明显现象 D、滴定用的锥形瓶装待测液前需要保持干燥,并用待测液润洗次
-
10、下列表示不正确的是A、的空间填充模型:
 B、乙炔的结构简式:
C、的水溶液中主要存在的氢键:
B、乙炔的结构简式:
C、的水溶液中主要存在的氢键: D、易燃类物质的标识:
D、易燃类物质的标识:
-
11、下列关于元素及其化合物的性质说法不正确的是A、与铝粉反应会释放出大量气体,可作管道疏通剂 B、具有氧化性,可作暂时性漂白剂 C、酸性比柠檬酸弱,能除去水垢(主要成分为) D、具有腐蚀性和挥发性,使用时应注意防护和通风
-
12、下列物质中属于两性化合物的是A、 B、 C、 D、
-
13、某化合物由原子序数依次增大的短周期主族元素W、X、Y、Z、Q组成(结构如图)。X的最外层电子数等于内层电子数,Y是有机物分子骨架元素,Q和W能形成两种室温下常见的液态化合物。下列说法错误的是
 A、第一电离能: B、该化合物中Q和W之间可形成氢键 C、X与Al元素有相似的性质 D、W、Z、Q三种元素可形成离子化合物
A、第一电离能: B、该化合物中Q和W之间可形成氢键 C、X与Al元素有相似的性质 D、W、Z、Q三种元素可形成离子化合物 -
14、由O、F、I组成化学式为的化合物,能体现其成键结构的片段如图所示。下列说法正确的是
 A、图中O代表F原子 B、该化合物中存在过氧键 C、该化合物中I原子存在孤对电子 D、该化合物中所有碘氧键键长相等
A、图中O代表F原子 B、该化合物中存在过氧键 C、该化合物中I原子存在孤对电子 D、该化合物中所有碘氧键键长相等 -
15、光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。

下列说法错误的是
A、该高分子材料可降解 B、异山梨醇分子中有3个手性碳 C、反应式中化合物X为甲醇 D、该聚合反应为缩聚反应 -
16、
某化学兴趣小组通过实验对硫酸。 氢氧化钙的化学性质进行了验证和总结,如图所示“——”表示物质两两之间能发生化学反应,请据图回答问题。
总结一:硫酸的化学性质

(1)写出氧化铁与硫酸反应的化学方程式:。
(2)请补充一个实验,完善硫酸的化学性质,X可以是(用化学式表示)。
(3)发生中和反应的化学方程式为。
总结二:氢氧化钙的化学性质

(已知:CaCl2溶液呈中性,CaCl2+Na2CO3=CaCO3↓+2NaCl)
(4)乙同学将酚酞试液滴入氢氧化钙溶液中,观察到溶液变红,得出结论:氢氧化钙溶液呈(填“酸性”“碱性”或“中性”)。
(5)丙同学将过量的稀盐酸加入乙同学所得溶液中,观察到红色褪去,此时所得溶液中含有的溶质有(酸碱指示剂除外) , 请设计实验证明盐酸过量:。
(6)丁同学将碳酸钠溶液加入滴有酚酞的氢氧化钙溶液中,充分反应后,观察到的现象为;反应后溶液中的溶质一定有。
-
17、填空题:(1)、画原子结构示意图:C;Al。(2)、画离子结构示意图:;Na+。(3)、写化学式 :硫酸铝;碳酸氢钙。
-
18、将下列各组物质,按单质、氧化物、酸、碱、盐分类顺序排列正确的是A、银、二氧化硫、硫酸、烧碱、大理石 B、碘酒、冰、硫酸氢钠、烧碱、碳酸钙 C、氢气、干冰、硝酸、烧碱、硝酸钾 D、铜、氧化铜、醋酸、石灰水、碳酸氢钠
-
19、下列各化合物中Mn呈最高价的是A、MnO2 B、MnSO4 C、K2MnO4 D、KMnO4
-
20、航天科学技术测得三氧化二碳(C2O3)是金星大气层的成分之一、下列有关C2O3的说法不正确的是A、C2O3和CO2都属于非金属氧化物 B、C2O3和CO的完全燃烧产物都是CO2 C、C2O3和CO都是碱性氧化物 D、C2O3中C的化合价为+3