相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、钠元素有多种化合物的形式存在,其中NaOH、Na2CO3、NaHCO3是重要的化工原料,在日常生活和工业生产中有广泛的应用。(1)、NaHCO3可用于治疗胃酸过多,反应原理的化学方程式为。(2)、Na2CO3俗称纯碱,水溶液呈碱性。其在水溶液中的电离方程式为。(3)、无水Na2CO3是一种常见的基准物质。可用来准确配置一定浓度的标准溶液,用来标定酸性试剂的浓度。某兴趣小组需要配制0.2000mol/LNa2CO3标准溶液250mL。
①为配制溶液,准备了分析天平、药匙、烧杯、量筒、玻璃棒,还缺少的主要仪器有、。
②经计算,用分析天平准确称取g无水Na2CO3晶体。(保留四位有效数字)
③该溶液的配制过程中,会导致所配溶液浓度偏高的操作为(填序号)。
A.配制前洗涤容量瓶,但未干燥就进行配制
B.溶解药品的烧杯未进行洗涤
C.溶液未冷却立即转移
D.定容时,加蒸馏水超过刻度线,用胶头滴管吸出
E.定容时,俯视刻度线
(4)、已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,设计下图的装置进行实验。
主要实验步骤如下:按图组装仪器,并检查装置的气密性,将5.00g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;称量盛有碱石灰的U形管的质量,得到218.60g,从分液漏斗逐滴滴入6mol/L的硫酸。控制生成气体的速率不可太快,直到不再产生气体时为止,从导管A处缓缓鼓入一定量的空气,再次称量盛有碱石灰的U形管的质量,重复鼓入空气和称量的操作,直到U形管的质量不变,为220.40g。请回答问题:
①装置中干燥管B的作用是。
②从导管A处缓缓鼓入空气的目的是。
③该试样中纯碱的质量分数为。
-
2、利用NaClO和尿素[CO(NH2)2]反应制备N2H4·H2O(水合肼)的实验流程如下图,下列说法错误的是

已知:①氯气与烧碱溶液的反应是放热反应:若温度过高会产生副产物NaClO3;
②N2H4·H2O有强还原性,能与NaClO剧烈反应生成N2。
A、步骤1中应采用冰水浴 B、步骤Ⅰ制备NaClO洛液时,若溶液中NaClO与NaClO3的物质的量之比为5:1,则参与反应的氧化剂与还原剂的物质的量之比为3:5 C、步骤Ⅱ中每生成1molN2H4·H2O反应中转移2mol电子 D、步骤Ⅱ中应将NaClO碱性溶液逐滴滴入尿素水溶液中 -
3、下列实验操作、现象和结论均正确的是
选项
实验操作
现象
结论
A
用坩埚钳夹持一片打磨光亮的铝片,在酒精灯火焰上加热,轻轻晃动铝片
铝片表面呈灰白色,熔化而不滴落
铝的熔点很高
B
把CCl4加入碘水中,振荡、静置、分液。从上口倒出有机层
分层,上层呈紫红色
CCl4能萃取碘,CCl4密度比水小
C
各取浓度约为15%的双氧水3mL于两试管中,一支试管常温,另一支试管置于75℃热水浴
热水浴的试管中气泡产生速率比较快
升温可加快反应速率
D
用玻璃棒蘸取样品,在外焰上灼烧,观察现象
焰色呈黄色
样品中一定含有钠元素
A、A B、B C、C D、D -
4、数字化实验是利用传感器和信息处理终端进行实验数据的采集与分析。如图是利用数字化实验测定光照新制氯水过程得到的图象,该图象的纵轴表示的意义可能是
 A、氯离子的浓度 B、氧气的体积分数/% C、氯水的pH D、氯水的导电能力
A、氯离子的浓度 B、氧气的体积分数/% C、氯水的pH D、氯水的导电能力 -
5、设NA表示阿伏加德罗常数的值,下列说法正确的是A、7.1gCl2完全溶于水,转移电子数为0.1NA B、标准状况下,22.4L水中含有10NA个质子 C、在1mol/L的盐酸中,含有NA个H+ D、常温常压下,32gO2中含有个NA个氧分子
-
6、下列选项所表示的物质间转化关系不能一步转化的是A、CaO→Ca(OH)2→CaCO3 B、HCl→Cl2→NaCl C、CO2→Na2CO3→NaCl D、Cu→CuO→Cu(OH)2
-
7、下列溶液中,与200mL0.5mol/LMgCl2溶液中所含的Cl-物质的量浓度相同的是A、100mL1mol/LNaCl溶液 B、200mL0.25mol/LAlCl3溶液 C、100mL0.5mol/LHCl溶液 D、400mL0.5mol/LNH4Cl溶液
-
8、阅读材料,高铁酸钾(K2FeO4)为暗紫色的粉末,是一种新型的绿色环保水处理材料。在饮用水的处理过程中,具有集氧化、吸附、絮凝、沉淀、灭菌、消毒、脱色、除臭等八大特点为一体的综合性能。可利用氯气与过量氢氧化钠反应生成饱和次氯酸钠的浓碱液,再加入硝酸铁晶体,最后加入氢氧化钾饱和溶液,经冰水冷却可得高铁酸钾沉淀,反应原理为:Cl2+2NaOH=NaCl+NaClO+H2O,3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O,Na2FeO4+2KOH=K2FeO4+2NaOH,完成问题。(1)、根据物质的组成进行分类,K2FeO4属于A、酸 B、碱 C、盐 D、氧化物(2)、下列关于K2FeO4的描述不正确的是A、铁元素的价态为+3价 B、常温下易溶于水 C、具有强氧化性 D、在饮用水的处理过程中,可形成胶体粒子(3)、根据K2FeO4的制备原理。下列推断正确的是A、原理中涉及的反应均为氧化还原反应 B、Cl2在反应中只作氧化剂 C、碱性条件下,Na2FeO4氧化性强于NaClO D、0℃温度下,Na2FeO4水中的溶解度大于K2FeO4
-
9、现有三组混合液:①汽油和水;②分离乙醇(沸点78℃)和水;③分离溴水中的溴单质。分离以上各组混合液的正确方法依次是A、分液、萃取、蒸馏 B、分液、蒸馏、萃取 C、萃取、蒸馏、分液 D、蒸馏、萃取、分液
-
10、王勃《滕王阁序》中“落霞与孤鹜齐飞,秋水共长天一色”,描写了落日的余晖穿过薄薄云雾的唯美景象,形成这种美最本质原因是A、发生了丁达尔效应 B、空气中小水滴颗粒的布朗运动 C、雾是一种胶体,胶粒带有电荷 D、空气中小水滴颗粒直径为1~100nm
-
11、下列有关物质性质与用途对应关系不正确的是A、次氯酸具有不稳定性,可用于漂白纸张 B、NaOH能与Cl2反应,可用于Cl2尾气处理 C、CaO能与水反应,可用作食品干燥剂 D、稀硫酸具有酸性,可用于除去铁锈
-
12、我国古代四大发明黑火药爆炸方程式为:2KNO3+S+3C=K2S+N2↑+3CO2↑。下列说法不正确的是A、KNO3属于电解质 B、CO2属于酸性氧化物 C、中子数为8的碳原子表示为: D、S2-的结构示意图是:

-
13、我国第十四个五年规划和2035年远景目标纲要第十一篇是《推动绿色发展,促进人与自然和谐共生》。下列有利于实现该目标的是A、大量使用化肥,增加农作物收成 B、参与植树造林,扩大植被面积 C、大量使用一次性餐盒,保证饮食卫生 D、大力发展火力发电,满足用电需求
-
14、以印刷线路板的碱性蚀刻废液(主要成分为)为原料可制取CuO。
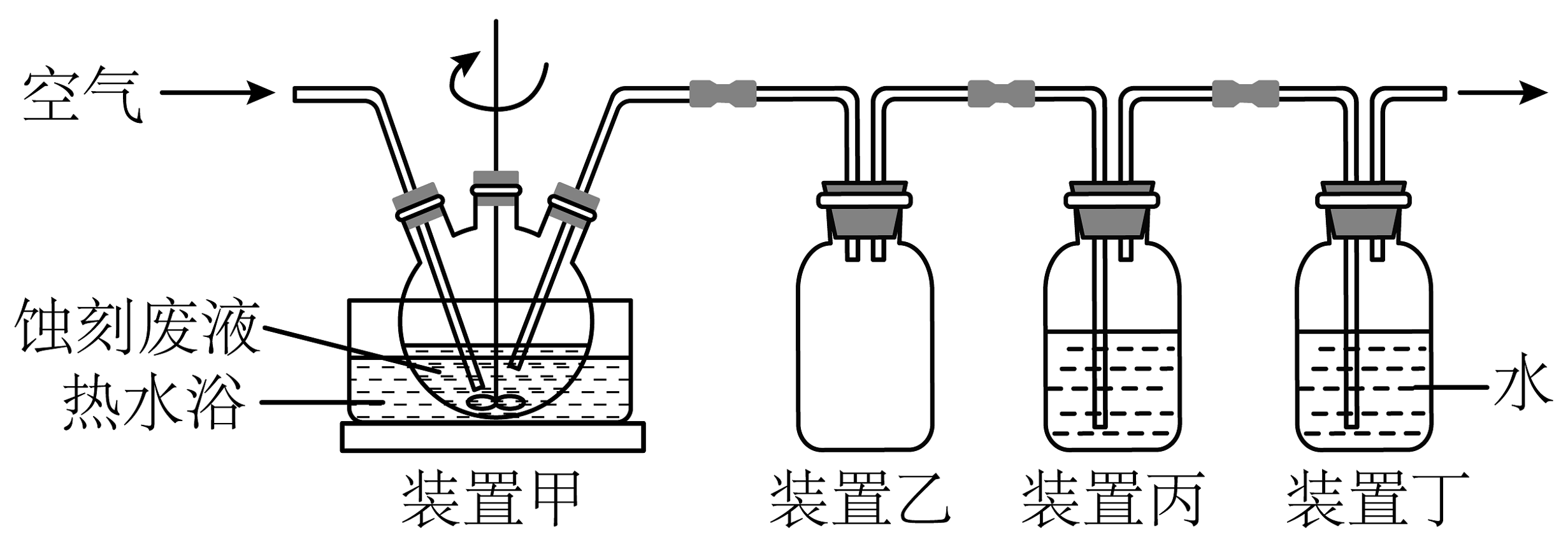 (1)、取一定量蚀刻废液和稍过量的NaOH溶液加入到装置甲的三颈瓶中,在搅拌下加热反应并通入空气,有产生,反应结束后将装置甲内混合物过滤,得到含NaCl的滤液,将滤渣洗涤,得到CuO。
(1)、取一定量蚀刻废液和稍过量的NaOH溶液加入到装置甲的三颈瓶中,在搅拌下加热反应并通入空气,有产生,反应结束后将装置甲内混合物过滤,得到含NaCl的滤液,将滤渣洗涤,得到CuO。①写出三颈瓶内反应的化学方程式:。
②检验滤渣已经洗涤干净的方式是:。
③装置乙的作用是:。
④为检验反应中有生成,装置丙中可盛装的溶液是。
(2)、将含少量杂质的CuO溶于稀硫酸中,向其中加入KI溶液,发生反应:。向溶液中滴加溶液,发生反应:。恰好完全反应时消耗的溶液20.00mL。计算CuO的质量,写出计算过程(杂质不参与反应)。 -
15、是常见的试剂,可用于有机物的转化。一定条件下,可以发生如下图所示的转化:
 (1)、写出转化Ⅰ反应的化学方程式:。(2)、乙酸中所含官能团的名称为。(3)、如图所示为实验室制取乙酸乙酯的实验装置(试剂未标注)。
(1)、写出转化Ⅰ反应的化学方程式:。(2)、乙酸中所含官能团的名称为。(3)、如图所示为实验室制取乙酸乙酯的实验装置(试剂未标注)。
①写出如图所示装置中乙醇和乙酸反应的化学方程式:。
②右侧小试管中应装有溶液。
-
16、固体为紫色,是一种高效水处理剂,为探究其性质,现进行如下实验:
实验1:取相同质量的二份固体,分别加入等体积的浓KOH溶液和水中,加入水中的完全溶解,溶液中有气体生成,用激光笔照射溶液,内部出现一条光亮的通路,浓KOH溶液中有大量紫色固体未溶解,溶液中无气体生成,用激光笔照射溶液,内部无光亮的通路。
实验2:向少量固体中加入足量盐酸,固体完全反应,有黄绿色气体产生。所得溶液为黄色,滴加KSCN溶液后变为红色。
依据实验现象所得结论不正确的是
A、可作水处理剂的原因是其具有强氧化性 B、在水中的溶解性大于在浓KOH溶液中 C、在水中可能有和胶体生成 D、与盐酸反应后有和生成 -
17、下列实验方案能达到预期目的的是A、用浓硫酸干燥氨气 B、用溶液鉴别溶液和溶液 C、用加热的方法除去固体中的 D、用焰色试验(又称焰色反应)鉴别NaCl和固体
-
18、短周期主族元素X、Y、Z的原子序数依次增大,X原子最外层电子数是次外层电子数的3倍,Y是短周期中金属性最强的元素,Z与X位于同一主族。下列叙述正确的是A、原子半径: r(Z)>r(X)>r(Y) B、X的简单气态氢化物的热稳定性比Z弱 C、X、Y、Z三种元素可形成化合物Y2ZX3 D、Y形成的最高价氧化物的水化物是弱碱
-
19、下列各组物质互为同分异构体的是A、金刚石和石墨 B、和 C、和 D、和
-
20、下列关于各有机物的说法正确的是A、甲烷分子中所有原子均在同一平面上 B、苯的结构简式为C6H6 C、乙醇与钠反应比水与钠反应剧烈 D、乙酸可与NaHCO3溶液反应生成CO2