相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、化学与生活、生产、科技、及社会发展密切相关。下列说法正确的是( )A、宇航服材料之一聚酰胺纤维是天然有机高分子材料 B、醴陵釉下五彩瓷烧制温度达1380℃,该过程中发生了复杂的物理、化学变化 C、为增强“84”消毒液的消毒效果,可加入适量稀盐酸 D、侯氏制碱法中为提高气体利用率,向饱和食盐水中先通入后通入氨气
-
2、某化学小组利用变量控制法研究外界条件对化学反应速率的影响,进行如下实验。
【实验原理】
【实验内容及记录】实验编号
加入溶液的体积
加入水的体积
加入溶液的体积
加入稀的体积
室温下溶液褪色所需时间
1
3.0mL
2.0mL
3.0mL
2.0mL
4.0min
2
2.0mL
3.0mL
3.0mL
2.0mL
5.2min
3
1.0mL
amL
3.0mL
2.0mL
6.4min
(1)、根据上表中的实验数据,得到的结论为(填“”、“”或“稀”)的浓度增大,化学反应速率增大。(2)、利用实验1中数据进行计算,用的浓度变化表示的化学反应速率为。(3)、实验3中加入的体积a为mL。(4)、该小组同学查阅资料发现对该反应有催化作用。于是与实验1对比,设计实验4进行验证。实验编号
加入溶液的体积
加入水的体积
加入溶液的体积
加入稀的体积
加入的物质
室温下溶液褪色所需时间
4
3.0mL
2.0mL
3.0mL
2.0mL
t
①上述表格中,加入的物质是。
②实验4中,t4.0min(填“大于”或“小于”)。
-
3、海带中含有碘元素,从海带中提取碘的实验过程如下图。
 (1)、步骤①一定不会用到下列仪器中的。
(1)、步骤①一定不会用到下列仪器中的。a.酒精灯 b.漏斗 c.坩埚
(2)、步骤④选用的试剂为氯水,则该反应的离子方程式为;检验该步骤中有生成的方法是。(3)、步骤⑤包含以下四个过程。
①过程Ⅰ使用的(填“能”或“不能”)用乙醇代替。
②过程Ⅱ中与浓NaOH溶液反应的离子方程式为。
③过程Ⅲ中化合价发生变化的元素为(填元素符号)。
④过程Ⅳ的操作名称为。
-
4、乙烯的产量被用作衡量一个国家石油化工产业发展水平的标志,截至2022年底,我国乙烯产能首次超过美国,成为世界乙烯产能第一大国。已知乙烯能发生以下转化(部分条件和产物已略去):
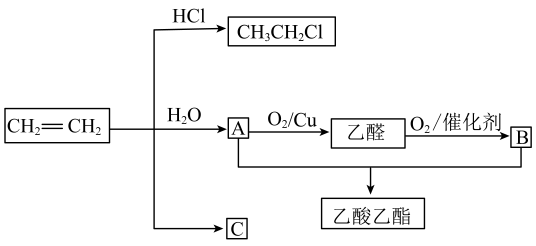 (1)、A中官能团的名称为 , A转化为乙醛的化学方程式为。(2)、B能去除少量水垢(主要成分),是利用了B的性。(3)、上图中生成氯乙烷的反应类型为。(4)、某研究小组利用A与B反应制备乙酸乙酯的装置如下图。
(1)、A中官能团的名称为 , A转化为乙醛的化学方程式为。(2)、B能去除少量水垢(主要成分),是利用了B的性。(3)、上图中生成氯乙烷的反应类型为。(4)、某研究小组利用A与B反应制备乙酸乙酯的装置如下图。
①试管a中反应的化学方程式为。
②试管b中导气管下端管口不浸入液面的目的是。
(5)、C是高分子化合物,可用于制作食品塑料袋,C的结构简式为。 -
5、元素周期律的发现和元素周期表的诞生,开创了化学科学的新纪元。有关短周期主族元素A、B、C、D、E的相关信息如下表所示。
序号
相关信息
A
单质为双原子分子,1个分子中含有14个电子
B
短周期主族元素中原子半径最大
C
最高正价与最低负价的绝对值相差6
D
单质为黄色或淡黄色固体,易溶于
E
M层比K层多1个电子
(1)、A的元素符号为 , 其原子结构示意图为。(2)、B在周期表中位于第3周期第族。(3)、B形成的碱性氧化物的化学式为 , 该化合物属于(填“离子”或“共价”)化合物。(4)、依据C、D在周期表中的位置判断:C和D的得电子能力较强的是(填元素符号)。(5)、B、D、E的最高价氧化物对应水化物相互之间均能反应,①E与B二者的最高价氧化物对应水化物反应的化学方程式为。
②E与D二者的最高价氧化物对应水化物反应的离子方程式为。
-
6、下列各组物质中,
①和;②和;③
 和
和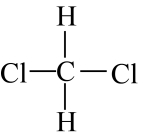 ;④石墨和金刚石;⑤正丁烷()和异丁烷(
;④石墨和金刚石;⑤正丁烷()和异丁烷(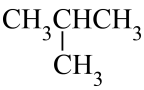 )(1)、互为同位素的是(填序号,下同)。(2)、互为同素异形体的是。(3)、互为同系物的是。(4)、互为同分异构体的是。(5)、属于同一种物质的是。
)(1)、互为同位素的是(填序号,下同)。(2)、互为同素异形体的是。(3)、互为同系物的是。(4)、互为同分异构体的是。(5)、属于同一种物质的是。 -
7、用下图装置探究原电池中的能量转化。图中注射器用来收集气体并读取气体体积,实验数据记录如下表:
时间/min
实验①
实验②
气体体积/mL
溶液温度/℃
气体体积/mL
溶液温度/℃
0
0
22.0
0
22.0
8.5
30
24.8
50
23.8
10.5
50
26.0
—
—

下列说法正确的是( )
A、①②中的碳棒表面均有气泡产生 B、生成相同体积气体时,实验①所用时间较短 C、0~8.5min,实验②反应较快,是因为该实验装置构成了原电池 D、反应至8.5min,对比两实验溶液温度,说明反应释放的总能量:①>② -
8、除去下列物质中的少量杂质,所选除杂试剂正确的是( )
选项
物质
除杂试剂
A
氨气中混有水蒸气
浓
B
溴苯中混有溴
苯
C
二氧化碳中混有氯化氢气体
NaOH溶液
D
甲烷中混有乙烯
溴水
A、A B、B C、C D、D -
9、在一定条件下,对于恒容密闭容器中进行的反应 , 能说明该反应达到化学平衡状态的是( )A、生成的速率与生成的速率相等 B、消耗的速率与生成的速率之比为 C、反应混合物中、、的浓度不再发生改变 D、反应混合物中、、的物质的量之比为
-
10、燃烧法是测定有机物分子式的一种重要方法。将0.1mol烃在中完全燃烧,得到(标准状况)和。若该烃不能使酸性溶液褪色,则下列说法错误的是( )A、该烃的分子式为 B、该烃分子中所有原子共平面 C、该烃分子中含有碳碳单键和碳碳双键 D、该烃是有特殊气味、难溶于水的有毒液体
-
11、氢气在氧气中燃烧的过程,可用如下模型表示(“—”表示化学键)。下列说法正确的是( )
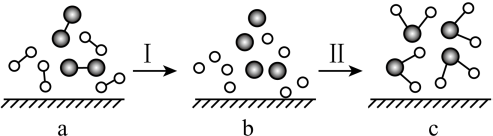 A、过程Ⅰ有化学键的断裂 B、过程Ⅱ是吸收能量的过程 C、总能量:状态a<状态c D、能量转化:化学能仅转化为热能
A、过程Ⅰ有化学键的断裂 B、过程Ⅱ是吸收能量的过程 C、总能量:状态a<状态c D、能量转化:化学能仅转化为热能 -
12、郑州宇通客车股份有限公司制造的氢燃料电池客车是北京冬奥会体育赛事用车之一,其反应原理如下图。下列说法正确的是( )
 A、电极a是负极 B、阴离子移向电极b C、离子导体可以选择蔗糖溶液 D、电子由电极b沿导线移向电极a
A、电极a是负极 B、阴离子移向电极b C、离子导体可以选择蔗糖溶液 D、电子由电极b沿导线移向电极a -
13、某原电池的总反应是 , 该原电池的构成正确的是( )A、
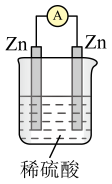 B、
B、 C、
C、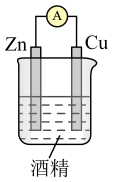 D、
D、
-
14、某汽车安全气囊的气体发生剂含有、 , 、等。汽车发生碰撞时,会产生大量气体使气囊迅速膨胀。下列说法错误的是( )A、受到撞击后分解产生和Na B、与Na反应中,作还原剂 C、因吸收产气过程中释放的热量而分解 D、中Cl的化合价为+7,推测具有氧化性
-
15、下列有关甲烷的说法错误的是( )A、甲烷的结构式:
 B、甲烷分子的空间填充模型:
B、甲烷分子的空间填充模型: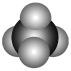 C、甲烷是最简单的不饱和链烃
D、甲烷和氯气在光照条件下发生取代反应
C、甲烷是最简单的不饱和链烃
D、甲烷和氯气在光照条件下发生取代反应
-
16、下列有关Cl、Br及其化合物的说法正确的是( )A、原子半径:Cl>Br B、单质的氧化性: C、酸性: D、气态氢化物的稳定性:HBr>HCl
-
17、高铁列车上的烟雾传感器,其主体是有镅()放射源的电离室。下列关于的说法正确的是( )A、电子数为146 B、质量数为336 C、中子数为241 D、质子数为95
-
18、下列反应与图中能量变化关系一致的是( )
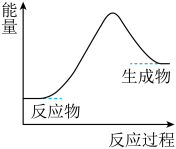 A、碳酸钙受热分解 B、铝与盐酸反应 C、生石灰与水反应 D、氢氧化钠与硫酸反应
A、碳酸钙受热分解 B、铝与盐酸反应 C、生石灰与水反应 D、氢氧化钠与硫酸反应 -
19、下列物质中,属于烃的衍生物的是( )A、甲烷 B、乙酸 C、乙烯 D、苯
-
20、下列物质中,只含共价键的是( )A、 B、 C、 D、