相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列物质分类正确的是( )A、甲苯为电解质 B、为碱性氧化物 C、淀粉溶液为胶体 D、水玻璃为化合物
-
2、研究氮的循环和转化对生产、生活有重要的价值。(1)、Ⅰ.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示:

设备1、3中发生反应的化学方程式分别是、;设备2中通入的物质A是。
(2)、Ⅱ.氨氮废水的处理是当前科学研究的热点问题之一。氨氮废水中的氮元素多以和的形式存在。某工厂处理氨氮废水的流程如下:
过程①的目的是将转化为 , 并通过鼓入大量热空气将氨气吹出,写出转化为的离子方程式:。(3)、过程②中加入NaClO溶液可将氨氮化合物转化为无毒物质,反应后含氮元素、氯元素的物质的化学式分别为、。(4)、图中含余氯废水中含有NaClO,则X可选用(填序号)的溶液达到去除余氯的目的。a.KOH
b.
c.
d.
-
3、(1)、I.在2L密闭容器内,800 ℃时发生反应: , 体系中n(NO)随时间的变化 如表:
时间/s 0 1 2 3 4 5 0.020 0.010 0.008 0.007 0.007 0.007
如图所示,表示浓度变化的曲线是(填字母)。 (2)、800 ℃,反应达到平衡时,NO的转化率是。(3)、 用表示0~2s内该反应的平均速率v=。(4)、Ⅱ.将一定量纯净的氨基甲酸铵()置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡: ,
(2)、800 ℃,反应达到平衡时,NO的转化率是。(3)、 用表示0~2s内该反应的平均速率v=。(4)、Ⅱ.将一定量纯净的氨基甲酸铵()置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡: ,
下列不能说明该分解反应已经达到化学平衡状态的是____(填序号)。A、 B、密闭容器中气体的总物质的量不变 C、容器中与的物质的量之比保持不变 D、密闭容器中总压强保持不变 E、气体中形成6个N—H键的同时有2个C=O键断裂(5)、能使该反应的反应速率增大的是____(填序号)。A、及时分离出气体 B、适当升高温度 C、加入少量 D、选择高效催化剂(6)、如图所示,上述反应中断开反应物中化学键吸收的能量(填“大于”“等于”或“小于”)形成生成物中化学键放出的能量。
-
4、某化学小组为了证明二氧化硫和氯水的漂白性,设计了如图所示的实验装置:

他们用亚硫酸钠和浓硫酸制备二氧化硫,用二氧化锰和浓盐酸制备氯气。
(1)、用来制取氯气的装置是(填字母序号),反应中浓盐酸所表现出的化学性质是和。(2)、反应开始一段时间后,B、D试管中的品红溶液均褪色。停止通气后,再将B、D两个试管分别加热,(填“B”或“D”')试管中无明显现象。(3)、装置C的主要作用是。(4)、该小组同学将两种气体混合后通入品红溶液中,发现漂白效果并不像预期的一样增强。查阅资料得知:两种气体混合,再与水反应可生成两种常见的酸,因而漂白作用减弱,该反应的化学方程式是。 -
5、根据如图所示的N2(g)和O2(g)反应生成NO(g)过程中能量变化情况,判断下列说法正确的是( )
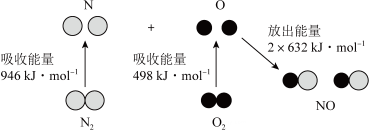 A、该反应中反应物所具有的总能量高于生成物所具有的总能量 B、2mol氮原子结合生成N2(g)时需要放出946kJ能量 C、1mol NO(g)分子中的化学键断裂时需要放出632kJ能量 D、上述过程描述的是2mol的N2与2mol O2反应的能量变化过程
A、该反应中反应物所具有的总能量高于生成物所具有的总能量 B、2mol氮原子结合生成N2(g)时需要放出946kJ能量 C、1mol NO(g)分子中的化学键断裂时需要放出632kJ能量 D、上述过程描述的是2mol的N2与2mol O2反应的能量变化过程 -
6、化学课外活动小组设计的用化学电源使LED灯发光的装置示意图如图。
下列有关该装置的说法正确的是( )
 A、如果将锌片换成铁片,那么电路中的电流方向将改变 B、该装置工作时,电解质溶液中阴离子移向锌片 C、铜片为负极,其附近的溶液变蓝 D、如果将稀硫酸换成柠檬汁,那么LED灯一定不会发光
A、如果将锌片换成铁片,那么电路中的电流方向将改变 B、该装置工作时,电解质溶液中阴离子移向锌片 C、铜片为负极,其附近的溶液变蓝 D、如果将稀硫酸换成柠檬汁,那么LED灯一定不会发光 -
7、下列物质中不能与
 发生化学反应的是( )
发生化学反应的是( )①
②
③Na
④
A、①② B、①④ C、② D、③④ -
8、表示阿伏加德罗常数的值,下列叙述正确的是( )A、个分子占有的体积为22.4 L B、标准状况下,22.4 L含有的原子数目为3 C、常温常压下,0.78 g含有的数目为0.02 D、物质的量浓度为0.5的溶液中,含有的数目为0.5
-
9、用如图所示的装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )

选项
气体
a
b
c
A
盐酸
碳酸钙
饱和溶液
B
浓硫酸
Fe
浓硫酸
C
浓氨水
生石灰
碱石灰
D
浓盐酸
粉末
浓硫酸
A、A B、B C、C D、D -
10、对于反应2SO2(g)+O2(g)⇌2SO3(g),判断下列说法正确的是( )
①单位时间内生成 , 同时生成 , 则处于化学平衡状态
②的生成速率等于的消耗速率,则处于化学平衡状态
③的体积分数不再发生变化,则处于化学平衡状态
④的分子数之比为2:1:2,则处于化学平衡状态
A、①③ B、②④ C、②③ D、③④ -
11、对于的反应来说,以下化学反应速率的表示中反应速率最快的是( )A、 B、 C、 D、
-
12、某粗盐含等杂质,常用3种试剂,过滤后,用盐酸中和,最终蒸发结晶得到精盐。其中,加入3种试剂顺序错误的是( )A、 B、 C、 D、
-
13、下列离子方程式书写正确的是( )A、铁与稀硫酸反应: B、氢氧化铜溶液与硫酸溶液的反应: C、碳酸钙与盐酸反应: D、氯化铁溶液和铜:
-
14、下列物质或微粒之间的相互关系错误的是( )A、和
 互为同分异构体
B、干冰和冰为同一种物质
C、和互为同系物
D、和互为同位素
互为同分异构体
B、干冰和冰为同一种物质
C、和互为同系物
D、和互为同位素
-
15、下列反应属于氧化还原反应,且能量变化如图所示的是( )
 A、锌粒和稀硫酸反应 B、灼热的木炭与反应 C、甲烷在空气中燃烧的反应 D、 晶体与晶体的反应
A、锌粒和稀硫酸反应 B、灼热的木炭与反应 C、甲烷在空气中燃烧的反应 D、 晶体与晶体的反应 -
16、下列反应符合“原子经济性反应”的是( )A、 B、 C、 D、
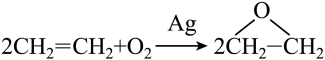
-
17、下列物质中,含有共价键的离子化合物是( )A、 B、NaOH C、 D、
-
18、化学与生产、生活、科研密切相关。下列说法错误的是( )A、制造月球探测器中的瞄准镜时使用的光导纤维,其主要成分是二氧化硅 B、火箭发射时使用液氢和液氧作推进剂,是利用燃烧反应提供能量 C、月球探测器使用的太阳能电池板,其主要成分是单质硅 D、氮化硅陶瓷、光导纤维、硅酸盐水泥均属于新型无机非金属材料
-
19、是制造电信器材软磁铁氧体,合成二氧化锰和制造其他锰盐的原料。用粉与矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备的工艺如下图所示:
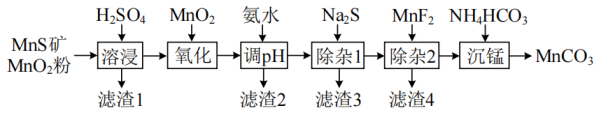
相关金属离子形成氢氧化物沉淀的pH范围如下:
金属离子
开始沉淀的pH
8.1
6.3
1.5
3.4
8.9
6.2
6.9
沉淀完全的pH
10.1
8.3
2.8
4.7
10.9
8.2
8.9
(1)、已知“滤渣1”含有S和 , 写出“溶浸”中生成S的化学方程式。(2)、加入氧化的是哪种离子?(3)、“调pH”控制的pH为4.7~6.0之间,写出“滤渣2”的化学式。(4)、“除杂1”的目的是加入除去和 , 分析该步骤不能通过调节pH除杂的原因。(5)、写出“沉锰”的离子方程式。(6)、在空气中加热易转化为不同价态的锰的氧化物,某小组称取一定质量的固体在空气中加热,测得固体质量的残留率随着温度的变化如图所示。
①写出从开始加热到A点过程中发生反应的化学方程式。
②若D点对应的固体残留率为64.52%,写出D点残留固体的成分及物质的量之比。
-
20、铍是原子能、火箭、导弹、航空以及冶金工业中不可缺少的宝贵材料。以绿柱石[Be3Al2(SiO3)6]为原料制备两性金属铍的工艺如图:

回答下列问题:
(1)、绿柱石写成氧化物的形式为。(2)、750℃烧结时,Na3FeF6仅与绿柱石中BeO作用生成易溶于水的Na2BeF4 , 滤渣的主要成分是Fe2O3和。(3)、“水浸”时“产物压碎磨细”的目的是 , 为检验“过滤1”的滤液中是否含有Na+ , 可选用的方法是(填方法名称)。(4)、“沉氟”的化学方程式为。(5)、镍坩埚作阴极、石墨作阳极,350~400℃电解NaCl-BeCl2熔融混合物得到金属铍,阳极反应式为;不能用该电解槽电解熔融氯化铍制金属铍的原因可能是。