相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、据脑科医生介绍,市面上所谓的“聪明药”,主要成分是哌醋甲酯(结构如图),是一种中枢神经系统兴奋剂,由于哌醋甲酯的作用机制和冰毒的主要成分类似,因此没有经过医生的指导服用会很危险。下列关于哌醋甲酯的说法正确的是( )
 A、分子式为C14H18NO2 B、能发生加成反应和取代反应 C、分子中的所有碳原子均共面 D、该物质不可能和盐酸反应
A、分子式为C14H18NO2 B、能发生加成反应和取代反应 C、分子中的所有碳原子均共面 D、该物质不可能和盐酸反应 -
2、使用下图装置制备乙酸乙酯,下列说法正确的是( )
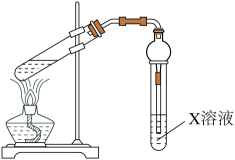 A、将缓缓加入浓 B、X中溶液是NaOH溶液 C、球形干燥管的作用是防倒吸 D、试管中油层在下面
A、将缓缓加入浓 B、X中溶液是NaOH溶液 C、球形干燥管的作用是防倒吸 D、试管中油层在下面 -
3、2022年诺贝尔生理或医学奖授予DNA研究领域的科学家。下列有关DNA的叙述错误的是( )A、DNA水解的最终产物为磷酸、葡萄糖和碱基 B、DNA中含C、H、O、N等元素 C、DNA分子的双螺旋结构两条链上的碱基通过氢键作用 D、DNA和RNA均以核苷酸为基本构成单元,且RNA分子一般呈单链状结构
-
4、萘(
 )与浓硫酸发生取代反应可以生成 2 种取代产物,反应进程中能量变化如图所
)与浓硫酸发生取代反应可以生成 2 种取代产物,反应进程中能量变化如图所示。其中相同投料,经历相同时间, 不同反应温度时产物的比例不同, 在 40℃和 160℃时,
得到 1-取代产物与 2-取代产物的比例分别为 96:4 和 15:85,下列说法正确的是( )
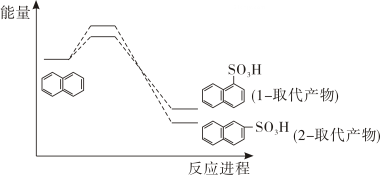 A、1-取代产物比 2-取代产物更稳定 B、与 40℃相比,160℃时萘的平衡转化率更大 C、选择合适的催化剂同样可以提高 2-取代产物比率 D、延长反应时间, 最终以 1-取代产物为主
A、1-取代产物比 2-取代产物更稳定 B、与 40℃相比,160℃时萘的平衡转化率更大 C、选择合适的催化剂同样可以提高 2-取代产物比率 D、延长反应时间, 最终以 1-取代产物为主 -
5、抗生素克拉维酸的结构简式如图所示, 下列关于克拉维酸的说法错误的是( )
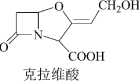 A、含有 5 种官能团 B、可使高锰酸钾溶液褪色 C、可以发生加成、取代、氧化等反应 D、1mol 该物质最多可与 1molNaOH 反应
A、含有 5 种官能团 B、可使高锰酸钾溶液褪色 C、可以发生加成、取代、氧化等反应 D、1mol 该物质最多可与 1molNaOH 反应 -
6、NA 代表阿伏加德罗常数的值。下列说法正确的是( )A、1molHC≡CH 分子中所含 σ 键数为 5 NA B、1L0.1 mol·L- 1 的 Na2CO3 溶液含 CO32- 的数目为 0.1 NA C、78 gNa2O2 与足量水完全反应, 电子转移数为 NA D、标准状况下,2.24 L C2H5OH 所含氢原子数为 0.6 NA
-
7、五育并举, 劳动先行。下列劳动项目与所述的化学知识没有关联的是( )
选项
劳动项目
化学知识
A
在未成熟水果的包装袋中充入乙烯
乙烯可用于催熟果实
B
用食醋除去水壶中的水垢
食醋可溶解水垢的主要成分 CaCO3
C
宣传推广使用免洗手酒精消毒液
乙醇具有特殊香味
D
利用铝热法焊接铁轨
铝与氧化铁反应,且放出大量的热
A、A B、B C、C D、D -
8、实验室用浓硫酸与乙醇制备乙烯。下列装置能达到实验目的的是( )




A.制备乙烯
B.净化乙烯
C.检验乙烯
D.收集乙烯
A、A B、B C、C D、D -
9、化学科学在科技强国中发挥着重要作用。下列有关叙述正确的是( )A、“天舟六号”货运飞船太阳能电池板主要材料为晶体硅,是一种分子晶体 B、C919 成功商飞, 大量采用第三代铝锂合金,铝锂合金的熔点比铝、锂都高 C、全球首枚液氧甲烷运载火箭朱雀二号遥二发射成功,甲烷是含有极性键的非极性分子 D、“液态太阳燃料”技术成功将 H2O 和 CO2 转化为甲醇等,H2O 和 CO2 都是直线型分子
-
10、(1)、【任务一】某小组研究和的性质,实验如下:
室温下,的溶解度大于的实验证据是。序号
操作
现象
在两支试管中加入或固体,再加入水,振荡;将温度计分别插入其中
温度由变为;放置至室温时,试管内无固体
温度由变为;放置至室温时,试管内有少量固体残留
室温时,分别向所得溶液中滴入滴酚酞溶液
溶液变红
溶液微红
(2)、该实验不能说明溶液的碱性强于溶液,理由是。(3)、【任务二】为进一步探究和的性质,利用传感器继续做如下实验:
信息提示:溶液越小,的浓度越小,溶液碱性越弱。澄清石灰水显碱性,用电离方程式表示其原因是。编号 实验操作 实验数据 测量下面实验过程中温度的变化 

测量下面实验过程中溶液的变化  注:溶液和溶液的浓度相等
注:溶液和溶液的浓度相等 (4)、实验中,溶解时吸收热量的物质是填化学式。(5)、实验中,溶液和澄清石灰水反应的离子方程式为 , 未参与该反应的实验证据是。(6)、实验中,滴加溶液的烧杯中溶液的变化与滴加溶液的有明显差异,原因是滴加溶液的烧杯中填离子符号参与了反应,写出反应初期的离子方程式:。
(4)、实验中,溶解时吸收热量的物质是填化学式。(5)、实验中,溶液和澄清石灰水反应的离子方程式为 , 未参与该反应的实验证据是。(6)、实验中,滴加溶液的烧杯中溶液的变化与滴加溶液的有明显差异,原因是滴加溶液的烧杯中填离子符号参与了反应,写出反应初期的离子方程式:。 -
11、计算(1)、标准状况下,甲烷和一氧化碳的混合气体共 , 其质量为 , 则混合气体中甲烷的物质的量为 。(2)、测定样品含氯化钠杂质中的质量分数:称取样品放入烧杯内加水溶解,加入过量的氯化钙溶液充分反应,过滤、洗涤、干燥,称量沉淀的质量为。则样品中的质量分数为。(3)、中含有 , 则的相对原子质量为。(4)、标准状况下,氯气通入足量溶液中,转移的电子数目为。
-
12、常温下,下列各组离子一定能在指定溶液中大量共存的是( )A、在中性溶液中:、、、 B、与反应能放出的溶液中:、、、 C、的溶液中:、、、 D、水电离的的溶液中:、、、
-
13、为预防新型冠状病毒肺炎,某同学购买了一瓶消毒液,其包装说明如图所示。
基本信息:含质量分数为的、、密度
使用方法:稀释倍后使用
注意事项:密封保存,易吸收空气中的、而变质
根据图中信息和相关知识判断,下列分析不正确的是 ( )
A、从物质分类的角度看消毒液的有效成分属于强电解质 B、消毒液在空气中敞口放置一段时间后浓度会变小 C、该消毒液中的物质的量浓度约为 D、用容量瓶配制上述消毒液时,定容时俯视刻度线,所得溶液浓度会偏大 -
14、用表示阿伏加德罗常数的值,下列叙述正确的是 ( )A、与充分反应生成时,转移电子数为 B、标准状况下,乙烷中所含的极性共价键数目为 C、羟基与所含电子数之比为 D、一定温度下溶液与溶液含的物质的量相同
-
15、已知氧化性:。向溶液中逐渐通入 , 其中、随通入的物质的量变化如图所示,下列说法错误的是( )
 A、还原性强弱:Fe2+>Br- B、曲线①为Fe2+ , 且c=1.5 C、n(Cl2)=0.35 mol时,溶液中c(Fe3+)=c(Br-) D、n(Cl2)=0.45 mol时,总的离子方程式为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
A、还原性强弱:Fe2+>Br- B、曲线①为Fe2+ , 且c=1.5 C、n(Cl2)=0.35 mol时,溶液中c(Fe3+)=c(Br-) D、n(Cl2)=0.45 mol时,总的离子方程式为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- -
16、某化学兴趣小组模拟侯氏制碱法进行实验,流程如下图。下列说法正确的是( )
 A、该流程中可循环的物质只有 B、生成的离子方程式为: C、获得纯净晶体的操作为蒸发结晶、过滤、洗涤、干燥 D、用澄清石灰水可以鉴别和
A、该流程中可循环的物质只有 B、生成的离子方程式为: C、获得纯净晶体的操作为蒸发结晶、过滤、洗涤、干燥 D、用澄清石灰水可以鉴别和 -
17、下列实验中,能够正确描述反应的离子方程式是( )A、磁性氧化铁溶于稀: B、海水提溴工艺中,用纯碱溶液富集: C、用石灰乳制漂白粉: D、用足量的碱性溶液除去水中的:
-
18、如图所示是配制一定物质的量浓度溶液的过程。下列说法中不正确的是( )
 A、所配制的溶液中的物质的量浓度为 B、操作中玻璃棒的下端应该抵在容量瓶的刻度线下方 C、操作如果仰视,所配得溶液浓度偏高 D、操作中,定容摇匀后发现液面低于刻度线,不再需要加水
A、所配制的溶液中的物质的量浓度为 B、操作中玻璃棒的下端应该抵在容量瓶的刻度线下方 C、操作如果仰视,所配得溶液浓度偏高 D、操作中,定容摇匀后发现液面低于刻度线,不再需要加水 -
19、为阿伏加德罗常数的值,下列说法不正确的是( )A、常温常压下,气体中含有的氧原子数小于 B、中含有的键的数目为 C、中含有的离子总数为 D、盐酸与足量共热,转移的电子数为
-
20、下列离子方程式正确的是( )A、澄清石灰水与过量反应: B、与在酸性溶液中的反应: C、向沸水中滴加饱和的溶液制备胶体: D、向碳酸氢铵溶液中加入足量石灰水: