相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列关于离子共存或离子反应的说法正确的是( )A、无色透明的溶液中能大量共存: 、、、 B、溶液中能大量共存: C、与 H₂O₂在酸性溶液中的反应: D、稀硫酸和氢氧化钡溶液反应:
-
2、阿伏加德罗常数的值为 , 下列说法正确的是( )A、0.1mol的 中,含有 个中子 B、1mol Fe溶于过量硝酸,电子转移数为 C、2.4gMg与 H₂SO₄完全反应,转移的电子数为 D、标准状况下, 2.24LN₂和 O₂的混合气体中分子数为
-
3、下列实验中,不能达到实验目的的是( )
由海水制取蒸馏水
萃取碘水中的碘 分离粗盐中的不溶物 由FeCl3·6H2O制取无水FeCl3固体 



A B C D A、A B、B C、C D、D -
4、实验室将粗盐提纯并配制 的 NaCl溶液。 下列仪器中,本实验必须用到的有( )
①天平 ②温度计 ③坩埚 ④分液漏斗⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A、①②④⑥ B、①④⑤⑥ C、②③⑦⑧ D、①⑤⑥⑧ -
5、为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于盐酸,再进行下列实验,其中结论正确的是( )A、若滴加KSCN溶液,溶液变红,说明铁粉变质 B、若滴加KSCN溶液,溶液未变红,说明铁粉未变质 C、若依次滴加氯水、KSCN溶液,溶液变红,说明铁粉全部变质 D、若滴加KSCN溶液,溶液未变红;再滴加氯水,溶液变红,说明铁粉全部变质
-
6、离子化合物 Na2O2和 与水的反应分别为:
①2Na2O2 + 2H2O ═ 4NaOH + O2↑ ② CaH2+ 2H2O ═ Ca(OH)2+ 2H2↑
下列说法正确的是( )
A、Na2O2、CaH2中均有非极性共价键 B、①中水发生氧化反应,②中水发生还原反应 C、Na2O2中阴、阳离子个数比为1:2,CaH2中阴、阳离子个数比为2:1 D、当反应①和②中转移的电子数相同时,产生的 O2和 H2的物质的量相同 -
7、下列反应的离子方程式不正确的是( )A、Cl₂通入氢氧化钠溶液: B、氧化铝溶于氢氧化钠溶液: C、过量 CO₂通入饱和碳酸钠溶液: 2NaHCO₃↓ D、H2SO₃溶液中滴入氯化钙溶液:
-
8、物质的性质决定用途,下列两者对应关系不正确的是 ( )A、SO₂能使某些色素褪色,可用作漂白剂 B、金属钠导热性好,可用作传热介质 C、NaClO 溶液呈碱性,可用作消毒剂 D、Fe2O₃呈红色,可用作颜料
-
9、下列过程与水解反应无关的是( )A、热的纯碱溶液去除油脂 B、重油在高温、高压和催化剂作用下转化为小分子烃 C、蛋白质在酶的作用下转化为氨基酸 D、向沸水中滴入饱和FeCl₃溶液制备Fe(OH)₃胶体
-
10、化学在文物的研究和修复中有重要作用。下列说法错误的是( )A、竹简的成分之一纤维素属于天然高分子 B、龟甲的成分之一羟基磷灰石属于无机物 C、古陶瓷修复所用的熟石膏,其成分为 Ca(OH)₂ D、古壁画颜料中所用的铁红,其成分为 Fe2O₃
-
11、下列物质中属于耐高温酸性氧化物的是( )A、CO₂ B、SiO₂ C、MgO D、Na2O
-
12、氧氮杂环是新药研制过程中发现的一类重要活性物质,有抗肿瘤功效。下面是某研究团队提出的一种氧氮杂环类化合物F的合成路线:

已知:
 +
+
 (1)、A的名称是 , B中含氧官能团的名称是羧基、 , E中手性碳原子的数目为。(2)、根据C的结构特征,分析预测其可能的化学性质,完成下表。
(1)、A的名称是 , B中含氧官能团的名称是羧基、 , E中手性碳原子的数目为。(2)、根据C的结构特征,分析预测其可能的化学性质,完成下表。序号
结构特征
反应的试剂、条件
反应形成的新结构或产物
反应类型
①

、

还原反应
②
M的结构简式
D
反应
(3)、B有多种同分异构体,满足以下条件的同分异构体有种。①仅含苯环一个环状结构,且苯环上仅有2个取代基
②仅含2种官能团且能发生银镜反应
③不含 , 不含
 .
.其中核磁共振氢谱有三组吸收峰,峰面积之比为3∶2∶2的一种同分异构体结构简式。
(4)、参照上述合成路线和信息,写出由 和
和  为原料合成
为原料合成 的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件,无机试剂任选) 。
的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件,无机试剂任选) 。 -
13、含氮化合物在生产、生活中有着广泛的用途。回答下列问题:
已知:Ⅰ.
Ⅱ.
Ⅲ.
(1)、若反应Ⅲ的逆反应活化能为 , 则正反应活化能为(用含的式子表示)。(2)、在恒容密闭容器中按投料比发生反应Ⅲ,不同催化剂条件下,反应相同时间时,测得转化率与温度的关系如图所示。①下列能够说明反应Ⅲ在某种条件下已达到化学平衡状态的是(填标号)。
A. B.混合气体的密度不再变化
C.200℃时,容器内气体总压强不再变化
D.混合气体的平均相对分子质量不再变化

②使用催化剂乙,温度高于350℃时,转化率降低,原因可能是。
③研究表明该反应速率 , 其中为速率常数,与温度、活化能有关。℃的初始速率为 , 当转化率为50%时,反应速率为 , 由此可知。
(3)、工业上常利用反应 合成氨气,在、不同物质的量分数(75%的和25%的;67.5%的、22.5%的和10%的惰性气体)条件下进行实验,测得平衡时体积分数与温度的关系如图所示。
①物质的量分数为75%的和25%的所对应的曲线是(填“a”或“b”)。
②点时,的转化率为。点对应温度下,反应的压强平衡常数(用平衡分压代替平衡浓度,分压=总压×物质的量分数。保留两位有效数字)。
-
14、过氧化氢(H2O2)是一种绿色氧化剂。为了方便贮存、运输,工业上将其转化为固态过碳酸钠(2Na2CO3·3H2O2)。该物质具有Na2CO3与H2O2的双重性质,可用作无毒漂白剂和供氧剂。制备过碳酸钠的工艺流程如下图所示:

回答下列问题:
(1)、H2O2电子式为。(2)、"滤液”中的溶质可作氮肥的是。(3)、“反应II”的化学方程式为。(4)、加入NaCl的作用是。(5)、得到过碳酸钠粗品,经过滤、洗涤、干燥得到产品,证明产品洗涤干净的操作是。(6)、为测定产品纯度,称量m g产品并配制成250mL溶液,量取25.00mL该溶液于锥形瓶中,用0.100mol/L的酸性KMnO4溶液滴定,重复三次实验,平均消耗V mL酸性KMnO4溶液,则产品纯度为(用m、V表示)(7)、过硼酸钠晶体(NaBO3·4H2O)也可用作无毒漂白剂,加热至70℃以上会逐步失去结晶水。实验测得过硼酸钠晶体的质量随温度变化的曲线如下图所示,则T2~ T3所对应的化学方程式为。 (8)、与同周期,、、可形成一种具有特殊导电性的晶体(化学式为 , 、为整数),其立方晶胞如图所示,与最小间距大于与最小间距。
(8)、与同周期,、、可形成一种具有特殊导电性的晶体(化学式为 , 、为整数),其立方晶胞如图所示,与最小间距大于与最小间距。①该晶体中,1个周围与其最近的的个数为。
②若与最小间距为 , 阿伏加德罗常数为 , 则该晶体的密度为。

-
15、磺酰氯( SO2Cl2 )可用于制造锂电池正极活性物质。实验室可利用SO2和Cl2在活性炭催化下反应制取少量SO2Cl2 , 装置如图(部分夹持装置已省略)。

已知:①SO2(g) +Cl2(g)=SO2Cl2(1) △H = -97.3 kJ/mol;
②SO2Cl2熔点为-54.1℃ ,沸点为69.1℃,常温较稳定,遇水剧烈水解,100℃以上易分解。
回答下列问题:
(1)、仪器A的名称是 , 装置丙中橡胶管的作用是。(2)、装置丙中发生反应的离子方程式为 ,上述仪器的正确连接顺序是e →g,h←←f(填仪器接口字母编号,仪器可重复使用)。
(3)、仪器F的作用是。(4)、装置丁中三颈烧瓶需置于冷水浴中,其原因是。(5)、某实验小组利用该装置消耗氯气1120 mL(标准状况下,SO2足量) ,最后得到纯净的磺酰氯4.0 g,则磺酰氯的产率为(结果精确到0.01%)。 -
16、已知。室温下,向一元弱酸溶液中逐滴滴加溶液,溶液的随的变化关系如图所示。下列说法正确的是( )
 A、当时,溶液中 B、当时,加入的溶液体积大于 C、当加入溶液时,溶液中 D、、、三点对应溶液中水电离出来的浓度:点点点
A、当时,溶液中 B、当时,加入的溶液体积大于 C、当加入溶液时,溶液中 D、、、三点对应溶液中水电离出来的浓度:点点点 -
17、近期科技工作者开发了一套CO和甘油(C3H8O3)的共电解装置,如下图所示。下列说法正确的是( )
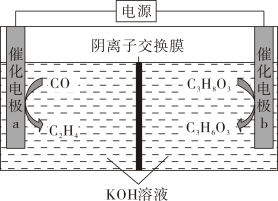 A、催化电极b连接电源的负极 B、电解过程中K+从阳极区移向阴极区 C、阴极区的电极反应为2CO+8e- +6H2O=C2H4+ 8OH- D、电解前后溶液的pH不变
A、催化电极b连接电源的负极 B、电解过程中K+从阳极区移向阴极区 C、阴极区的电极反应为2CO+8e- +6H2O=C2H4+ 8OH- D、电解前后溶液的pH不变 -
18、硒能增强人体免疫功能,抗氧化,延缓衰老,有效抑制肿瘤生长。实验室模拟工业上由含硒废料(主要含、、、、、等)制取硒的流程如下:

下列有关说法正确的是( )
A、“分离”前,将废料粉碎可以提高活化分子百分数,加快分离速率 B、“分离”、“酸溶”、“浸取”时都需要用到的玻璃仪器有:烧杯、玻璃棒、分液漏斗 C、“酸化”过程中发生的离子反应为 D、若向“酸溶”所得的滤液中滴入少量KSCN溶液,无明显现象 -
19、中科院院士研究发现,纤维素可在低温下溶于NaOH溶液,恢复至室温后不稳定,加入尿素可得到室温下稳定的溶液,为纤维素绿色再生利用提供了新的解决方案。下列说法错误的是( )
 A、纤维素是自然界分布广泛的一种多糖 B、纤维素难溶于水主要原因是其链间有多个氢键 C、NaOH提供破坏纤维素链之间的氢键 D、低温降低纤维素在NaOH溶液中的溶解性
A、纤维素是自然界分布广泛的一种多糖 B、纤维素难溶于水主要原因是其链间有多个氢键 C、NaOH提供破坏纤维素链之间的氢键 D、低温降低纤维素在NaOH溶液中的溶解性 -
20、用下列实验装置进行相应实验,能达到实验目的的是( )
 A、用图1所示装置验证浓硫酸具有强氧化性 B、用图2所示装置制取并收集乙烯 C、用图3所示装置制取干燥的NH3 D、用图4所示装置制取Cl2
A、用图1所示装置验证浓硫酸具有强氧化性 B、用图2所示装置制取并收集乙烯 C、用图3所示装置制取干燥的NH3 D、用图4所示装置制取Cl2