相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列溶液中,与200mL0.5mol/LNa2SO4溶液所含物质的量浓度相同的是( )A、200mL0.25mol/LNaCl溶液 B、100mL1mol/LNaCl溶液 C、100mL0.5mol/LNaOH溶液 D、100mL2mol/LNaOH溶液
-
2、下列说法正确的是( )A、铁丝、石墨均能导电,所以它们都是电解质 B、盐酸是强电解质,所以导电能力比醋酸溶液强 C、氯化银难溶于水,所以氯化银是非电解质 D、蔗糖溶液和熔融的蔗糖都不能导电,所以蔗糖是非电解质
-
3、下列物质按化合物、单质、混合物顺序排列的是( )A、烧碱、液态氮、碘酒 B、生石灰、白磷、熟石灰 C、干冰、铁、氯化氢 D、空气、氮气、胆矾
-
4、只能表示一个化学反应的离子方程式是( )A、 B、 C、 D、
-
5、以淀粉为主要原料合成一种具有果香味的物质C和化合物D的合成路线如下图所示。

请回答下列问题:
(1)、反应⑦中物质X的分子式为 , 反应⑧的类型为。(2)、反应③的化学方程式为。(3)、反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是。(4)、检验反应①进行程度,需要的试剂有____。A、新制的Cu(OH)2悬浊液 B、碘水 C、NaOH溶液 D、FeCl3溶液(5)、乙烯的同系物丙烯(CH2=CH-CH3)可以通过加聚反应生成高分子化合物,其结构简式是。 -
6、某研究性学习小组利用如图装置制备 , 并对的性质进行探究(装置的气密性已检查)。
 (1)、Ⅰ.探究与可溶性钡的强酸盐是否反应(接口a接b)
(1)、Ⅰ.探究与可溶性钡的强酸盐是否反应(接口a接b)
滴加浓硫酸之前,打开弹簧夹,通入一段时间 , 再关闭弹簧夹,此操作的目的是。(2)、实验过程中装置B中没有明显变化,装置C中有白色沉淀生成,该沉淀不溶于稀盐酸。据B中现象得出的结论是 , 装置C中反应的离子方程式是。(3)、装置D中全部转化为的离子方程式为:。(4)、Ⅱ.探究亚硫酸与次氯酸的酸性强弱(接口a接c)
将少量装置A中生成的气体直接通入装置G中,不能根据G中现象判断亚硫酸与次氯酸的酸性强弱,理由是(5)、为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置E中药品是 , 其作用是 , 通过现象即可证明亚硫酸的酸性强于次氯酸。 -
7、化学反应伴随能量变化,获取反应能量变化有多条途径。(1)、下列反应中,属于吸热反应的是____(填字母)。A、Na2O与水反应 B、甲烷的燃烧反应 C、Ba(OH)2·8H2O与氯化铵反应 D、锌与盐酸反应(2)、获取能量变化的途径
①通过化学键的键能计算。已知:
化学键种类
H-H
Cl-Cl
H-Cl
键能(kJ/mol)
436
247
434
计算可得:H2(g)+Cl2(g)=2HCl(g) △H= kJ·mol-1
②通过盖斯定律可计算。已知在25℃、101 kPa时:
I.2Na(s)+O2(g)=Na2O(s) △H=-414 kJ·mol-1
II.2Na(s)+O2(g)=Na2O2(s) △H=-511 kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式:。
(3)、以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。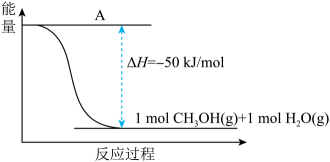
①补全上图:图中A处应填入。
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的△H(填“变大”“变小”或“不变”)。
③某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如图所示。
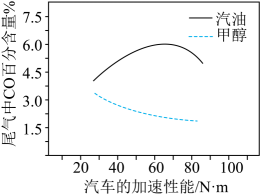
据图信息分析,与汽油相比,甲醇作为燃料的优点是。
-
8、海洋资源的利用具有广阔前景。(1)、下图是从海水中提取粗溴的主要流程

①从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是。
②可用热空气吹出溴是因为溴的(选填编号)
A.熔点较低 B.熔点较高 C.沸点较低 D.沸点较高
(2)、海带灰中富含以形式存在的碘元素。实验室提取的途径如下所示:
①灼烧海带至灰烬时所用的主要仪器名称是。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式。反应结束后,再加入作萃取剂,振荡、静置,该步操作用到的仪器名称为 , 可以观察到层呈色。
-
9、将铜镁合金完全溶解于某浓度的硝酸中,得到和的混合气体(标准状况),当向反应后的溶液中加入一定浓度溶液时,金属离子全部转化为沉淀,测得沉淀的质量为。和的混合气体中,的体积分数是( )A、 B、 C、 D、
-
10、《中国碳中和与清洁空气协同路径(2022)》报告指出,我国要在2030年实现“碳达峰”,2060年前实现“碳中和”。某科研小组用电化学方法将转化为CO实现再利用,转化的基本原理如图所示。下列说法不正确的是( )
 A、该装置能将化学能转化为电能 B、N极电极反应方程式为 C、工作一段时间后,M电极室中的溶液pH下降 D、外电路中,电流由N极经负载流向M极
A、该装置能将化学能转化为电能 B、N极电极反应方程式为 C、工作一段时间后,M电极室中的溶液pH下降 D、外电路中,电流由N极经负载流向M极 -
11、由一种工业废渣(主要成分为、少量Fe、Al的氧化物,其他杂质酸浸时不反应)为原料制备的实验过程如下。下列说法不正确的是( )
 A、将废渣粉碎同时酸浸时不断搅拌可以加快酸浸时反应速率 B、“酸浸”时发生反应的离子方程式为 C、“氧化”后的溶液中存在的阳离子为、、、 D、操作X为萃取分液,使用的玻璃仪器为分液漏斗和烧杯
A、将废渣粉碎同时酸浸时不断搅拌可以加快酸浸时反应速率 B、“酸浸”时发生反应的离子方程式为 C、“氧化”后的溶液中存在的阳离子为、、、 D、操作X为萃取分液,使用的玻璃仪器为分液漏斗和烧杯 -
12、根据图示的能量转化关系判断下列说法正确的是( )
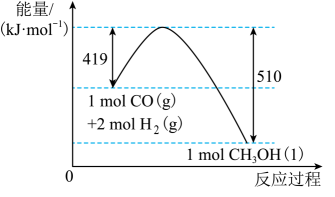 A、与反应生成32 g 吸收91 kJ能量 B、形成2 mol H-H和1 mol C≡O(CO)共吸收419 kJ的能量 C、分子中只含有极性共价键 D、1 mol 具有的能量高于2 mol 和1 mol 具有的能量
A、与反应生成32 g 吸收91 kJ能量 B、形成2 mol H-H和1 mol C≡O(CO)共吸收419 kJ的能量 C、分子中只含有极性共价键 D、1 mol 具有的能量高于2 mol 和1 mol 具有的能量 -
13、下列实验操作、现象和得出的结论正确的是( )
实验操作
现象
结论
A
取少量Fe(NO3)2溶液于试管中,滴入硫酸酸化的H2O2溶液
溶液由浅绿色变为黄色
氧化性:H2O2>Fe3+
B
取2mL0.1mol/LKI溶液于试管中,加入5mL0.1mol/LFeCl3溶液,充分反应后滴入5滴10%KSCN溶液
溶液变血红色
KI与FeCl3反应有一定限度
C
向Na2SiO3溶液中通入CO2气体
有白色沉淀生成
非金属性:C>Si
D
两只试管中均加入2mL0.1mol/L酸性KMnO4溶液,分别加入2mL0.1mol/L和0.2mol/LH2C2O4溶液,比较溶液褪色的时间
加入0.2mol/LH2C2O4溶液的褪色时间更短
其它条件相同时,反应物浓度越大,反应速率越大
A、A B、B C、C D、D -
14、反应4NH3(g)+5O2(g)4NO(g)+6H2O(g),在5L的密闭容器中进行,反应开始时NH3为1mol,半分钟后,NO的物质的量增加了0.30mol。下列叙述正确的是( )A、容器中H2O的物质的量减少了0.45mol B、NH3的平均反应速率是0.010mol/(L·s) C、当容器中NH3、O2、NO、H2O的物质的量之比是4∶5∶4∶6时,说明该反应达到平衡 D、容器中NH3的转化率为30%
-
15、海洋生物参与氮循环过程如图所示(其它含氮物质不参与反应)。下列说法不正确的是( )
 A、以上六种含氮微粒,一共呈现了氮的五种价态 B、反应①~⑤中只有1个非氧化还原反应 C、反应③中若N2H4与O2反应,则N2H4作还原剂 D、反应③和⑤若生成等质量的N2 , 转移的电子数一样多
A、以上六种含氮微粒,一共呈现了氮的五种价态 B、反应①~⑤中只有1个非氧化还原反应 C、反应③中若N2H4与O2反应,则N2H4作还原剂 D、反应③和⑤若生成等质量的N2 , 转移的电子数一样多 -
16、如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,发现试管①内的水立刻沸腾了。则液体A和气体B的组合不可能是下列的( )
 A、亚硫酸钠溶液、二氧化硫 B、氢氧化钠溶液、二氧化氮 C、饱和食盐水、氯气 D、硫酸溶液、氨气
A、亚硫酸钠溶液、二氧化硫 B、氢氧化钠溶液、二氧化氮 C、饱和食盐水、氯气 D、硫酸溶液、氨气 -
17、如图所示四种化学实验操作的名称按①②③④顺序排列分别为( )
 A、过滤、蒸馏、蒸发、萃取(或分液或萃取分液) B、蒸发、蒸馏、过滤、萃取(或分液或萃取分液) C、萃取(或分液或萃取分液)、过滤、蒸发、蒸馏 D、过滤、蒸发、蒸馏、萃取(或分液或萃取分液)
A、过滤、蒸馏、蒸发、萃取(或分液或萃取分液) B、蒸发、蒸馏、过滤、萃取(或分液或萃取分液) C、萃取(或分液或萃取分液)、过滤、蒸发、蒸馏 D、过滤、蒸发、蒸馏、萃取(或分液或萃取分液) -
18、分枝酸可用于生化研究,其结构简式如图。下列关王分枝酸的叙述正确的是( )
 A、该有机物属于芳香族化合物 B、该有机物可发生取代反应、加成反应和氧化反应 C、该有机物的分子式是C10Hl2O6 D、该有机物分子中所有原子可能处于同一平面
A、该有机物属于芳香族化合物 B、该有机物可发生取代反应、加成反应和氧化反应 C、该有机物的分子式是C10Hl2O6 D、该有机物分子中所有原子可能处于同一平面 -
19、下列物质有关用途与性质的对应关系错误的是( )
物质
用途
性质
A
浓硫酸
实验室干燥气体
浓硫酸具有吸水性
B
金属钠
用于冶炼钛、锆等金属
金属钠有强还原性
C
二氧化硫
常用于漂白秸秆、织物
能跟其中的有色物质结合
D
纯碱
用于清洗餐具
水溶液呈碱性
A、A B、B C、C D、D -
20、在给定条件下,下列选项所示的物质间转化均能实现的是( )A、NH3NO2NO B、FeFe3O4Fe C、Al2O3AlAl(OH)3 D、SiO2H2SiO3Na2SiO3