相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、由多糖和多功能无机纳米颗粒组成的多糖基复合纳米材料(直径 1- 100 nm)在生物医学领 域具有潜在的应用价值,具有协同性能和功能。多糖基复合纳米颗粒分散到水中,下列关于该分散系的说法错误的是( )A、该分散系属于胶体 B、多糖基复合纳米颗粒直径较大,不能透过滤纸 C、利用丁达尔效应可以区分氯化钡溶液和该分散系 D、一束光通过该分散系,可观察到光亮的通路
-
2、科学家为人类社会的进步作出了巨大的贡献。下列研究成果与科学家的对应关系不符合事实的是( )A、屠呦呦因发现抗疟药青蒿素而获得诺贝尔生理学或医学奖 B、侯德榜发明的侯氏制碱法推动了我国制碱工业的发展 C、道尔顿发现的分子论推动了人们对物质世界的认识 D、拉瓦锡提出的氧化学说使近代化学取得了革命性的进展
-
3、宏观辨识与微观探析相结合是重要的化学核心素养。下列不属于对宏观事实的微观解释
的选项是( )
选项
宏观事实
微观解释
A
冰水混合物是纯净物
只由一种分子组成
B
熔融的氯化钠导电
温度升高,离子运动更加剧烈,克服了离子间相互作用,可以自由移动
C
氧气变成臭氧是化学变化
分子种类发生改变
D
电解水是氧化还原反应
水中氢、氧元素的化合价发生了变化
A、A B、B C、C D、D -
4、研究CO、在一定条件下与催化合成等有机化工产品,对实现“碳中和”目标具有重要的意义。在一定条件下与可发生如下反应:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
(1)、部分物质的标准生成焓数据如表所示(由最稳定的单质合成单位量物质B的反应焓变叫做物质B的标准摩尔生成焓):物质
标准生成焓
0
x
则x=;。
(2)、一定温度范围内反应Ⅰ和反应Ⅱ的的线性关系如图所示。
①依据图像,可知℃时,反应Ⅲ的平衡常数。
②图中(填“>”、“<”或“=”)。
(3)、在密闭容器中起始时按投料,分别在压强为和的恒压下进行反应(两压强下均只发生反应Ⅱ和反应Ⅲ)。恒压条件下反应温度对平衡中体积分数(含碳元素)[x为CO或 , %]的影响如图所示。
则在时,表示和CO的平衡体积分数随温度变化关系的曲线依次是(填“a”、“b”、“c”或“d”,下同)和;在T℃、一定压强下,反应在M点达到化学平衡,平衡时的分压MPa,反应Ⅲ的平衡常数。
-
5、Na2SO3、NaHSO3是常见的化工原料,常用作还原剂。(1)、25℃,H2SO3、HSO、SO的物质的量分数[]与pH的关系如图所示。

①若向NaOH溶液中通入SO2制取NaHSO3溶液,则当溶液的pH为时应停止通入。
②向NaOH溶液中通入SO2 , 所得溶液中一定存在的等式是(用溶液中所含微粒的物质的量浓度表示)。
③NaHSO3溶液的酸碱性:。
④若测得25℃时,某溶液中=10,则溶液的pH为。
(2)、Na2SO3固体久置后会被氧化,为测定某久置Na2SO3固体中Na2SO3的含量,现进行如下实验:称取0.3000g该固体于锥形瓶中,加水溶解后,边振荡边向其中滴加0.1000mol•L-1I2标准溶液28mL,充分反应后,向溶液中滴加2滴淀粉溶液作指示剂,继续滴加0.1000mol•L-1Na2S2O3标准溶液与过量的I2反应(发生反应I2+2Na2S2O3=2NaI+Na2S4O6),恰好完全反应时消耗Na2S2O3标准溶液16mL。①如何判断滴定终点:。
②滴定过程中,滴定管液面如图所示,此时滴定管的读数为mL。

③计算久置Na2SO3固体中Na2SO3的质量分数为
④下列情况会造成样品中Na2SO3含量测定结果偏低的是(填序号)。
A.滴定过程中用蒸馏水冲洗锥形瓶瓶壁
B.装Na2S2O3标准溶液的滴定管水洗后未润洗
C.开始滴定时,滴定管尖嘴部分未充满液体
D.滴定前仰视读数,滴定后俯视读数
-
6、是食品加工中最为快捷的食品添加剂,用于焙烤食品;在分析试剂、医药、电子工业中用途广泛。请回答下列问题:(1)、可作净水剂,其理由是(用必要的化学用语和相关文字说明)。(2)、相同条件下,
中(填“等于”“大于”或“小于”)中。
(3)、如图所示是电解质溶液的pH随温度变化的图像。

①其中符合的pH随温度变化的曲线是(填Ⅰ、Ⅱ、Ⅲ、Ⅳ),导致pH随温度变化的原因是。
②20℃时,中。
(4)、室温时,向溶液中滴加溶液,所得溶液pH与溶液体积的关系曲线如图所示。试分析图中a、b、c、d四个点,水的电离程度最大的是点;在b点,溶液中各离子浓度由大到小的排列顺序是。
-
7、25℃时,等体积两种一元酸HA和HB分别用等浓度的溶液滴定,滴定曲线如图所示。下列说法正确的是( )
 A、酸性:HA<HB B、酸HB的电离度约为0.5% C、起始浓度: , D、用溶液滴定HB可用甲基橙作指示剂
A、酸性:HA<HB B、酸HB的电离度约为0.5% C、起始浓度: , D、用溶液滴定HB可用甲基橙作指示剂 -
8、在起始温度均为T℃、容积均为10L的密闭容器A(恒温)、B(绝热)中均加入和4molCO,发生反应。已知:、分别是正、逆反应速率常数, , , A、B容器中的转化率随时间的变化关系如图所示。下列说法中正确的是( )
 A、曲线M、N的平衡常数大小为: B、与浓度比为1∶1时,标志此反应已达平衡 C、T℃时, D、用CO的浓度变化表示曲线N在0~100s内的平均速率为
A、曲线M、N的平衡常数大小为: B、与浓度比为1∶1时,标志此反应已达平衡 C、T℃时, D、用CO的浓度变化表示曲线N在0~100s内的平均速率为 -
9、某研究小组以为催化剂,在容积为的容器中,相同时间下测得化为的转化率随温度变化如图所示[无CO时反应为;有CO应为。下列说法正确的是( )
 A、Y点再通入CO、各 , 此时 B、X点可以通过更换高效催化剂提高NO转化率 C、达平衡后,其他条件不变,使 , CO转化率降低 D、CO氧化NO是绿色低能耗的脱硝技术
A、Y点再通入CO、各 , 此时 B、X点可以通过更换高效催化剂提高NO转化率 C、达平衡后,其他条件不变,使 , CO转化率降低 D、CO氧化NO是绿色低能耗的脱硝技术 -
10、最新报道的“人工固氮”反应为: , 常压下测得该反应的部分数据如表所示。则关于该反应的说法中错误的是( )
T/℃
30
40
50
的平衡浓度
4.8
5.9
6.0
A、该反应的 B、常温下该反应的 C、反应在30℃、40℃时化学平衡常数分别为、 , 则 D、在常温常压下,人工固氮比较容易进行 -
11、将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s)⇌2NH3(g)+CO2(g)。下的平衡数据列下表:下列说法正确的是( )
温度/℃
15.0
20.0
25.0
30.0
35.0
平衡总压强/kPa
5.7
8.3
12.0
17.1
24.0
平衡气体总浓度/10-3 mol⋅L-1
2.4
3.4
4.8
6.8
9.4
A、该可逆反应达到平衡的标志之一是混合气体平均相对分子质量不变 B、因该反应熵变(ΔS)大于0,焓变(ΔH)大于0,所以在低温下自发进行 C、达到平衡后,若在恒温下压缩容器体积,氨基甲酸铵固体的质量增加 D、根据表中数据,计算15.0℃时的NH3平衡浓度为1.6 mol⋅L-1 -
12、常压下羰基化法精炼镍的原理:Ni(s)+4CO(g)Ni(CO)4(g)。230 ℃时,该反应的平衡常数K=2×10-5。已知:Ni(CO)4的沸点为 42.2 ℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230 ℃制得高纯镍。下列判断正确的是( )
A、增加 c(CO),平衡向正向移动,反应的平衡常数增大 B、该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO) C、第一阶段,在 30 ℃和 50 ℃两者之间选择反应温度,选50 ℃ D、第二阶段,Ni(CO)4分解率较低 -
13、相同温度下,分别在起始体积均为1L的两个密闭容器中发生反应:X2(g)+3Y2(g)2XY3(g)△H=-akJ/mol。实验测得反应的有关数据如表。下列叙述正确的是( )
容器
反应条件
起始物质的量/mol
达到平衡所用时间/min
达平衡过程中的能量变化
X2
Y2
XY3
①
恒容
1
3
0
10
放热0.1akJ
②
恒压
1
3
0
t
放热bkJ
A、对于上述反应,①、②中反应的平衡常数K的值不同 B、①中:从开始至10min内的平均反应速率v(X2)=0.1mol/(L•min) C、②中:X2的平衡转化率小于10% D、b>0.1a -
14、化学图像可以综合并直观地反应外界条件对化学反应的影响,如图所示图像是描述外界条件对化学反应的进程或结果的影响,下列说法正确的是( )
 A、图①表示在时扩大容器体积,随时间变化的曲线 B、若图②中A、B、C三点表示反应在不同温度、压强下NO的平衡转化率,则压强最小的是点B,化学平衡常数最小的是A点 C、图③表示在恒温恒容的密闭容器中,按不同投料比充入和进行反应 , 由图可知 D、图④表示工业合成氨平衡时体积分数随起始变化的曲线,则转化率:
A、图①表示在时扩大容器体积,随时间变化的曲线 B、若图②中A、B、C三点表示反应在不同温度、压强下NO的平衡转化率,则压强最小的是点B,化学平衡常数最小的是A点 C、图③表示在恒温恒容的密闭容器中,按不同投料比充入和进行反应 , 由图可知 D、图④表示工业合成氨平衡时体积分数随起始变化的曲线,则转化率: -
15、下列叙述正确的是( )A、取等体积等pH的醋酸和盐酸两种酸分别与完全一样的足量锌粒反应,开始时反应速率盐酸大于醋酸 B、取等体积等pH的醋酸和盐酸两种酸溶液分别稀释至原体积的m倍和n倍,稀释后两溶液的pH仍然相同,则m小于n C、pH均为4的盐酸和氯化铵溶液等体积混合后,所得溶液的 D、用同浓度的溶液分别与等体积、等pH的盐酸和醋酸溶液恰好完全反应,盐酸消耗溶液的体积更大
-
16、已知: ,
,
,
,
下列说法错误的是( )
A、 , B、 C、 D、 -
17、下列叙述错误的是( )A、稀溶液加水稀释,溶液的碱性减弱 B、稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强 C、在滴有酚酞的溶液中慢慢滴入溶液,溶液的红色逐渐褪去 D、pH相等的① ② ③溶液的物质的量浓度大小:①>②>③
-
18、已知电离常数: , 、。下列离子方程式书写正确的是( )A、向KCN(aq)中通入少量的气体: B、饱和碳酸钠溶液中通入 C、氢氧化铁溶于氢碘酸(强酸): D、同浓度同体积的溶液与NaOH溶液混合:
-
19、一定条件下,气态反应物和生成物的相对能量与反应进程如图所示。下列说法正确的是( )
 A、两个进程中速率最快的一步反应的 B、为进程Ⅱ的催化剂,可以减少反应热,加快反应速率 C、相同条件下,进程Ⅰ、Ⅱ中的平衡转化率不同 D、
A、两个进程中速率最快的一步反应的 B、为进程Ⅱ的催化剂,可以减少反应热,加快反应速率 C、相同条件下,进程Ⅰ、Ⅱ中的平衡转化率不同 D、 -
20、工业生产硫酸的一步重要反应是 , 如果该反应在容积不变的密闭容器中进行,图中表示当其他条件不变时,改变某一条件对上述反应的影响,其中结论正确的是( )
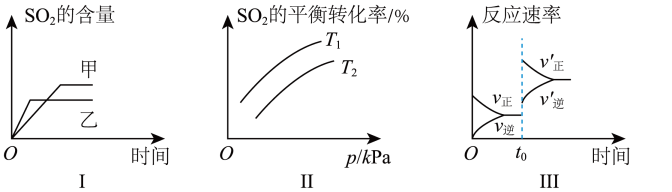 A、图Ⅰ表示催化剂对化学平衡的影响,且甲使用了催化剂 B、图Ⅰ表示温度对化学平衡的影响,且乙温度高 C、图Ⅱ表示平衡转化率与温度及压强的关系,可以判断 D、图Ⅲ表示时刻升高温度或增大压强对反应速率的影响
A、图Ⅰ表示催化剂对化学平衡的影响,且甲使用了催化剂 B、图Ⅰ表示温度对化学平衡的影响,且乙温度高 C、图Ⅱ表示平衡转化率与温度及压强的关系,可以判断 D、图Ⅲ表示时刻升高温度或增大压强对反应速率的影响