相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、有氧条件下,在Fe基催化剂表面,NH3还原NO的反应机理如图所示。该反应能够有效脱除烟气中的NO。下列说法正确的是( )
 A、在酸性配位点上,NH3与H+通过离子键形成NH4+ B、增大压强有利于NO与O2吸附在Fe3+配位点上形成NO2 C、反应物NH3和生成物H2O的杂化类型分别为sp3、sp2 D、催化剂表面发生的总反应为4NH3+6NO=5N2+6H2O
A、在酸性配位点上,NH3与H+通过离子键形成NH4+ B、增大压强有利于NO与O2吸附在Fe3+配位点上形成NO2 C、反应物NH3和生成物H2O的杂化类型分别为sp3、sp2 D、催化剂表面发生的总反应为4NH3+6NO=5N2+6H2O -
2、X、Y、Z、W、P五种元素,核电荷数依次增大。X基态原子核外只有三个能级,且各能级电子数相等;Z与W元素位于同一主族,且W的核电荷数是Z的2倍;P原子核外有4个能层,最外层只有1个电子,其余各层均排满电子。下列说法正确的是( )A、元素的第一电离能:Z>Y>X B、Y和Z最多能形成5种二元化合物 C、基态P原子的价层电子排布式为4s1 D、P单质分别与Z、W单质反应,产物中P的化合价不同
-
3、实验室用以下装置(夹持和加热装置略)制备乙酸异戊酯(沸点142℃),实验中利用环己烷-水的共沸体系(沸点69℃)带出水分。已知体系中沸点最低的有机物是环己烷(沸点81℃),其反应原理如下。下列说法不正确的是( )

 A、使用稍过量乙酸能提高异戊醇的转化率 B、装置A的加热方式为水浴加热 C、以共沸体系带水能促使反应正向进行 D、乙酸异戊酯最终在装置B中收集到
A、使用稍过量乙酸能提高异戊醇的转化率 B、装置A的加热方式为水浴加热 C、以共沸体系带水能促使反应正向进行 D、乙酸异戊酯最终在装置B中收集到 -
4、由下列实验操作和现象,能得到对应结论的是( )
选项
实验操作
现象
结论
A
向NaBr溶液中滴加足量氯水,再加入淀粉-KI溶液
溶液先变橙色,后变蓝色
氧化性:Cl2>Br2>I2
B
向乙醇中加入一小粒金属钠
产生无色气体
乙醇中含有水
C
将Fe3O4溶于稀硫酸,再滴入KMnO4溶液
溶液紫色褪去
Fe3O4中含有Fe2+
D
向Ca(ClO)2溶液中通入SO2气体
有沉淀生成
酸性:H2SO3>HClO
A、A B、B C、C D、D -
5、含铁物质或微粒所带电荷数与化合价的关系如图所示,下列说法不正确的是( )
 A、若M为氢氧化物,则制备M所用的溶液需先煮沸 B、常温下,可以用R制的容器盛装浓硝酸 C、可用KSCN溶液检验N D、Fe3+与强氧化剂在碱性条件下可反应生成FeO42-
A、若M为氢氧化物,则制备M所用的溶液需先煮沸 B、常温下,可以用R制的容器盛装浓硝酸 C、可用KSCN溶液检验N D、Fe3+与强氧化剂在碱性条件下可反应生成FeO42- -
6、实验室用如图所示装置研究不同价态硫元素之间的转化,下列说法正确的是( )
 A、将①中生成的气体通入BaCl2溶液中会出现白色沉淀 B、②中棉花紫色褪去,体现SO2的漂白性 C、③中有黄色固体生成,氧化剂与还原剂物质的量之比为2∶1 D、实验后向④的小烧杯中加入足量盐酸,可能产生黄绿色气体
A、将①中生成的气体通入BaCl2溶液中会出现白色沉淀 B、②中棉花紫色褪去,体现SO2的漂白性 C、③中有黄色固体生成,氧化剂与还原剂物质的量之比为2∶1 D、实验后向④的小烧杯中加入足量盐酸,可能产生黄绿色气体 -
7、近日北京大学肿瘤医院发现,天然小分子白皮杉醇在胃癌治疗中有重要应用价值。其结构如图所示,下列有关白皮杉醇的说法不正确的是( )
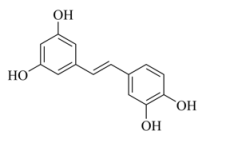 A、分子式为C14H12O4 B、苯环上氢原子的一氯代物有4种 C、能发生取代、加成、氧化、加聚反应 D、分子中所有原子可能在同一平面
A、分子式为C14H12O4 B、苯环上氢原子的一氯代物有4种 C、能发生取代、加成、氧化、加聚反应 D、分子中所有原子可能在同一平面 -
8、五育并举,劳动先行。下列劳动项目与所述的化学知识具有关联的是( )
选项
劳动项目
化学知识
A
学农活动:用厨余垃圾制肥料
厨余垃圾含N、P、K等元素
B
社区服务:宣传推广使用84消毒液
84消毒液呈碱性
C
帮厨活动:检验食盐是否加碘
食盐中的碘为KI
D
工厂实践:向食品包装袋内充氮气
氮气的密度接近空气
A、A B、B C、C D、D -
9、下列解释事实的离子方程式正确的是( )A、过量铁粉与稀硝酸反应:Fe +NO3- +4H+ = Fe3++NO↑+2H2O B、将稀硫酸滴入Na2S2O3溶液中:2H++ S2O32- = SO2↑+S↓+H2O C、向海水提溴工艺中用SO2溶液吸收Br2:Br2+SO2+2H2O = 2H++SO42-+2HBr D、向酸性FeI2溶液中滴入少量H2O2稀溶液:2Fe2++ H2O2 +2H+ = 2Fe3+ +2H2O
-
10、设NA为阿伏加德罗常数的值。下列说法不正确的是( )A、2.8 g N2与CO混合气体中含有原子数目为0.2 NA B、0.1 mol氯气分别与足量铁和铜完全反应时转移的电子数均为0.2 NA C、16.9 g过氧化钡(BaO2)固体中阴、阳离子总数为0.3 NA D、1 L pH=1的H2SO4溶液中含有H+的数目为0.1 NA
-
11、实验室从废定影液[含Ag(S2O3)23-和Br -等]中回收Ag和Br2的主要步骤为:向废定影液中加入Na2S溶液沉银,过滤、洗涤及干燥,灼烧Ag2S制Ag;制取Cl2并通入滤液氧化Br - , 用苯萃取分液。其中部分操作的装置如图,下列叙述正确的是( )
 A、用装置甲分离Ag2S时,用玻璃棒不断搅拌 B、用装置乙在空气中高温灼烧Ag2S制取Ag C、用装置丙制备用于氧化滤液中Br -的Cl2 D、用装置丁分液时,从下口放出有机相
A、用装置甲分离Ag2S时,用玻璃棒不断搅拌 B、用装置乙在空气中高温灼烧Ag2S制取Ag C、用装置丙制备用于氧化滤液中Br -的Cl2 D、用装置丁分液时,从下口放出有机相 -
12、化学“暖手袋”是充满过饱和醋酸钠溶液的密封塑胶袋,袋内置有一个合金片,当合金片轻微震动使溶质结晶,该过程放热,下列说法正确的是( )A、醋酸钠溶液属于强电解质 B、可以利用醋酸与NaHCO3溶液反应制备醋酸钠溶液 C、化学“暖手袋”工作过程中发生了化学变化 D、所有物质溶解过程均吸热,结晶过程均放热
-
13、中国“天宫”空间站运用的“黑科技”很多,下列对所涉及物质性质的描述正确的是( )A、“百变金刚”太空机械臂主要成分为铝合金,具有硬度大、熔点高等优点 B、“问天”实验舱采用了砷化镓太阳能电池片,能将光能转化为化学能 C、核心舱配置的离子推进器以氙和氩气作为推进剂,氙和氩属于副族元素 D、电池翼采用碳纤维框架和玻璃纤维网,二者均为无机非金属材料
-
14、建筑承载着文明。下列建筑材料的主要成分属于金属材料的是( )




A.PVC管道
B.不锈钢管材
C.钢化玻璃
D.砂石
A、A B、B C、C D、D -
15、工业上用氯化铁腐蚀铜箔制造电路板。某实验小组为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
(1)、试剂a与腐蚀废液反应的离子方程式为。(2)、试剂b是 , 操作Ⅱ为。滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为 。上述流程中操作Ⅲ包括在HCl气流中蒸发浓缩、、过滤、洗涤。 -
16、类比推理是研究物质性质的常用方法,可预测许多物质的性质,但类比是相对的,不能违背客观实际。下列说法中正确的是( )A、与水反应生成和 , 推测与水反应生成和 B、与反应生成 , 则与反应生成 C、溶液与反应生成、 , 则溶液与反应生成和 D、少量通入溶液中产生白色沉淀,则少量通入溶液也产生白色沉淀
-
17、一种提纯白磷样品(含惰性杂质)的工艺流程如图所示。下列说法不正确的是( )
 A、过程Ⅰ中,白磷既做氧化剂又做还原剂 B、过程Ⅱ中,发生复分解反应 C、过程Ⅲ中,反应的化学方程式: D、理论上,通过本提纯工艺不会产生白磷损失
A、过程Ⅰ中,白磷既做氧化剂又做还原剂 B、过程Ⅱ中,发生复分解反应 C、过程Ⅲ中,反应的化学方程式: D、理论上,通过本提纯工艺不会产生白磷损失 -
18、在体积固定的密闭容器中,发生反应:2CO(g) + 4H2(g) ⇋CH3CH2OH(g)+H2O(g) 下列叙述中不能说明上述反应已达到化学反应限度的是( )A、混合气体密度不变 B、体系压强不变 C、混合气体的平均相对分子质量不变 D、反应体系中乙醇的物质的量浓度不再变化
-
19、是国际上公认的新一代高效、安全、环保的杀菌消毒剂。利用(Fe的化合价为+2)制备和用除去水体中的反应如下:反应①:
反应②: 下列说法正确的是( )A、反应①中,是还原剂,发生还原反应 B、反应中①,每生成1mol , 反应转移1mol电子 C、由反应①可知:氧化产物只有 D、由反应②可知酸性:大于HCl -
20、下列各组离子在给定条件的溶液中一定能大量共存的是( )A、在强酸性溶液中:、、、 B、加入铝粉有大量氢气产生的溶液中:、、、 C、在无色溶液中:、、、 D、滴入酚酞显红色的溶液中:、、、