相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列事实中一定能证明CH3COOH是弱电解质的是( )
①用CH3COOH溶液做导电实验,灯泡很暗
②溶液中
③往NaHCO3溶液中滴加CH3COOH溶液,产生大量气泡
④溶液恰好与溶液完全反应
⑤1 mL 的CH3COOH溶液稀释至1L,
A、②⑤ B、②③ C、①② D、③④ -
2、已知: , 不同条件下反应进程的能量变化如图所示。下列说法正确的是能量( )
 A、该反应达平衡时,升高温度,v(正)增大,v(逆)减小,平衡逆向移动 B、过程b使用了催化剂,使反应的减小 C、由可知,该反应低温能自发进行 D、恒温恒容条件下通入氦气,可使单位体积内O2的活化分子数增大
A、该反应达平衡时,升高温度,v(正)增大,v(逆)减小,平衡逆向移动 B、过程b使用了催化剂,使反应的减小 C、由可知,该反应低温能自发进行 D、恒温恒容条件下通入氦气,可使单位体积内O2的活化分子数增大 -
3、下列各可逆反应达平衡后,改变反应条件,其变化趋势正确的是( )A、
 B、
B、 C、
C、 D、
D、
-
4、已知反应①和反应②在T℃时的平衡常数分别为K1和K2 , 该温度下反应③的平衡常数为K3。则下列说法正确的是( )A、反应①的平衡常数 B、反应②中,增大氢气浓度,平衡时其体积分数增大 C、对于反应③,CO和H2O的转化率一定相等 D、T℃时,
-
5、下列事实能用勒夏特列原理解释的是( )A、工业上SO2催化氧化为SO3 , 采用常压而不是高压 B、由NO2和N2O4组成的平衡体系: , 恒温缩小容积,气体颜色变深 C、 , 工业上将钾蒸气从反应混合体系中分离出来,以制备金属钾 D、500℃高温比室温更有利于合成氨的反应
-
6、在一定温度下,下列叙述不是可逆反应达到平衡的标志的是( )
①C的生成速率与C的分解速率相等;
②单位时间内生成a mol A,同时生成3a mol B;
③A、B、C的浓度不再变化;
④A、B、C的体积分数不再变化;
⑤混合气体的总压强不再变化;
⑥混合气体的物质的量不再变化;
⑦单位时间内消耗a mol A,同时生成3a mol B;
⑧A、B、C、D的分子数之比为1:3:2:2。
A、②⑧ B、②⑤⑧ C、①③④⑦ D、②⑤⑥⑧ -
7、下列实验不能达到目的的是( )
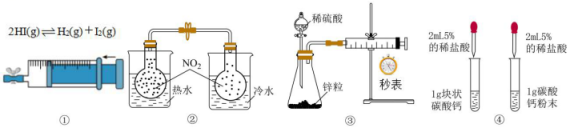 A、图①:探究压强对化学平衡的影响 B、图②:探究温度对化学平衡的影响 C、图③:测定锌与稀硫酸反应的反应速率 D、图④:探究反应物的接触面积对反应速率的影响
A、图①:探究压强对化学平衡的影响 B、图②:探究温度对化学平衡的影响 C、图③:测定锌与稀硫酸反应的反应速率 D、图④:探究反应物的接触面积对反应速率的影响 -
8、在5L的密闭容器中进行反应 , 10s后,SO3的物质的量增加了0.3mol。下列叙述正确的是( )A、 B、 C、当容器内气体密度不再变化时,反应达到平衡 D、当容器内SO3的消耗速率等于SO2的生成速率,反应达到平衡
-
9、下列热化学反应方程式书写正确的是(的绝对值均正确)( )A、 (燃烧热) B、 (中和热) C、 (反应热) D、 (反应热)
-
10、下列反应中,反应物键能大于生成物键能的是( )A、锌粒与稀盐酸反应 B、与NH4Cl反应 C、酸碱中和反应 D、甲烷在O2中燃烧
-
11、有机物Ⅸ是合成酮基布洛芬的重要中间体,一种合成Ⅸ的路线如图:

已知:
①

②

回答下列问题:
(1)、化合物Ⅴ中含有的官能团的名称为;化合物Ⅵ的结构简式为。(2)、验证苯中混有化合物Ⅳ的方法是。(3)、写出反应Ⅵ→Ⅶ的化学方程式: , 该反应的反应类型为。(4)、化合物Ⅳ的同分异构体中能同时满足以下条件的有种(不考虑立体异构)。a.含有联苯结构(
 )且其中一个苯环除连有另一个苯环外,无其他侧链;
)且其中一个苯环除连有另一个苯环外,无其他侧链;b.能发生银镜反应。
(5)、结合以上合成路线信息,设计以 、
、 为原料(其他试剂任选)合成
为原料(其他试剂任选)合成 的路线。
的路线。 -
12、碳中和作为一种新型环保形式,目前已经被越来越多的大型活动和会议采用。回答下列有关问题:(1)、利用合成二甲醚有两种工艺。
工艺1:涉及以下主要反应:
Ⅰ.甲醇的合成:
Ⅱ.逆水汽变换:
Ⅲ.甲醇脱水:
工艺2:利用直接加氢合成(反应Ⅳ)
①反应Ⅳ的热化学方程式为 , 平衡常数(用、表示)。
②恒温恒容情况下,下列说法能判断反应Ⅳ达到平衡的是。
A.气体物质中碳元素与氧元素的质量比不变
B.容器内压强不变
C.容器内气体密度不变
D.容器内浓度保持不变
(2)、工艺1需先合成甲醇。在不同压强下,按照投料合成甲醇,实验测定的平衡转化率和的平衡产率随温度的变化关系如下图所示。
①下列说法正确的是
A.图甲纵坐标表示的平衡产率
B.
C.为了同时提高的平衡转化率和的平衡产率,应选择低温、高压条件
D.一定温度压强下,提高的平衡转化率的主要方向是寻找活性更高的催化剂
②图乙中,某温度时,三条曲线几乎交于一点的原因是。
(3)、对于合成甲醇的反应: , 一定条件下,单位时间内不同温度下测定的转化率如图丙所示。温度高于710K时,随温度的升高转化率降低的原因可能是。 -
13、碱式碳酸铜在烟火、农药、颜料、杀菌剂等方面应用广泛。一种以辉铜矿( , 含有和少量等杂质)为原料制备碱式碳酸铜的流程如图所示:

已知: , 为无色液体,是硫、磷、硒、溴、碘、樟脑等的良好溶剂,具有挥发性。
回答下列问题:
(1)、加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有(任写一种)。(2)、滤渣Ⅰ经提取后可获得一种淡黄色副产品,则滤渣I中的主要成分是(填化学式)。由回收滤渣I中的淡黄色副产品过程中温度控制在50~60℃之间,不宜过高或过低的原因是。(3)、“除铁”时检验是否除尽时常用的化学试剂。(4)、写出“沉锰”(除)过程中反应的离子方程式:。(5)、“赶氨”时,最适宜的操作方法是。(6)、测定副产品样品的纯度:准确称取样品14.00g,加蒸馏水配成100mL溶液,取出25.00mL用标准的溶液测定,完全反应后得到了4.66g沉淀,则此样品的纯度为(保留到小数点后两位) -
14、某种常见补铁药物的主要成分为琥珀酸亚铁,该药品难溶于水但能溶于常见稀酸。某学习小组同学设计实验检验药片中的存在并测定的含量(假设杂质不参与反应)。已知与会产生蓝色沉淀。回答下列问题:(1)、甲同学为了检验药品中的存在。将药物碾碎、水溶后过滤。取少量所得滤液于两支试管中,分别加入溶液和KSCN溶液,观察并记录实验现象。
①甲同学过滤时进行的下列操作不规范的是(填标号)。
a.用玻璃棒在漏斗中搅动以加快过滤速率
b.滤纸边缘高于漏斗边缘
c.将滤纸润湿,使其紧贴漏斗内壁
②滤液加入溶液或KSCN溶液中均未出现明显现象,其主要原因为。
(2)、乙同学设计如下实验测定药片中的含量。步骤一:取本药品10片,碾碎后加入一定浓度的稀硫酸,在适当的条件下配成100mL溶液。
步骤二:准确量取20.00mL步骤一所得溶液放入烧杯中。
步骤三:向烧杯中加入过量溶液后,再加入过量NaOH溶液,产生沉淀,将沉淀过滤出来后洗涤、干燥,灼烧至固体质量恒定,得0.64g固体。
①步骤二中,量取20.00mL溶液应使用的仪器为(填“酸式滴定管”、“碱式滴定管”或“25mL量筒”)。
②步骤三中,加入溶液时发生反应的离子方程式为 , 灼烧后所得固体的颜色为。
③若将步骤三中的溶液换为也能达到目的,但使用溶液的好处是。
④由实验数据计算,每片药片中含mg 。
(3)、也可用作补铁剂,使用时建议与维生素C同服,甲同学猜测维生素C可将转化为 , 以利于人体吸收。为了验证这一猜想,设计了如下实验:实验方案
实验现象
取适量溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液
紫色褪去
由上述实验能否得出“维生素C可将转化为”的结论?回答并说明理由:。
-
15、室温时,向100mL 0.1 溶液中滴加0.1 NaOH溶液,溶液pH随NaOH溶液体积的变化如图所示。下列说法正确的是( )
 A、a点处存在 B、b点处存在 C、由b到c发生反应的离子方程式为 D、图中a、b、c、d四个点,水的电离程度最大的是d点
A、a点处存在 B、b点处存在 C、由b到c发生反应的离子方程式为 D、图中a、b、c、d四个点,水的电离程度最大的是d点 -
16、纳米硅基锂电池是一种新型二次电池,电池装置如图所示,电池充电时,三元锂电极上发生的电极反应为。下列说法错误的是( )
 A、电池工作时,硅基电极上发生的电极反应: B、电池工作时,三元锂电极为正极,发生还原反应 C、充电时,由三元锂电极经电解质溶液移向硅基电极 D、为提高电池工作效率并延长电池使用寿命,可将有机聚合物电解质换为锂盐水溶液
A、电池工作时,硅基电极上发生的电极反应: B、电池工作时,三元锂电极为正极,发生还原反应 C、充电时,由三元锂电极经电解质溶液移向硅基电极 D、为提高电池工作效率并延长电池使用寿命,可将有机聚合物电解质换为锂盐水溶液 -
17、有机物M是重要的药物合成中间体。下列关于有机物M的说法错误的是( )
 A、分子中所有的原子不可能共平面 B、能与发生显色反应 C、1mol有机物M最多能与22mol 发生加成反应 D、分子中的碳原子有2种杂化方式
A、分子中所有的原子不可能共平面 B、能与发生显色反应 C、1mol有机物M最多能与22mol 发生加成反应 D、分子中的碳原子有2种杂化方式 -
18、类比法是一种学习化学的重要方法。下列说法错误的是( )A、溶液显碱性,则溶液显碱性 B、为三角锥形分子,则为三角锥形分子 C、与水反应生成乙炔,则与水反应生成丙炔 D、酸性强于 , 则酸性强于
-
19、下列实验操作与现象和结论对应正确的是( )
实验操作与现象
结论
A
加热盛有少量固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变蓝
显碱性
B
向某溶液中先加入氯化钡溶液,再滴入盐酸,先产生白色沉淀,后白色沉淀不消失
该溶液中可能含有
C
将晶体溶于稀硫酸,再滴加KSCN溶液,溶液变红
晶体已氧化变质
D
向2支盛有2mL不同浓度溶液的试管中同时加入221mL 2%溶液,未观察到明显的实验现象差异
浓度对反应速率的影响不大
A、A B、B C、C D、D -
20、设为阿伏加德罗常数的值,下列叙述正确的是( )A、0.4mol白磷( , 正四面体结构)含共价键的数目为1.2 B、0.1mol 与0.1mol 反应,生成的分子数为0.1 C、常温下,将2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3 D、常温常压下,2.2g由和组成的混合气体中含有的原子总数为0.15