相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、KClO3与浓盐酸的反应是实验室制备氯气的方法之一: , 下列说法错误的是( )A、氧化性:KClO3>Cl2 B、被氧化的氯原子与被还原的氯原子的物质的量之比为5:1 C、用双线桥法表示电子得失情况:
 D、HCl在反应中表现出还原性和酸性
D、HCl在反应中表现出还原性和酸性
-
2、在下列物质间的每一步转化中(反应条件已经略去),不能只通过一步反应实现的是( )A、Na→Na2O→Na2CO3→NaHCO3→NaOH B、S→SO2→H2SO3→Na2SO3 C、C﹣CO→CO2→Na2CO3 D、Cl2→FeCl2→FeCl3→Fe(OH)3
-
3、从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。以下是氯元素形成物质的二维图的部分信息。下列说法正确的是( )
 A、HCl中氯显﹣1价,是氯的最低价态,因此盐酸只有还原性 B、要实现反应④⑤⑥,要加入氧化剂 C、反应⑦⑧⑨⑩都属于氧化还原反应 D、氯的最高价氧化物化学式为Cl2O7
A、HCl中氯显﹣1价,是氯的最低价态,因此盐酸只有还原性 B、要实现反应④⑤⑥,要加入氧化剂 C、反应⑦⑧⑨⑩都属于氧化还原反应 D、氯的最高价氧化物化学式为Cl2O7 -
4、下列实验操作、现象及结论都正确的是( )
选项
实验操作和现象
结论
A
向氯水中滴加石蕊试液,溶液先变红后褪色
溶液中有盐酸和次氯酸
B
取少量溶液X加入稀盐酸至溶液呈酸性,产生使澄清石灰水变浑浊的无色无味气体
该溶液中含有
C
取少量金属Na放在坩埚中灼烧,产生白色固体
该白色固体为Na2O2
D
金属Na与TiCl4水溶液反应可制备Ti
说明Na 比Ti活泼
A、A B、B C、C D、D -
5、Cl2与NH3可发生反应: , 生成的氯化铵呈白烟状,此反应常用于检验氯气管道是否漏气。对这一反应描述正确的是( )A、NH4Cl既是氧化产物又是还原产物 B、反应中,Cl2是氧化剂,发生氧化反应 C、若有213gCl2完全参加反应,被氧化的NH3有136g D、若生成1个N2 , 反应中转移6个e
-
6、数字化实验是利用传感器和信息处理终端进行实验数据的采集和分析。光照装有氯水的广口瓶,测定氧气的体积分数随时间变化如图,下列关于氯水光照过程说法不正确的是( )
 A、溶液pH变大 B、变大 C、颜色变浅 D、滴入紫色石蕊可能只变红不褪色
A、溶液pH变大 B、变大 C、颜色变浅 D、滴入紫色石蕊可能只变红不褪色 -
7、下列离子方程式正确的是( )A、氨水与盐酸反应: B、钠与水的反应: C、氯气溶于水: D、碳酸氢钠与氢氧化钠反应:
-
8、以下各组离子能在溶液中大量共存的是( )A、含有大量的溶液:加入、、、 B、滴加酚酞变红的溶液:加入、、、 C、所含溶质为NaHSO4的溶液:加入、、、 D、含有大量NaClO的溶液中:、、、
-
9、表中对于相关物质的分类全部正确的是( )
编号
纯净物
混合物
酸性氧化物
碱性氧化物
电解质
非电解质
A
液氯
氨水
CO
Na2O
NH3·H2O
NH3
B
纯碱
冰水混合物
SO2
CaO
NaHCO3
Cl2
C
熟石灰
合金
SiO2
Fe2O3
Na2CO3
乙醇
D
氢气
盐酸
CO2
Na2O2
K2SO4
CO
A、A B、B C、C D、D -
10、化学在生产和日常生活中有着重要的应用,下列说法不合理的是( )A、Na2CO3可用于制玻璃、肥皂、造纸、纺织等工业,NaHCO3可用于治疗胃酸过多、制造发酵粉等,它们都可以用作食用碱 B、盐碱地(含较多Na2CO3等)不利于作物生长,可施加熟石灰进行改良 C、Na2O2常用作潜水艇或呼吸面具的供氧剂 D、氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
-
11、自从1909年化学家哈伯研究出合成氨的方法以来,氮的化合物在生产生活中有着广泛应用,与此有关的研究已经获得三次诺贝尔化学奖。目前气态含氮化合物及相关转化仍然是科学家研究的热门问题。请回答下列问题:(1)、①合成氨的原料气H2可以通过天然气和二氧化碳转化制备,已知CH4、H2和CO的燃烧热(ΔH)分别为 , , 则通过天然气和二氧化碳转化制备H2的热化学反应方程式为。
②673K时,合成氨反应机理中各步反应的能量变化如图所示,其中吸附在催化剂表面上的粒子用“*”标注。
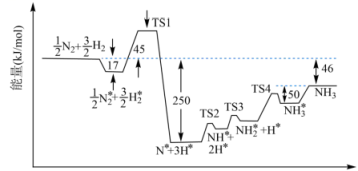
图中决速步骤的反应方程式为。
(2)、用NH3催化还原NO,可以消除氮氧化物的污染。已知:①
②
写出NH3还原NO至N2和水蒸气的热化学方程式。
(3)、活性炭还原法是消除氮氧化物污染的有效方法,其原理为:。已知该反应的正、逆反应速率方程分别为、 , 其中、分别为正、逆反应速率常数,变化曲线如左下图所示,则该反应的反应热O(填“>”、“<”或“=”),写出推理过程
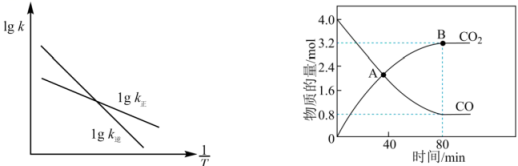 (4)、一定温度下,在体积为2L的恒容密闭容器中加入和发生反应 , 测得和的物质的量随时间的变化如右上图所示:
(4)、一定温度下,在体积为2L的恒容密闭容器中加入和发生反应 , 测得和的物质的量随时间的变化如右上图所示:①在A点时,N2O的生成速率N2的生成速率(填“>”、“<”或“=”)。
②若平衡时总压强为p kPa,用平衡分压代替其平衡浓度表示的化学平衡常数(平衡分压=总压×物质的量分数)。
-
12、已知 , 常温下N2O4为无色气体。(1)、某课外活动小组为了探究压强对化学平衡的影响,设计了相关实验,请根据所学知识预测实验结果:
在容积为30cm3针筒中抽入10cm3的NO2气体,将针筒前端封闭,静置一段时间至气体颜色不变。将针筒活塞拉至20cm3处,此时气体的颜色(填“变深”、“变浅”或“不变”),一段时间后气体颜色(填“变深”、“变浅”或“不变”),但仍比拉动活塞之前针筒内气体的颜色(填“深”或“浅”)。在此过程中,该反应的化学平衡常数(填“增大”、“减小”或“不变”),混合气体中NO2的百分含量(填“增大”、“减小”或“不变”)。
(2)、利用现代手持技术传感器可以探究压强对该平衡的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。

①有关该过程说法正确的是。
a.E、H两点对应的NO2的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
②反应至B点时NO2的转化率为。
③图像中C、E两点气体平均摩尔质量较大的点为(填代号)。
(3)、某温度下,在体积恒为1 L的密闭容器内,起始时只加入1 mol NO2 , 达到平衡时其转化率为75%,则该温度下反应的平衡常数L⋅mol-1。 -
13、重铬酸钾(K2Cr2O7)又名红矾钾,是化学实验室中的一种重要分析试剂,在工业上用途广泛。已知K2Cr2O7溶液中存在平衡:
请回答下列问题:
(1)、K2Cr2O7溶液中反应平衡常数的表达式为。(2)、复分解法制备重铬酸钾以Na2CrO4溶液为原料,步骤如下:
①先向Na2CrO4溶液中加入酸调节溶液pH,其目的是。
②再向①的溶液中加入适量KCl,搅拌溶解、蒸发浓缩、冷却结晶,抽滤得到K2Cr2O7粗产品。则相同温度时的溶解度:Na2Cr2O7K2Cr2O7(填“>”“<”或“=”)。
(3)、K2Cr2O7溶液中存在的平衡又可分解为以下两步:(ⅰ)
(ⅱ)

①下列有关K2Cr2O7溶液的说法正确的有。
A.加入少量硫酸,溶液颜色由橙色向黄色转变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量NaOH溶液,反应(ⅰ)的平衡逆向移动
D.加入少量K2Cr2O7固体,平衡时与的比值保持不变
②在0.10 mol⋅L-1 K2Cr2O7溶液中设、、的平衡浓度分别为x、y、z mol·L-1 , 则x、y、z之间的关系式为=0.10。
③已知在稀溶液中,一种物质对光的吸收程度(A)与其所吸收光的波长(λ)有关;在一定波长范围内,最大A对应的波长()取决于物质的结构特征;浓度越高,A越大。混合溶液在某一波长的A是各组分吸收程度之和。为研究对反应(ⅰ)和(ⅱ)平衡的影响,配制浓度相同、pH不同的K2Cr2O7稀溶液,测得其A随λ的变化曲线如右上图所示,波长λ1、λ2和λ3中,与的最接近的是;溶液pH从a变到b的过程中,的值(填“增大”“减小”或“不变”)。
-
14、食醋是烹饪美食的调味品,有效成分主要为醋酸(CH3COOH也可用HAc表示)。CH3COOH的应用与其电离平衡密切相关。(1)、某小组研究25℃下CH3COOH电离平衡的影响因素。
提出假设:稀释CH3COOH溶液或改变浓度,HAc电离平衡会发生移动。
设计方案并完成实验:
用浓度均为的CH3COOH和CH3COONa溶液,按下表配制总体积相同的系列溶液;测定 , 记录数据(表格中CH3COOH和CH3COONa分别用HAc和NaAc表示)。
序号
Ⅰ
40.00
/
/
0
Ⅱ
4.00
/
36.00
0
…
Ⅶ
4.00
a
33.00
3:4
Ⅷ
4.00
4.00
b
1:1
①根据表中信息,补充数据:a= , b=。
②由实验Ⅰ和Ⅱ可知,稀释CH3COOH溶液,电离平衡(填“正”或“逆”)向移动。
③由实验Ⅱ-Ⅷ可知,增大浓度,CH3COOH电离平衡逆向移动。
实验结论假设成立。
(2)、下列方法中可以使的CH3COOH电离程度增大的是____(填字母)。A、加入少量的稀盐酸 B、加热该CH3COOH溶液 C、加入少量冰醋酸 D、加水稀释至 E、加入少量氯化钠晶体 F、加入少量的NaOH溶液(3)、某化学实验小组欲测定反应的热效应,设计如下实验。实验装置:

室温/℃
20.0
20.0
20.0
ΔT/℃
0.70
0.69
0.71
实验步骤:
在装有温度计和仪器X的烧杯中先加入已恒定为室温的0.1 mol⋅L-1 NaOH溶液100mL,使用仪器X搅拌,待温度计数字稳定读数后,迅速加入0.1 mol⋅L-1 CH3COOH溶液100mL。密切关注温度变化,将最高温度记为反应后体系的温度,计算出溶液上升的温度ΔT。重复上述操作3次,记录实验数据如上表所示:
已知:反应Ⅰ.
反应Ⅱ.
本实验条件下,混合溶液的密度和比热容分别按照1 g/mL和进行计算。
回答下列问题:
①本实验重复进行三次的目的为。
②由题给数据计算可知反应Ⅰ的。
③反应的热效应(用符号ΔH1和ΔH2表示)。
-
15、部分弱电解质的电离常数如下表:
弱电解质
HCOOH
HCN
H2CO3
电离常数(25℃)
下列说法错误的是( )
A、根据电离常数,可判断酸性HCOOH>H2CO3>HCN B、可能发生反应 C、0.1 mol/L HCN溶液中存在平衡: , 加水可使溶液中变大 D、25℃时,反应的化学平衡常数约为 -
16、“千畦细浪舞晴空”,氮肥保障了现代农业的丰收。为探究的离子键强弱,设计如图所示的循环过程,可得为( )
 A、+533 B、+686 C、+838 D、+1143
A、+533 B、+686 C、+838 D、+1143 -
17、某温度下,HNO2和CH3COOH的电离常数分别为:和。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是( )
 A、曲线Ⅰ代表HNO2溶液 B、两种溶液中加入足量镁条充分反应后,产生氢气体积相同 C、溶液中溶质的电离程度:c点>d点 D、溶液的导电能力:b点>c点>d点
A、曲线Ⅰ代表HNO2溶液 B、两种溶液中加入足量镁条充分反应后,产生氢气体积相同 C、溶液中溶质的电离程度:c点>d点 D、溶液的导电能力:b点>c点>d点 -
18、温度为T时,向2.0L恒容密闭容器中充入1.0 mol PCl5 , 反应经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s
0
50
150
250
350
0
0.16
0.19
0.20
0.20
下列说法正确的是( )
A、反应在前50s的平均速率 B、保持其他条件不变,升高温度,平衡时 , 则反应的 C、相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2 , 反应达到平衡前v(正)>v(逆) D、相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2 , 达到平衡时,PCl3的转化率小于80% -
19、标准状况下,气态反应物和生成物的相对能量与反应历程示意图如下[已知和的相对能量为0],下列说法错误的是( )
 A、 B、相同条件下,O3的平衡转化率:历程Ⅱ>历程Ⅰ C、可计算Cl—Cl键能为 D、历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
A、 B、相同条件下,O3的平衡转化率:历程Ⅱ>历程Ⅰ C、可计算Cl—Cl键能为 D、历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为: -
20、根据以下热化学方程式,和的大小比较不正确的是( )A、; , 则 B、; , 则 C、; , 则 D、; , 则