相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、我国化学家侯德榜改进国外的纯碱生产工艺,生产流程如图所示:

下列说法中不正确的是( )
A、循环2中的气体X为CO2 B、沉淀池中得到的沉淀为碳酸氢钠 C、为提高原料氯化钠的利用率,主要是设计了循环1 D、向饱和食盐水中先通入足量的CO2 , 再通入足量的NH3 -
2、下列实验装置可以达到实验目的是( )
A
B
C
D


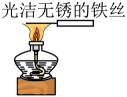

验证和反应是否放热
除去中的
焰色试验检验固体中是否含有钾元素
比较、的稳定性
A、A B、B C、C D、D -
3、实验室制取Cl2时,净化与收集Cl2所需装置如图所示。下列说法错误的是( )
 A、装置接口连接顺序为d→c→b→a→e B、饱和食盐水可用来除去HCl杂质 C、干燥纯净的Cl2能使鲜花褪色,所以Cl2具有漂白性 D、烧杯中发生反应的化学方程式:Cl2+2NaOH=NaCl+NaClO+H2O
A、装置接口连接顺序为d→c→b→a→e B、饱和食盐水可用来除去HCl杂质 C、干燥纯净的Cl2能使鲜花褪色,所以Cl2具有漂白性 D、烧杯中发生反应的化学方程式:Cl2+2NaOH=NaCl+NaClO+H2O -
4、下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项
陈述Ⅰ
陈述Ⅱ
陈述Ⅲ
A
纯碱可用于治疗胃酸过多
纯碱可与盐酸反应
Ⅰ对,Ⅱ对,无
B
将过氧化钠加入石蕊溶液中,石蕊先变红,后褪色
过氧化钠与水反应生成氢氧化钠,有氧化性物质生成
Ⅰ对,Ⅱ对,有
C
金属钠保存在煤油中以隔绝空气
常温下,金属钠在空气中会被氧化生成过氧化钠
Ⅰ对,Ⅱ对,有
D
过氧化钠可用于制作呼吸面罩
过氧化钠能和、反应生成氧气
Ⅰ对,Ⅱ对,有
A、A B、B C、C D、D -
5、化学实验操作有严格的规范,下列实验操作描述错误的是( )A、实验剩余的钠块可以放回原瓶 B、进行焰色试验前,将铂丝用硫酸清洗 C、向试管中滴加试剂时,滴管下端不能接触试管内壁 D、制备氢氧化铁胶体实验时,不宜用玻璃棒搅拌,也不宜使液体沸腾时间过长
-
6、生活因化学更美好。下列对化学物质在生活中的用途的知识解读正确的是( )
选项
生活中的用途
知识解读
A
自来水厂用氯气消毒
氯气有毒,能杀死病毒和细菌
B
用石灰石处理酸性废水
石灰石属于强碱,具有碱性
C
面包师用小苏打作发泡剂烘焙面包
小苏打不稳定、受热易分解
D
碳酸氢钠加入的量过多会使蒸出的馒头发黄
碳酸氢钠是淡黄色固体
A、A B、B C、C D、D -
7、某离子反应涉及H2O、、、H+、、Cr3+六种微粒,已知反应过程中数目变化如图所示,下列说法不正确的是( )
 A、中Cr化合价是+6价 B、反应的氧化产物是 C、反应中消耗的氧化剂与转移电子的数目比为1:6 D、随着反应的进行,溶液中的数目增大
A、中Cr化合价是+6价 B、反应的氧化产物是 C、反应中消耗的氧化剂与转移电子的数目比为1:6 D、随着反应的进行,溶液中的数目增大 -
8、下列反应的离子方程式书写正确的是( )A、钠与水反应: B、过氧化钠与水反应: C、氯化铝与氨水反应: D、醋酸与反应:
-
9、图中相连物质间在一定条件下可以发生反应,下表提供的四组物质符合要求的是( )

选项
甲
乙
丙
丁
A
H2
O2
CO2
CuO
B
Mg
HCl
CuCl2
NaOH
C
Ca(OH)2
CO2
NaOH
CuSO4
D
Na2CO3
BaCl2
HCl
Ca(OH)2
A、A B、B C、C D、D -
10、下列各组离子,在无色溶液中可大量共存的是( )A、、、、 B、、、、 C、、、、 D、、、、
-
11、我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3×10-9m)恢复了磁性。“钴酞菁”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列说法中正确的是( )A、其分子直径比氯离子小 B、在水中形成的分散系属于悬浊液 C、在水中形成的分散系具有丁达尔效应 D、“钴酞菁”分子不能透过滤纸
-
12、下列物质的分类正确的是( )
选项
碱
酸
盐
碱性氧化物
酸性氧化物
A
Na2CO3
H2SO4
KClO3
Na2O
SO3
B
Ca(OH)2
NaHSO4
CaCO3
CuO
CO2
C
KOH
H2S
NaHCO3
CaO
SO2
D
NaOH
HNO3
CuCl2
Fe2O3
CO
A、A B、B C、C D、D -
13、化学与生产、生活及环境密切相关,下列说法错误的是( )A、新冠病毒直径约为80~100nm,扩散到空气中可形成气溶胶 B、“青蒿一握,以水二升渍,绞取汁,尽服之”,推测青蒿素高温下可能不稳定 C、用自来水(用漂白粉消毒)配制溶液,溶液不会变质 D、超轻多孔材料“碳海绵”可用于吸收海上泄漏的原油,该过程是物理变化
-
14、疟疾是由按蚊叮咬人体后而感染的一种血液寄生虫病,患者可口服青蒿素类复方制剂进行治疗,他非诺喹是一种抗疟疾新药。其中间体合成路线如下(部分条件已省略):
 (1)、A→B反应的化学方程式为。(2)、D中所含官能团的名称为。(3)、G→H反应的类型为( )。A、加成反应 B、消去反应 C、还原反应 D、氧化反应(4)、J的结构简式为。(5)、X是D的同分异构体,请写出一种符合下列条件的X的结构简式:。
(1)、A→B反应的化学方程式为。(2)、D中所含官能团的名称为。(3)、G→H反应的类型为( )。A、加成反应 B、消去反应 C、还原反应 D、氧化反应(4)、J的结构简式为。(5)、X是D的同分异构体,请写出一种符合下列条件的X的结构简式:。i.能发生水解和银镜反应ii.X的核磁共振氢谱中3组吸收峰,且峰面积比为1∶3∶6
(6)、已知: , 以环己醇
, 以环己醇 和不多于3个碳的物质为原料,试参考中间体的合成路线制备
和不多于3个碳的物质为原料,试参考中间体的合成路线制备 , 写出合成路线。 (7)、从C60、C70的混合物中纯化C60的过程如图,杯酚和C60之间通过( )形成超分子。A、金属键 B、范德华力 C、氢键 D、离子键
, 写出合成路线。 (7)、从C60、C70的混合物中纯化C60的过程如图,杯酚和C60之间通过( )形成超分子。A、金属键 B、范德华力 C、氢键 D、离子键
-
15、采用氨浸法处理含锌物料回收有价金属,具有原料适应性广、工艺流程短、净化负担轻、环境污染小、产品品种多、投资少等特点,对推动湿法炼锌技术的进步具有深远的意义。
【不定项】控制温度不变,向10mL0.1mo/LHX溶液中逐滴加入0.1mol/L的氨水,其导电能力、pH与所加氨水体积V的关系变化如图所示,下列说法不正确的是( )。
 A、水的电离程度:b>d,a>c B、Kb(NH3·H2O)=Ka(HX)=10-4.6 C、d点所得溶液的pH<7 D、a点对应的溶液中存在:[HX]+2[H+]=[X—]+[NH3·H2O]+2[OH-]
A、水的电离程度:b>d,a>c B、Kb(NH3·H2O)=Ka(HX)=10-4.6 C、d点所得溶液的pH<7 D、a点对应的溶液中存在:[HX]+2[H+]=[X—]+[NH3·H2O]+2[OH-] -
16、经员工检测发现仓库中CuSO4·5H2O晶体原材料存在被污染的情况(纯度大于90%则可以继续使用),因而安排了下列方法进行其纯度的测定:
①取0.500g晶体样品,加入足量KI溶液
发生反应:2Cu2++4I-=2CuI↓+I2
②用0.1000mol/L的Na2S2O3标准溶液进行滴定
发生反应:I2+2S2O32-=2I-+S4O62-
③以淀粉为指示剂,到达滴定终点时消耗标准溶液15.00mL。
(1)、试通过计算,判断该批原材料是否能够继续使用(写出计算过程)。(2)、已知CuI能够吸附大量I2 , 若不对其进行适当的处理,则会导致测得纯度的结果 (填“偏大”、“偏小”或“无影响”)。 -
17、锌一般能够起到促进食欲、促进生长发育等作用,属于人体不可缺少的微量元素。除了人体内,在电镀、合金、电池领域都能找到Zn元素的身影。“湿法炼锌”是现代炼锌的主要方法,下列是以硫化锌精矿制备单质锌的工业流程:
 (1)、ZnS精矿在空气中焙烧时,通常会将硫化锌精矿粉碎,其目的是。(2)、已知电解时Cl-会腐蚀阳极板,因此实际生产会同时加入Cu和CuSO4从而生成CuCl沉淀以降低对电解的影响,原理为:2Cl-(aq)+Cu(s)+Cu2+(aq)=2CuCl(s) ΔH<0,实验测得电解液pH对溶液中c(Cl-)的影响如图所示,下列说法正确的是( )。
(1)、ZnS精矿在空气中焙烧时,通常会将硫化锌精矿粉碎,其目的是。(2)、已知电解时Cl-会腐蚀阳极板,因此实际生产会同时加入Cu和CuSO4从而生成CuCl沉淀以降低对电解的影响,原理为:2Cl-(aq)+Cu(s)+Cu2+(aq)=2CuCl(s) ΔH<0,实验测得电解液pH对溶液中c(Cl-)的影响如图所示,下列说法正确的是( )。 A、加入适当过量的Cu,平衡正向移动 B、Ksp-CuCl的表达式为Ksp=c(Cu2+)c(Cl-) C、向电解液中加入稀硫酸,不利于Cl-的去除 D、若加入1molCu单质,则完全反应后转移的电子总数为NA(3)、在进行上述操作时,工厂对多余的铜粉进行了回收,为检验其表面的Cl—是否已经洗净,写出具体的实验步骤、现象和结论:。
A、加入适当过量的Cu,平衡正向移动 B、Ksp-CuCl的表达式为Ksp=c(Cu2+)c(Cl-) C、向电解液中加入稀硫酸,不利于Cl-的去除 D、若加入1molCu单质,则完全反应后转移的电子总数为NA(3)、在进行上述操作时,工厂对多余的铜粉进行了回收,为检验其表面的Cl—是否已经洗净,写出具体的实验步骤、现象和结论:。 -
18、【不定项】某工厂进行了另外的实验,向某密闭容器中按n(H2):n(CO)=2:1的比例投入反应物,测量了15min后H2在四种不同温度下的转化率如下表所示,且T1<T2<T3<T4 , 则下列说法正确的是( )。
温度
T1
T2
T3
T4
转化率
10%
70%
70%
60%
A、该反应ΔH>0 B、T温度时(T2<T<T3),相同时间内H2的转化率为70% C、T3温度下,若反应在15min后继续进行,则H2的转化率会增大 D、T4温度下,若15min后,[CO]=0.5mol/L,则T4时的K=1.5 -
19、甲醇是一种清洁能源,在交通、化工等领域应用广泛,具有广阔的研究前景。工业上使用水煤气(CO与H2的混合气体)转化成甲醇,反应为2H2(g)+CO(g)=CH3OH(g)。
 (1)、CO的平衡转化率与温度、压强的关系如右图所示:
(1)、CO的平衡转化率与温度、压强的关系如右图所示:p1、p2的大小关系是p1p2(填“>”、“<”或“=”)
A、B、C三点的平衡常数的大小关系是。(用“KA”、“KB”、“KC”表示)
(2)、【多选】能说明恒容容器中上述反应达到化学平衡状态的是( )。A、v正(H2)=2v逆(CH3OH) B、容器内的压强不再改变 C、混合气体的平均摩尔质量不再改变 D、容器中氧元素的质量分数不再改变(3)、该反应平衡常数的表达式为。 -
20、作为实现碳中和目标的重要技术路径的CCUS,其中CO2资源化、高值化利用近年来受到高度关注。其中,CO2合成CH3OH是市场潜力最大、关注度最高的碳利用途径之一。下列化学概念与实验事实关联匹配错误的是( )。A、取代基的吸电子能力——酸性:CH3CH2CH2COOH<CH3CH2CHClCOOH B、分子的极性——CH3OH中正负电荷重心不重合,是极性分子 C、分子之间作用力——NaCl熔点较高 D、分子间氢键——CH3CH2CH2NH2的沸点比
 高
高