相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、在一定温度下,对冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题:
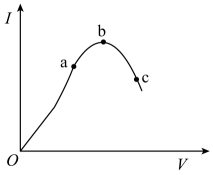 (1)、在一定温度下,向上述醋酸溶液中,加入加水稀释,按要求填空。
(1)、在一定温度下,向上述醋酸溶液中,加入加水稀释,按要求填空。①电离平衡将(填“向电离方向”、“向生成醋酸分子方向”或“不”)移动;
②醋酸的平衡常数Ka将(填“增大”、“减小”或“不变”)
(2)、a、b、c三点对应的溶液中,c(H+)最小为。(3)、a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是。(4)、若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是____(填字母,下同)。A、加热 B、加入NaOH稀溶液 C、加入K2CO3固体 D、加水(5)、部分弱酸的电离平衡常数如下表:弱酸
电离平衡常数
(25℃)
①依据表格中三种酸的电离常数,判断三种酸酸性强弱的顺序为。
②向NaCN溶液中通入CO2气体,反应的化学方程式为。
-
2、探究化学反应的快慢和限度具有十分重要的意义。(1)、Ⅰ.某实验小组欲通过用酸性和(草酸)反应测定单位时间内生成的体积,探究影响反应速率的因素。设计的实验方案如下(溶液已酸化),实验装置如图甲所示:

完成上述反应的离子方程式为: , 该实验是探究对反应速率的影响。实验序号
A溶液
B溶液
①
20 mL 0.01 mol·L 溶液
30 mL 0.01 mol·L 溶液
②
20 mL 0.01 mol·L 溶液
30 mL 0.01 mol·L 溶液
(2)、若实验①在2 min末收集了4.48 mL (标准状况下,则在2 min末mol/L(假设混合溶液的体积为50 mL,反应前后体积变化忽略不计)。(3)、小组同学发现反应速率变化如图乙,其中时间内速率变快的主要原因可能是①生成的可作为反应的催化剂;②。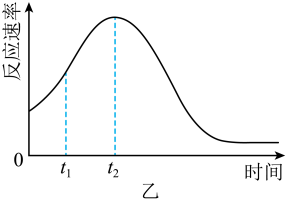 (4)、Ⅱ.溶液中存在平衡:(橙色)(黄色)。该溶液具有强氧化性。其还原产物在水溶液中呈绿色或蓝绿色。用溶液进行下列实验:
(4)、Ⅱ.溶液中存在平衡:(橙色)(黄色)。该溶液具有强氧化性。其还原产物在水溶液中呈绿色或蓝绿色。用溶液进行下列实验:
向溶液中加入30%NaOH溶液。溶液呈色:向溶液中逐滴加入溶液(已知为黄色沉淀),则平衡向着方向移动,溶液颜色变化为。 -
3、一碳化学是以分子中只含一个碳原子的化合物为原料生产化工产品的方法。合成气(和的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
I:
II:
III:
(1)、当反应I达到平衡后,下列措施可提高正反应速率的是____(填标号)。A、加入焦炭 B、通入CO C、升高温度 D、分离出氢气(2)、若在恒温恒容容器中仅发生反应II,则下列能说明反应达到平衡状态的是____。A、容器内气体的压强不变 B、容器内气体的总质量不变 C、容器内气体的平均相对分子质量不变 D、单位时间内,每有2 mol 键断裂,同时有1 mol 键断裂(3)、向容积为的密闭容器中加入活性炭(足量)和 , 发生反应 , 和的物质的量变化如下表所示。条件
保持温度为/℃
时间
0
5min
10min
15min
20min
25min
30min
物质的量
2.0
1.4
1.0
0.70
0.50
0.40
0.40
物质的量
0
0.3
0.50
0.65
0.75
0.80
0.80
①内,以表示的该反应速率 , 最终达平衡时的转化率 , 该温度℃下的平衡常数。
②保持温度℃不变,向该密闭容器中加入该四种反应混合物各 , 该时刻,正、逆反应速率的大小关系为:(填“>”“<”或“=”)。
(4)、已知4CO(g) +2NO2(g)4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在(填“高温”、“低温”或“任何温度”)下能自发进行。 -
4、生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:(1)、冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用(填“放热”或“吸热”)的化学变化或物理变化。(2)、“即热饭盒”给人们生活带来方便,它可利用下面____(填字母)反应释放的热量加热食物。A、生石灰和水 B、浓硫酸和水 C、纯碱和水 D、食盐和白醋(3)、研究含碳、氮的物质间转化的热效应,在日常生活与工业生产中均有很重要的意义。(1)已知:H2O(l)= H2O(g) △H= +44.0kJ·mol-1 , 甲烷完全燃烧与不完全燃烧的热效应如下图所示。

①写出表示甲烷燃烧热的热化学方程式:。
②CO的燃烧热△H=kJ·mol-1。
(4)、以NH3、CO2为原料生产尿素[CONH2)2]的反应历程与能量变化示意图如下。
①第一步反应的热化学方程式为。
②第二步反应的△H0(填“>”、“<”或“=”)。
③从图象分析决定生产尿素的总反应的反应速率的步骤是第步反应。
-
5、已知25℃时,关于0.1mol/L醋酸溶液 , 下列说法正确的是( )A、升高温度,醋酸的电离程度增大,增大 B、向该溶液中通入HCl气体,平衡逆向移动,减小 C、该温度下1mol/L的醋酸溶液 D、加水稀释后,溶液中增大
-
6、关于合成氨反应 , 下列说法不正确的是( )A、使用高效催化剂能减小反应活化能 B、为了提高原料利用率,和循环使用 C、工业合成氨温度为700K是因为升高温度有利于提高的平衡转化率 D、恒温恒容下,若体系的总压强不再改变,说明该反应已达平衡状态
-
7、对反应A+3B⇌2C来说,下列反应速率中最快的是( )A、υ(B)=0.9 mol/(L•min) B、υ(B)=0.6 mol/(L•min) C、υ(C)=0.5 mol/(L•min) D、υ(A)=0.5 mol/(L•min)
-
8、利用如图所示装置可以将温室气体CO2转化为燃料气体CO,下列说法正确的是( )
 A、该过程中包括太阳能、化学能、电能间的转化 B、电极a上发生还原反应 C、该装置工作时,H+从b极区向a极区移动 D、该装置中每生成1molCO,同时生成1molO2
A、该过程中包括太阳能、化学能、电能间的转化 B、电极a上发生还原反应 C、该装置工作时,H+从b极区向a极区移动 D、该装置中每生成1molCO,同时生成1molO2 -
9、将浓度为0.05mol/L的HClO的溶液加水不断稀释,下列各量始终保持增大的是( )A、 B、c(HClO) C、 D、
-
10、对于反应N2O4(g)2NO2(g)ΔH>0,要使该反应的平衡常数值增大,可以采取的措施有( )A、增大N2O4的浓度 B、增大NO2的浓度 C、升高体系的温度 D、减小压强
-
11、反应A+B―→C(ΔH<0)分两步进行:①A+B―→X(ΔH>0),②X―→C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )A、
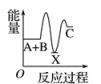 B、
B、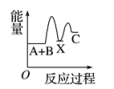 C、
C、 D、
D、
-
12、用NA表示阿伏加德罗常数的值,下列说法正确的是( )A、0.2mol/LNa2SO4溶液中含有Na⁺和总物质的量为0.6mol B、标准状况下,22.4L乙醇所含分子数为NA C、65gZn与足量H2SO4完全反应生成的H2所含原子数目为2NA D、11.2L氢气在足量的O2中完全燃烧,生成的水分子数为0.5NA
-
13、对于反应2SO2(g)+O2(g)2SO3(g),下列说法正确的是( )A、反应的ΔS>0 B、反应的平衡常数可表示为K= C、增大体系的压强能提高SO2的反应速率和转化率 D、使用催化剂能改变反应路径,提高反应的活化能
-
14、已知反应: 。图中a、b曲线表示在一定条件下,D的体积分数随时间的变化情况。若使曲线a变为曲线b,可采取的措施是( )
 A、增大反应容器的体积 B、减小B的浓度 C、升高温度 D、缩小反应容器的体积
A、增大反应容器的体积 B、减小B的浓度 C、升高温度 D、缩小反应容器的体积 -
15、下列热化学方程式书写正确的是( )A、2SO2+O2 2SO3 ΔH=-196.6 kJ·mol-1 B、H2(g)+O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1 C、2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ D、C(s)+O2(g)=CO2(g) ΔH=+393.5 kJ·mol-1
-
16、我国在探索太空、开发深海、建设高铁、5G技术等方面取得举世瞩目的成就,这些成就与化学有着密切联系。下列说法正确的是( )A、航天服壳体使用的铝合金材料熔点比纯铝高 B、打印机墨粉中常加有Fe3O4 , 这是利用了其颜色和磁性特点,可用CuO替代Fe3O4 C、华为5G手机芯片的主要成分是二氧化硅 D、中国天眼FAST用到的高性能碳化硅是一种新型的无机非金属材料
-
17、实验室需要溶液和硫酸溶液。根据这两种溶液的配制情况回答下列问题:(1)、如下图所示的仪器中,配制溶液肯定不需要的是(填序号),配制上述溶液还需用到的玻璃仪器有(填仪器名称)。
A.
 B.
B. C.
C. D.
D. (2)、配制溶液时,其正确的操作顺序是(字母表示,每个字母只能用一次)。
(2)、配制溶液时,其正确的操作顺序是(字母表示,每个字母只能用一次)。A.将容量瓶盖紧,颠倒摇匀
B.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
C.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
D.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
E.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
F.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
(3)、配制溶液时,在实验中其他操作均正确,若定容时仰视容量瓶刻度线,则所配溶液浓度(填“偏高”、“偏低”或“无影响”)。(4)、配制硫酸溶液480mL时,所需量取质量分数为98%、密度为的浓硫酸的体积为mL(保留1位小数)。(5)、配制硫酸溶液时,在实验中其他操作均正确,若用量筒量取浓硫酸时仰视刻度线,则所配溶液浓度。(填“偏大”、“偏小”或“无影响”)(6)、配制溶液时,所需称取的质量g。 -
18、氯气、“84”消毒液、漂白粉等都是含氯的消毒剂,某化学兴趣小组利用如图装置制备“84”消毒液、漂白粉,并收集纯净干燥的氯气。回答下列问题:
 (1)、盛装浓盐酸的仪器的名称为 , 装置甲中发生反应的化学方程式为。(2)、装置丁用来收集纯净且干燥的氯气,进气口为(填a或b);装置乙盛装的试剂是。(填名称)(3)、将氯气通入装置己中制备“84”漂白液,则装置己中发生反应的化学方程式为 , 有同学认为装置己还有一个作用,该作用为。(4)、装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为。
(1)、盛装浓盐酸的仪器的名称为 , 装置甲中发生反应的化学方程式为。(2)、装置丁用来收集纯净且干燥的氯气,进气口为(填a或b);装置乙盛装的试剂是。(填名称)(3)、将氯气通入装置己中制备“84”漂白液,则装置己中发生反应的化学方程式为 , 有同学认为装置己还有一个作用,该作用为。(4)、装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为。 -
19、请回答下列相关问题。(1)、现有以下物质:①熔融的;②Cu;③;④70%的乙醇;⑤;⑥稀硫酸。以上物质中属于混合物的是(填序号,下同),属于电解质的是 , 属于氧化物的是 , 能导电的是。(2)、请写出下列物质在水溶液中的电离方程式。
①; ②。
(3)、钙及其化合物之间的转化关系如下图所示:
上述反应中,属于化合反应的是(填序号,下同),属于复分解反应的是。
-
20、根据所学知识,回答下列问题:(1)、Ⅰ.硫酸是一种重要的工业原料。
稀硫酸具有酸性,稀硫酸溶液中,mol。(2)、稀硫酸与铝恰好完全反应,所得溶液中含有 , 则该溶液中物质的量浓度为。(3)、Ⅱ.回答下列问题:
在同温同压下,和两种气体,密度比为 , 若两者质量相等,其体积比为。(4)、中,核外电子总数比质子总数多 , 则R的摩尔质量为。(5)、实验室利用反应制取氧气,现有参加反应,计算得到标准状况下的氧气的体积是L。(6)、某元素G的一种含氧酸化学式为 , 属于二元酸,则与过量氢氧化钠溶液反应生成的产物为((填“酸式盐”或“正盐”)。(7)、某密闭容器,中间有一可自由滑动的隔板(厚度忽略不计)将容器分成两部分,装置如图所示(左、右两侧温度相同)。左边充入氦气,右边充入和的混合气体,原子总数为共 , 则左右两室体积比为。