相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、氯元素的化合价与部分物质类别的对应关系如图所示,据图判断下列说法错误的是( )。
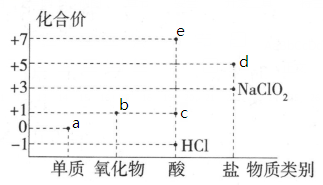 A、c在光照条件下很容易分解 B、b不是酸性氧化物,因为它没有对应的含氧酸 C、图中a、b、c、d、e五种物质中均含有共价键,且c、d、e属于电解质 D、将a通入溶液中,已知生成、和d的混合物,若与之比为 , 则氧化剂与还原剂的物质的量之比为
A、c在光照条件下很容易分解 B、b不是酸性氧化物,因为它没有对应的含氧酸 C、图中a、b、c、d、e五种物质中均含有共价键,且c、d、e属于电解质 D、将a通入溶液中,已知生成、和d的混合物,若与之比为 , 则氧化剂与还原剂的物质的量之比为 -
2、下列实验方案能达到实验目的(或所得结论正确)的是( )。A、用玻璃棒蘸取溶液点在pH试纸上测溶液的pH B、用湿润的淀粉KI试纸区分溴蒸气与二氧化氮气体 C、向溶液中通入 , 验证非金属性:C>Si D、向某溶液中滴入溶液并加热,产生使湿润红色石蕊试纸变蓝的气体,则该溶液一定是铵盐溶液
-
3、下列有关化学用语正确的是( )。A、聚丙烯的结构简式: B、核外有a个电子、b个中子,M的原子符号: C、的电子式: D、乙酸的结构式:
-
4、明·宋应星《天工开物》中记载:“凡海滨石山傍水处,咸浪积压.生出蛎房,闽中曰蚝房。……凡燔蛎灰者,执椎与凿,濡足取来,……叠煤架火燔成,与前石灰共法。粘砌城墙、桥梁,调和桐油造舟,功皆相同。”下列有关描述中正确的是( )。A、“蛎房”的主要成分是氧化钙 B、古人用“蚝房”煅烧制成的石灰可用作建筑材料 C、“桐油”是一种优良的植物油,从物质分类角度来看属于纯净物 D、“蚝房”受热分解的反应属于放热的非氧化还原反应
-
5、实验室有浓盐酸的质量分数为 , 密度为(1)、需要配制的盐酸,配制时需用量筒量取以上浓盐酸的体积为;(2)、用浓盐酸配制稀盐酸,操作步骤的正确顺序是(填序号)
a、计算需要浓盐酸的体积
b、用量筒量取浓盐酸:
c、将烧杯中的溶液转移入仪器A中,并用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也转移入仪器A中;
d、把量好体积的浓盐酸倒入烧杯中,加适量蒸馏水稀释,冷却;
e、盖好瓶塞,反复上下颠倒,摇匀;
f、继续向仪器A中加蒸馏水至距离刻度线处,改用仪器B,小心滴加蒸馏水至。
(3)、填写实验中用到的仪器名称:A、B。(4)、在配制过程中,玻璃棒所起的作用。(5)、仪器A使用前,需进行的实验操作为。(6)、请将上述操作f中的空白处补充完整。(7)、下列操作使溶液物质的量浓度偏高的是:____。A、没有将洗涤液转移到仪器A中 B、仪器A洗净后未经干燥处理 C、转移过程中有少量溶液溅出 D、未冷却至室温就转移定容 E、定容时俯视刻度线 F、量取盐酸时仰视 -
6、(1)、I.离子反应是中学化学中重要的反应类型;离子方程式是用来表示离子反应的化学用语。
回答下列问题:
在发生离子反应的反应物或生成物中,一定存在____(填标号)。A、单质 B、化合物 C、水 D、电解质(2)、从下列物质中选择合适反应物,按①③的要求,各写出一个符合条件的离子方程式。、、、、、、、、
①写出一个有气体生成的置换反应的离子反应方程式:。
②有难溶性碱生成的离子反应方程式:。
(3)、某兴趣小组的同学向一定体积的溶液中逐滴加入的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是____。 A、XY段混合溶液的导电能力逐渐减弱,说明生成的白色沉淀BaSO,不是电解质 B、a时刻,两溶液恰好完全反应 C、YZ段的导电能力不断增大,主要是由于溶液电离出的离子导电 D、向一定体积的溶液中逐滴加入稀盐酸,测得溶液的导电能力-时间曲线图与该图保持一致(4)、属于酸;为盐(填序号)
A、XY段混合溶液的导电能力逐渐减弱,说明生成的白色沉淀BaSO,不是电解质 B、a时刻,两溶液恰好完全反应 C、YZ段的导电能力不断增大,主要是由于溶液电离出的离子导电 D、向一定体积的溶液中逐滴加入稀盐酸,测得溶液的导电能力-时间曲线图与该图保持一致(4)、属于酸;为盐(填序号)①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(5)、写出溶液与足量溶液反应的离子方程式。 -
7、(1)、I.生活中化学无处不在,家庭厨卫用品中有许多中学化学常见的物质。下表为部分厨卫用品名称及其主要成分表。回答下列问题:
若不慎将食盐洒在天然气灶的火焰上,观察到的现象是。名称 食盐 碱面 发酵粉 洁厕灵 “84”消毒液 主要成分 (2)、除去碳酸钠固体中含有少量碳酸氢钠的方法是 , 发生反应的化学方程式为。(3)、碳酸氢钠可以作为治疗胃酸(主要成分为盐酸)过多的药物的主要成分,其反应原理的离子方程式为。(4)、“84”消毒液不能与洁厕灵混合使用,否则可能会产生有毒气体单质,该气体单质是(填名称)。(5)、Ⅱ.亚硝酸钠()是肉制品生产中最常使用的一种食品添加剂。
某兴趣小组研究亚硝酸钠时,查阅资料得到以下信息:ⅰ.亚硝酸钠的水溶液呈碱性;
ⅱ.亚硝酸钠是一种强氧化剂,进入血液后与血红蛋白结合,导致组织缺氧,使人体出现青紫并中毒;
ⅱ.亚硝酸钠的外观与食盐极为相似,容易被误用而引起中毒。
回答下列问题:
①已知能与HI发生如下化学反应: , 该反应的还原剂是(填化学式),请用双线桥表示该反应电子转移的方向和数目。
②下列方法中可用来区分和的是(填标号)。
A.观察外形
B.在酸性条件下加入淀粉碘化钾溶液观察溶液变化
C.向两物质的水溶液中滴加酚酞溶液观察溶液颜色变化
-
8、(1)、I.铁是人体含量最多的微量元素,这些铁在人体中不是以金属单质的形式存在,而是以和的形式存在。亚铁离子易被吸收,所以给贫血者补充铁时,应该给予含亚铁离子的亚铁盐,如硫酸亚铁。
某同学预测:肯定既有还原性又有氧化性。你认为他预测的依据是;当人体中的被转化为而失去与结合的能力,可服用维生素C来缓解这种状况,这说明维生素C具有性。(2)、在的反应中,还原产物为 , 每有参加反应,被还原的为 , 转移电子数个(设表示阿伏加德罗常数的值)。(3)、Ⅱ.高铁酸钾()是一种易溶于水、高效的多功能水处理剂。工业上通常先制得高铁酸钠,然后在一定温度下,向高铁酸钠溶液中加入至饱和,从而使高铁酸钾析出。
高铁酸钾中铁元素的化合价为。(4)、高铁酸钾与水反应生成、(胶体)和。该反应的离子方程式为。 -
9、某离子反应涉及六种微粒,已知反应过程中浓度变化如图所示,下列说法不正确的是( )
 A、中化合价是价 B、反应的氧化产物是 C、反应中消耗的氧化剂与转移电子的数目比为 D、随着反应的进行,溶液中的H浓度增大
A、中化合价是价 B、反应的氧化产物是 C、反应中消耗的氧化剂与转移电子的数目比为 D、随着反应的进行,溶液中的H浓度增大 -
10、在指定溶液中,下列离子能大量共存的是( )A、透明的溶液中: B、使无色酚酞试液呈红色的溶液中: C、含有大量的溶液中: D、使紫色石蕊试液呈红色的溶液中:
-
11、在中加入溶有的稀盐酸,完全溶解。代表阿伏加德罗常数的值,下列说法正确的是( )A、反应后溶液中的溶质只有 B、该稀盐酸中数为 C、中原子个数为 D、反应生成标准状况下气体
-
12、设表示阿伏加德罗常数的值,下列叙述中正确的是( )A、所含有的原子数为 B、常温常压下,含有的钠离子数目为 C、标准状况下,所含的分子数为 D、物质的量浓度为的溶液中,含有氯离子的物质的量为
-
13、如图所示,两个集气瓶的容积相等,在同温、同压时瓶内气体的关系一定正确的是( )
 A、所含原子数相等 B、密度相等 C、气体质量相等 D、摩尔质量相等
A、所含原子数相等 B、密度相等 C、气体质量相等 D、摩尔质量相等 -
14、应用下列装置能达到实验目的的是( )
选项
A
B
C
D
装置




目的
灼烧固体制取
可用于制备并检验氢气的可燃性
除去中的并干燥
从溶液中分离出晶体
A、A B、B C、C D、D -
15、下列叙述错误的是( )A、钠着火时可以用沙子盖灭,少量的钠应保存在煤油中 B、将一小块钠投入溶液中可置换出红色的固体 C、反应中,水既不作氧化剂也不作还原剂 D、与中阳、阴离子的个数比均为
-
16、如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液面左边低于右边,恢复到原温度后液面左边与右边基本相平,则烧杯内的物质是( )
 A、过氧化钠 B、氧化钠 C、钠 D、氯化钠
A、过氧化钠 B、氧化钠 C、钠 D、氯化钠 -
17、下列指定反应的离子方程式正确的是( )A、将稀硫酸滴在铜片上: B、钠与水反应: C、利用溶液腐蚀的方法制作印刷线路板: D、用醋酸除去水垢:
-
18、下列说法中正确的有( )A、溶于水后能电离出氢离子的化合物一定是酸 B、强氧化剂与强还原剂混合一定发生氧化还原反应 C、两种盐反应一定生成两种新盐 D、某元素由化合态变为游离态,则它可能被还原也可能被氧化
-
19、下列有关溶液、胶体和浊液的说法中,正确的是( )A、用过滤的方法可以除去胶体中的 B、胶体和浊液中粒子的大小相同 C、向氧氧化铁胶体中继续滴加溶液,可看到红褐色沉淀 D、将饱和溶液中滴入浓溶液中,制备胶体
-
20、中国传统文化富载化学知识,下列有关说法正确的是( )A、“日照香炉生紫烟”涉及的原理为钾的焰色试验 B、“朱颜绿发照青铜”青铜指的是铜緑 C、石钟乳():“色黄,以苦酒(醋)洗刷则白”是物理变化 D、《元日》“爆竹声中一岁除,春风送暖入屠苏”句中涉及氧化还原反应