相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列实验装置或操作不能达到相应实验目的的是( )
 A、用图甲装置制备晶体 B、用图乙装置制备并检验气体 C、用图丙装置验证铁钉的吸氧腐蚀 D、用图丁装置合成氨并检验氨的生成
A、用图甲装置制备晶体 B、用图乙装置制备并检验气体 C、用图丙装置验证铁钉的吸氧腐蚀 D、用图丁装置合成氨并检验氨的生成 -
2、常温下,下列各组离子在指定溶液中一定能大量共存的是( )A、饱和氯水中:、、、 B、在的氯化铁溶液中:、、、 C、加入铝粉能放出的溶液中:、、、 D、加入产生气泡的溶液中:、、、
-
3、用表示阿伏加德罗常数的值,下列说法正确的是( )A、溶于水形成的氨水中质子数约为 B、完全水解生成的胶体粒子数目为 C、高温下,铁粉与水蒸气反应,固体的质量增加 , 则转移电子数目为 D、质量分数为46%的乙醇水溶液中所含氢原子数为
-
4、下列过程不涉及氧化还原反应的是( )A、雷雨过程中有少量硝酸生成 B、工业制取漂白粉 C、高铁酸盐处理水 D、用石灰石粉末修复被酸雨侵蚀的土壤
-
5、2023年10月8日第19届亚运会在杭州圆满闭幕,本届亚运会秉持“绿色、智能、节俭、文明”的办会理念。下列说法正确的是( )A、零碳甲醇作为本届亚运会的火炬燃料,甲醇燃烧属于吸热反应 B、吉祥物“江南忆”机器人所采用芯片的主要成分为硅单质 C、亚运会纪念章“琮琮”是由锌合金镀金制成的,锌合金镀金属于合成材料 D、场馆全部使用绿色能源,打造首届碳中和亚运会,碳中和就是不排放二氧化碳
-
6、奥美拉唑是一种抑酸药,适用于治疗胃溃疡、十二指肠溃疡等上消化道疾病,其合成路线如图。

已知:
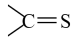 的某些性质与
的某些性质与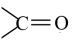 相似,都能与发生加成反应。
相似,都能与发生加成反应。回答下列问题:
(1)、A分子所含官能团的名称是。(2)、的反应条件是。(3)、的反应方程式是。(4)、的反应类型是。(5)、W是E的同分异构体,满足下列条件的W有种,写出任意一种的结构简式:。①苯环上只有三个取代基且不存在
②遇溶液显色
(6)、E经过三步形成F,请写出中间2的结构简式:。
-
7、推动的综合利用、实现碳中和是党中央作出的重大战略决策。(1)、科学家利用电化学装置实现和两种分子的耦合转化,其原理如图所示:

①电极B上生成的电极反应式为。
②若生成的乙烯和乙烷的体积比为 , 则消耗的和体积比为。
(2)、一定条件可转化为 ,①下列有关该反应的说法正确的是。
A.升高温度逆反应速率加快,正反应速率减慢
B.反应体系中的质量不再变化,说明反应达到平衡状态
C.恒温恒容下达到平衡后,再通入 , 平衡向正反应方向移动
D.平衡时,若压缩体积,则、均变大
②恒压下,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,分子筛膜能选择性分离出。P点甲醇产率高于T点的原因为。
 (3)、与丙烯催化合成甲基丙烯酸。催化剂在温度不同时对转化率的影响如图所示,时转化率低于和的原因可能为。
(3)、与丙烯催化合成甲基丙烯酸。催化剂在温度不同时对转化率的影响如图所示,时转化率低于和的原因可能为。
-
8、蛇纹石矿的主要成分为、、、、、等,现有一种利用该矿石制备高纯度工艺流程如图:


已知: , 氢硫酸的两步电离常数分别为 , 。
(1)、提高“加压酸浸”速率的措施有(填一项合理措施即可)。(2)、滤渣1的主要成分除S、外,还有。(3)、“氧化”时往装置鼓入空气,可作氧化剂,发生反应的离子方程式为。(4)、沉镍时,当镍离子恰好沉淀完全(离子浓度小于 , 可认为沉淀完全),要保证此时不会从溶液逸出,应控制溶液pH不小于(结果取整,已知饱和浓度约为)。(5)、晶体中阴离子采用面心立方最密堆积方式(如上图),实验测得的晶胞参数为, 则为pm,该晶体密度为(阿伏加德罗常数用表示)。
-
9、亚硝酰氯()是一种红褐色液体或黄色气体,熔点: , 沸点: , 遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室用下图装置由氯气与一氧化氮在常温常压下合成。

简要实验步骤:组装仪器,检查装置气密性良好后,先打开、 , 关闭 , 再打开装置A中分液漏斗活塞滴入适量稀硝酸,当观察到C中出现____现象时关闭、 , 之后可能观察到C中长颈漏斗中的液面上升。然后向装置G中通入纯净的 , 当瓶中充满黄绿色气体时,再打开、。回答下列问题:
(1)、根据实验原理和目的,制备亚硝酰氯的装置连接顺序为A、C、、、B。(2)、步骤划线处,装置C出现的现象是。(3)、仪器G的名称是。(4)、冰盐水的作用为。(5)、若制得的中含有少量杂质,为测定产品纯度进行如下实验:称取样品溶于溶液中,加入几滴溶液作指示剂,用足量硝酸酸化的溶液滴定至产生砖红色沉淀,消耗溶液。[已知:为砖红色沉淀, , ]①写出亚硝酰氯与溶液反应生成亚硝酸钠的离子方程式:。
②产品纯度为(保留4位有效数字)。
-
10、某温度下,改变溶液的pH时,各种含X元素粒子及浓度变化如图所示。下列有关说法正确的是( )
 A、 B、E点溶液中存在: C、 D、反应的平衡常数
A、 B、E点溶液中存在: C、 D、反应的平衡常数 -
11、一种含Pt催化剂活化甲烷中碳氢键的反应机理如图所示。下列说法错误的是( )
 A、、分别是非极性分子、极性分子 B、催化循环中S的VSEPR模型相同 C、配体
A、、分别是非极性分子、极性分子 B、催化循环中S的VSEPR模型相同 C、配体 完全加氢后产物含两个手性碳原子
D、上述过程的总反应:
完全加氢后产物含两个手性碳原子
D、上述过程的总反应:
-
12、羟基自由基()是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为和的原电池-电解池组合装置,实现了发电、环保两位一体。下列说法错误的是( )
 A、电池工作时,b极电极反应为 B、a极参与反应,理论上溶液中减少的离子为 C、右侧装置中,c、d两极产生气体的体积比(相同条件下)为 D、d极区苯酚被氧化的化学方程式为
A、电池工作时,b极电极反应为 B、a极参与反应,理论上溶液中减少的离子为 C、右侧装置中,c、d两极产生气体的体积比(相同条件下)为 D、d极区苯酚被氧化的化学方程式为 -
13、工业上利用和制备 , 相关化学键的键能如下表所示:
键
键能
745
436
462.8
413.4
351
已知:①温度为时,
②实验测得: , , 、为速率常数
下列说法错误的是( )
A、时,密闭容器充入浓度均为的、 , 反应至平衡,则体积分数为 B、反应 C、若温度为时, , 则 D、时,若向平衡后的体系中再充入、、各 , 此时 -
14、工业上用软锰矿(主要成分是 , 含有、等杂质)制备的流程如下:

已知:固体和溶液均为墨绿色,溶液呈碱性,在酸性环境中能发生歧化反应。下列说法错误的是( )
A、“熔融搬烧”过程发生了4KOH+2MnO2+O22K2MnO4+2H2O B、向“浸取液”中通入调pH后,“过滤”得滤渣Ⅰ的成分为和 C、“歧化”时的反应为: D、“操作Ⅱ”:当有大量晶体析出时,停止加热,利用余热蒸干即得紫黑色晶体 -
15、硫酰氯()是一种重要的化工试剂,常用纯净的氯气和二氧化硫合成。
已知:① ,
②常温下硫酰氯为无色液体,熔点 , 沸点 , 在潮湿空气中“发烟”。
实验室合成硫酰氯的实验装置如下图所示(部分夹持装置未画出):则下列说法错误的是( )
 A、硫酰氯在潮湿空气中“发烟”的原因是 B、装置A中发生反应的离子方程式为 C、仪器E的作用是冷凝回流,减少的挥发损失 D、F装置只起到吸收尾气的作用
A、硫酰氯在潮湿空气中“发烟”的原因是 B、装置A中发生反应的离子方程式为 C、仪器E的作用是冷凝回流,减少的挥发损失 D、F装置只起到吸收尾气的作用 -
16、由实验操作和现象,可得出相应正确结论的是( )
实验操作
现象
结论
A
向某钠盐粉末上滴加浓盐酸,将产生的气体通入品红溶液
品红溶液褪色
该钠盐只能为、或
B
向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的悬浊液
无砖红色沉淀
蔗糖未发生水解
C
铝粉与氧化铁发生铝热反应,冷却后将固体溶于盐酸,向所得溶液滴加溶液
溶液颜色无明显变化
氧化铁已经完全被铝粉还原
D
石蜡油加强热,将产生的气体通入的溶液
溶液由橙红色变为无色
气体中含不饱和烃
A、A B、B C、C D、D -
17、化合物A是一种重要的中间体,也用于医药,其结构如图所示。已知:W、X、Y、Z为四种短周期主族元素,原子序数依次增大,Z的某种单质是生命活动中不能缺少的物质,下列说法正确的是( )
 A、在A的阴离子中,键和键的比为 B、和的中心原子分别采取sp杂化、杂化 C、简单氢化物的沸点 , 主要原因是Z的氢化物相对分子质量大 D、由W、Y、Z三种元素组成的化合物的水溶液可能显酸性
A、在A的阴离子中,键和键的比为 B、和的中心原子分别采取sp杂化、杂化 C、简单氢化物的沸点 , 主要原因是Z的氢化物相对分子质量大 D、由W、Y、Z三种元素组成的化合物的水溶液可能显酸性 -
18、下列物质的转化在给定条件下不能实现的是( )A、 B、 C、 D、
-
19、下列说法正确的个数为( )
①煤的气化、液化是物理变化,煤的干馏是化学变化
②误食重金属盐会引起人体中毒,可以喝大量牛奶解毒
③“84消毒液”、的酒精都可用于消毒
④有化学键断裂的过程一定发生了化学变化
⑤钠是一种很强的还原剂,可以把锆、铌等金属从其化合物的水溶液中置换出来
⑥酸雨是pH小于7的雨水,燃煤脱硫可防治硫酸型酸雨
A、1 B、2 C、3 D、4 -
20、Sharpless教授和Meldal教授因“点击化学”“生物正交化学”研究获2022年诺贝尔化学奖。“点击化学”就是用简单的小分子与生物大分子进行合成。类似的分子结构修饰在药物设计与合成中应用广泛。布洛芬具有抗炎、镇痛、解热作用,但口服该药对胃、肠道有刺激性,结构修饰过程如图所示。下列说法错误的是( )
 A、乙的分子式为 B、乙的苯环上的二氯代物有3种(不考虑立体异构) C、甲、乙均可使酸性褪色,产物均有
A、乙的分子式为 B、乙的苯环上的二氯代物有3种(不考虑立体异构) C、甲、乙均可使酸性褪色,产物均有 D、甲分子中一定共面的碳原子有8个
D、甲分子中一定共面的碳原子有8个