相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知、、的摩尔电导率分别为0.60、1.98、0.45,据此可判断,向饱和的澄清石灰水中通入过量的 , 溶液导电能力随通入量的变化趋势正确的是( )A、
 B、
B、 C、
C、 D、
D、
-
2、在由Fe、FeO和组成的混合物中加入100mL 2的盐酸,恰好使混合物完全溶解,并放出448mL气体(标准状况),此时溶液中无 , 则下列判断正确的是( )A、混合物中3种物质反应时消耗盐酸的物质的量之比为3∶1∶3 B、反应后所得溶液中的与的物质的量浓度之比为1∶2 C、混合物中,FeO的物质的量无法确定,但比Fe的物质的量少 D、混合物中,的物质的量无法确定,但Fe比FeO的物质的量少
-
3、以太阳能为热源分解 , 经热化学铁氧化合物循环分解水制的过程如图所示。下列叙述不正确的是( )
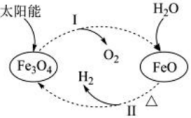 A、过程Ⅰ和过程Ⅱ都属于氧化还原反应 B、过程Ⅱ的化学方程式为 C、整个过程中和都是还原产物 D、铁氧化合物循环制具有节约能源、产物易分离等优点
A、过程Ⅰ和过程Ⅱ都属于氧化还原反应 B、过程Ⅱ的化学方程式为 C、整个过程中和都是还原产物 D、铁氧化合物循环制具有节约能源、产物易分离等优点 -
4、已知反应:①;②。下列说法正确的是( )A、反应①中,当有22.4L 参与完全反应时,有2mol电子转移 B、反应②中,HCl只做还原性 C、反应②中,氧化产物与还原产物之比为1∶1 D、根据反应①②得出,氧化性由弱到强的顺序为
-
5、如图所示是铁及其化合物的“价一类”二维图,下列有关叙述错误的是( )
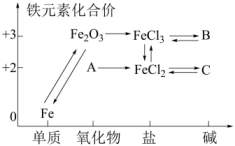 A、由图可预测:高铁酸盐()具有氧化性 B、可能是 C、的反应类型不可能是复分解反应 D、C在空气中受热转化为A
A、由图可预测:高铁酸盐()具有氧化性 B、可能是 C、的反应类型不可能是复分解反应 D、C在空气中受热转化为A -
6、下列除杂试剂和分离方法都正确的是( )
选项
物质(括号内为杂质)
除杂试剂
分离方法
A
Fe(Cu)
盐酸
过滤
B
()
NaOH溶液
过滤
C
(Fe)
水蒸气
加热
D
(HCl)
NaOH溶液
洗气
A、A B、B C、C D、D -
7、设表示阿伏加德罗常数的值,下列叙述正确的是( )A、常温常压下,11.2L氮气所含的原子数目为 B、常温常压下,28g CO中所含原子数为2 C、标准状况下,11.2L水中含有分子的数目为0.5 D、1mol 含有的电子数为11
-
8、体检时的一些指标常用物质的量浓度表示(可将元素近似折算成相应离子)。根据下图相关数据,下列分析不正确的是( )
项目名称
结果
状态单位
参考值范围
总钙 TCa
2.57
2.1~2.7
磷 P
1.51↑
0.8~1.5
镁 Mg
0.95
0.75~1.25
钾 K
仪器故障维修
3.5~5.5
钠 Na
135~160
氯 Cl
95~105
A、 B、可用焰色试验测定钾离子的含量 C、该报告中指标正常 D、若某人10mL血清样本中含钙离子1.2mg,则其钙含量略偏高 -
9、下列陈述Ⅰ和Ⅱ均正确且具有因果关系的是( )
选项
陈述Ⅰ
陈述Ⅱ
A
储氢合金可用于以为燃料的汽车
合金的熔点低,硬度大
B
纯碱能与酸反应
纯碱能与治疗胃酸过多
C
二氧化碳可以灭火
金属钠着火用二氧化碳灭火
D
过氧化钠可用作航天员的供氧剂
能与或水反应生成氧气
A、A B、B C、C D、D -
10、下列图示方法能完成相应实验的是( )
 A、用图①配制一定物质的量浓度的NaOH溶液 B、用图②制备氢气并检验其可燃性 C、用图③做焰色试验时用清洗铂丝后灼烧 D、用图④制备少量并能较长时间看到其白色
A、用图①配制一定物质的量浓度的NaOH溶液 B、用图②制备氢气并检验其可燃性 C、用图③做焰色试验时用清洗铂丝后灼烧 D、用图④制备少量并能较长时间看到其白色 -
11、下列有关0.2溶液的说法不正确的是( )A、100mL该溶液与200mL 0.1 溶液恰好完全反应 B、100mL该溶液中浓度与10mL 0.4 KCl溶液中相同 C、取出该溶液20mL,加水稀释至200mL后,得到溶液的浓度为0.02 D、100mL该溶液中的物质的量为0.02mol
-
12、水热法制备纳米颗粒Y(化合物)的反应为。下列说法中,不正确的是( )A、是还原剂 B、Y的化学式为 C、 D、每有1mol参加反应,反应转移的电子为4mol
-
13、管道工人用浓氨水检验氯气管道是否漏气,如果管道某处漏气,则会产生白烟,发生的反应为。下列叙述正确的是( )A、22.4L 的物质的量为1mol B、1mol 的质量为71g/mol C、只做还原剂 D、1mol 固体含有2mol离子
-
14、下列反应对应的离子方程式正确的是( )A、将溶液与酸性溶液混合: B、氢氧化镁与稀硫酸反应: C、向稀盐酸中加入少量铁粉: D、碳酸钡和稀硫酸:
-
15、下列叙述中正确的是( )A、中阴、阳离子的个数比为1∶1 B、为检验含有NaCl,先加入盐酸溶解,再滴入溶液,是否有白色沉淀 C、金属钠投入到溶液,能置换出红色的铜 D、相同质量的金属Na在常温和加热下与空气反应,失去的电子数一样多
-
16、将一定量潮湿通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。甲装置中所盛试剂可能是:①浓硫酸 ②NaOH溶液 ③纯碱溶液 ④饱和食盐水 ⑤溶液( )
 A、①④⑤ B、②④⑤ C、①②③⑤ D、①②③④⑤
A、①④⑤ B、②④⑤ C、①②③⑤ D、①②③④⑤ -
17、下列各组溶液中,离子间因氧化还原反应而不能大量共存的是( )A、、、、 B、、、、 C、、、、 D、、、、
-
18、中国科学技术大学的钱逸泰教授等以和金属钠为原料,在700℃时制造出1-50纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”。对此有下列一些理解,其中错误的是( )A、金刚石与石墨是同素异形体 B、这个反应是置换反应 C、是一种化合物 D、纳米级金刚石粉末属于胶体
-
19、分类是科学研究的重要方法。下列物质分类正确的是( )A、碱性氧化物:、 B、盐:、KSCN C、电解质:二氧化碳、氯气 D、碱:纯碱、一水合氨
-
20、人工合成Cn的过程可表示为:。下列叙述正确的是( )A、合成Cn的过程为化学变化 B、的中子数为165 C、Cn元素位于第七周期ⅡA族 D、与互为同位素