相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、(1)、Ⅰ.如图为相互串联的甲、乙两个电解池。
甲池若为用电解原理精炼铜的装置,B极材料是电极反应式为。电解一段时间后,电解质溶液的浓度。(填“增大”、“减小”或“不变”)。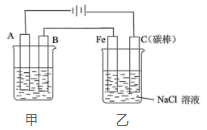 (2)、甲池若为铁制品上镀银的装置,A极材料是。(3)、乙池中发生反应的方程式为。(4)、Ⅱ.某些化学键的键能如表所示:
(2)、甲池若为铁制品上镀银的装置,A极材料是。(3)、乙池中发生反应的方程式为。(4)、Ⅱ.某些化学键的键能如表所示:化学键
H-H
N≡N
键能/(kJ/mol)
a
b
试回答下列问题:已知 ,
则N-H键的键能是kJ/mol(用含有a、b、c的式子表示)。
(5)、Ⅲ.如下图所示装置中都盛有0.1mol/L的NaCl溶液,放置一定时间后,装置中的五块相同锌片,腐蚀速率由快到慢的正确顺序是。
-
2、化学物质在汽车的动力、安全等方面有着极为重要的作用。(1)、汽油是以为主要成分的混合烃类。燃烧的化学方程式是。(2)、汽车尾气中含有NO,CO等污染物。其中NO生成过程的能量变化示意图如图。由该图形数据计算可得,该反应为(填“吸热”或“放热”)反应。

和反应生成NO(g)过程中的能量变化
(3)、通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:
①NiO电极上发生的是反应(填“氧化”或“还原”)
②外电路中,电子流动方向是从电极流向电极(填“NiO”或“Pt”)。
③Pt电极上的电极反应式为。
(4)、电动汽车普遍使用锂离子电池。某锂离子电池反应:。①放电时,Li做电池的极。
②Na也可以做电池的电极,但Li做电极更有优势。试解释原因。
(5)、安全性是汽车发展需要解决的重要问题.汽车受到强烈撞击时,预置在安全气囊内的化学药剂发生反应产生大量气体,气囊迅速弹出。某种产气药剂主要含有、、、 , 已知在猛烈撞击时分解产生两种单质,并放出大量的热。①推测的作用是。
②结合化学方程式解释的作用。
③结合上述例子,在设计气囊中所运用的化学反应时,需要考虑的角度有(填代号,可多选)。
a.反应速率 b.反应的能量变化 c.气体的量 d.气体毒性
-
3、支撑海港码头基础的钢管桩,常用电化学原理进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是( )
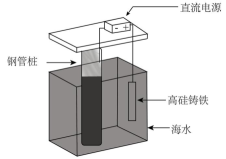 A、通入保护电流使钢管桩表面腐蚀电流接近于零 B、通电后外电路电子被强制从高硅铸铁流向钢管桩 C、此方法在化学上称之为牺牲阳极法 D、通入的保护电流应该根据环境条件变化进行调整
A、通入保护电流使钢管桩表面腐蚀电流接近于零 B、通电后外电路电子被强制从高硅铸铁流向钢管桩 C、此方法在化学上称之为牺牲阳极法 D、通入的保护电流应该根据环境条件变化进行调整 -
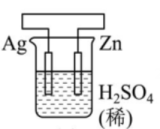
4、有关甲、乙、丙、丁四个图示的叙述正确的是( )
甲
 乙
乙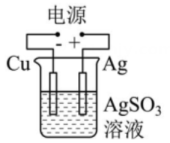 丙
丙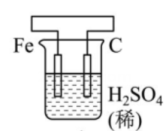 丁
丁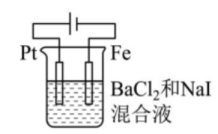 A、甲中Zn电极失去电子发生氧化反应,电子经过溶液后,流向Ag电极 B、乙中阴极反应式为 C、丙中向Fe电极方向移动 D、丁中电解开始时阳极产生黄绿色气体
A、甲中Zn电极失去电子发生氧化反应,电子经过溶液后,流向Ag电极 B、乙中阴极反应式为 C、丙中向Fe电极方向移动 D、丁中电解开始时阳极产生黄绿色气体 -
5、下列说法正确的是( )A、1mol物质完全燃烧生成指定产物时放出的热量,叫该物质的燃烧热 B、酸和碱发生中和反应生成1mol水时的反应热叫中和热 C、反应热就是焓变 D、简易量热计由内筒,外壳,隔热层,杯盖,温度计,玻璃搅拌器构成
-
6、如图是甲烷燃料电池的工作原理模拟示意图,下列说法不正确的是( )
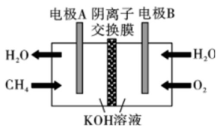 A、电极B为正极 B、在电极A上发生氧化反应 C、电极A区发生反应: D、当有通过外电路时,有通过阴离子交换膜
A、电极B为正极 B、在电极A上发生氧化反应 C、电极A区发生反应: D、当有通过外电路时,有通过阴离子交换膜 -
7、“国之重器”之一——曾侯乙编钟,是战国早期的青铜编钟,主要由铜锡合金冶炼铸造而成,至今保存完好。下列说法不正确的是( )A、铜比锡青铜更易腐蚀 B、在自然环境中,锡青铜中的铜可对锡起保护作用 C、青铜文物在潮湿环境中的腐蚀比在干燥环境中快 D、锡青铜表面生成覆盖物的过程属于电化学腐蚀
-
8、一种可充电锌—空气电池放电时的工作原理如下图所示。已知:Ⅰ室溶液中,锌主要以的形式存在,并存在。下列说法正确的是( )
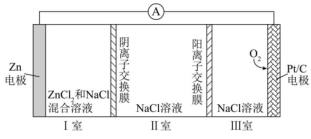 A、放电时,Ⅰ室溶液pH增大 B、放电时,该装置Ⅱ室可实现海水淡化 C、充电时,Zn电极反应为 D、充电时,每生成 , Ⅲ室溶液质量理论上减少32g
A、放电时,Ⅰ室溶液pH增大 B、放电时,该装置Ⅱ室可实现海水淡化 C、充电时,Zn电极反应为 D、充电时,每生成 , Ⅲ室溶液质量理论上减少32g -
9、下列关于物质应用的说法错误的是( )A、在医疗上,可用作钡餐 B、食用纯碱可用作食品添加剂 C、可用于制作抗胃酸药品“胃舒平” D、将铁粉、食盐和活性炭等混合可用于制作一次性保暖贴
-
10、已知:的能量变化如图所示,有关叙述正确的是( )
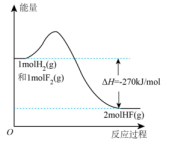 A、1mol HF(g)分解生成和需要吸收270kJ的热量 B、断裂1mol H—H键和1mol F—F键吸收的能量大于形成2mol H—F键放出的能量 C、在相同条件下,与的能量总和小于2mol HF(g)的能量 D、与反应生成2mol HF(l)放出的热量大于270kJ
A、1mol HF(g)分解生成和需要吸收270kJ的热量 B、断裂1mol H—H键和1mol F—F键吸收的能量大于形成2mol H—F键放出的能量 C、在相同条件下,与的能量总和小于2mol HF(g)的能量 D、与反应生成2mol HF(l)放出的热量大于270kJ -
11、设为阿伏加德罗常数的值,下列说法正确的是( )A、100g质量分数为46%的乙醇水溶液中含有氧原子数为 B、若将1mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为 C、向大量水中通入1mol氯气,反应中转移的电子数为 D、电解精炼铜,当电路中通过的电子数目为时,阳极质量减少6.4g
-
12、一种用于驱动潜艇的液氨—液氧燃料电池原理示意如图,下列有关该电池说法正确的是( )
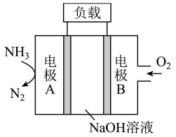 A、电极A为电池的正极 B、电池工作时,向电极B移动 C、电极A上发生的电极反应为: D、该电池工作时,每消耗转移4mol电子
A、电极A为电池的正极 B、电池工作时,向电极B移动 C、电极A上发生的电极反应为: D、该电池工作时,每消耗转移4mol电子 -
13、实验室用石墨电极电解含有酚酞的饱和NaCl溶液,装置如下图所示,下列说法不正确的是( )
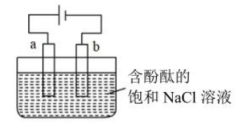 A、a极为电解池的阳极 B、a极发生的电极反应为: C、在电场作用下、向阴极移动 D、b极酚酞变红的原因是:放电,导致正向移动,
A、a极为电解池的阳极 B、a极发生的电极反应为: C、在电场作用下、向阴极移动 D、b极酚酞变红的原因是:放电,导致正向移动, -
14、中国是稀土大国,铈(Ce)是地壳中含量最高的稀土元素,主要存在与独居石中。金属铈在空气中易被氧化变暗,能与水反应,常见的化合价为+3和+4,氧化性:。下列说法正确的是( )A、、、互为同位素 B、可通过电解溶液制得金属铈 C、铈能从硫酸铜溶液中置换出铜: D、溶于氢碘酸的化学方程式可表示为
-
15、下列反应属于氧化还原反应,且是放热反应是( )A、稀醋酸与烧碱溶液反应 B、灼热的炭与的反应 C、铁片与稀盐酸的反应 D、与的反应
-
16、请回答下列问题:(1)、高铁酸钾()不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图1所示是高铁电池的模拟实验装置。
图1
 图2
图2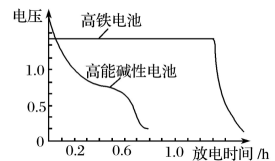
①该电池放电时正极反应式为。
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向(填“左”或“右”)移动;
③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有。
(2)、铜是人类最早使用的金属,它与人类生产、生活关系密切,请运用所学知识解释下列与铜有关的化学现象。甲
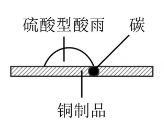 乙
乙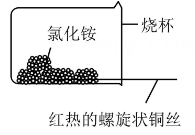
①如图甲,在硫酸型酸雨地区,不纯的铜制品发生电化学腐蚀,Cu发生(填“氧化”或“还原”)反应,写出正极的电极反应式:。
②如图乙,将螺旋状的铜丝在酒精灯上灼烧,铜丝变黑色,然后将红热的铜丝插入固体中,过一会取出,发现插入部分黑色变为光亮的红色,查阅资料可知,该过程有生成,写出由黑色变为光亮红色过程中反应的化学方程式:。
(3)、一定温度下,反应中的某一基元反应为 , 其能量变化如图所示。表示反应物分子旧化学键没有完全断裂、新化学键没有完全形成的过渡态。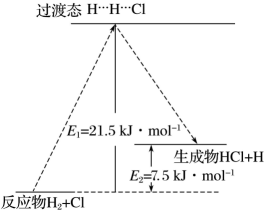
该基元反应的活化能为kJ/mol,为kJ/mol。
(4)、键能也可以用于估算化学反应的反应热()。下表是部分化学键的键能数据:化学键
键能/(kJ/mol)
172
335
498
X
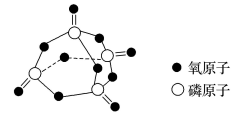
已知白磷的标准燃烧热为-2378kJ/mol,白磷的结构为正四面体,白磷完全燃烧的产物结构如图所示,则上表中。
-
17、为实现我国承诺的“碳达峰、碳中和”目标,中国科学院提出了“液态阳光”方案,即将工业生产过程中排放的二氧化碳转化为甲醇,其中反应之一是: 。回答下列问题:(1)、该反应的能量变化如图所示,反应的 , 曲线(填“a”或“b”)表示使用了催化剂。
 (2)、下列措施既能加快反应速率,又能提高CO转化率的是____;A、升高温度 B、增大压强 C、降低温度 D、增加投料量(3)、相同温度下,若已知:
(2)、下列措施既能加快反应速率,又能提高CO转化率的是____;A、升高温度 B、增大压强 C、降低温度 D、增加投料量(3)、相同温度下,若已知:①反应的平衡常数为;
②反应的平衡常数为;
则:反应的化学平衡常数(用含和的代数式表示)。
(4)、在恒温恒容密闭容器中按加入反应起始物Ⅰ.下列描述不能说明反应达到平衡状态的是。
A.容器内压强不再变化 B.氢气的转化率达到最大值
C.容器内CO与的浓度相等 D.容器内CO的体积分数不再变化
Ⅱ.若CO的平衡转化率[]随温度的变化曲线如图Ⅱ所示,R、S两点平衡常数大小:(填“>”、“=”或“<”)。温度下,测得起始压强 , 达平衡时。
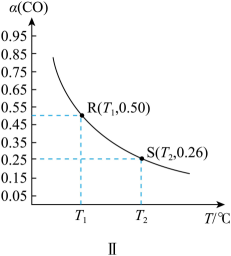
-
18、电池的种类繁多,应用广泛。根据电化学原理回答下列问题。(1)、电池是一种能被海水激活的一次性贮备电池,电池总反应为 , 则负极材料为 , 正极反应式为。(2)、浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。X极生成时,移向(填“X”或“Y”)极。
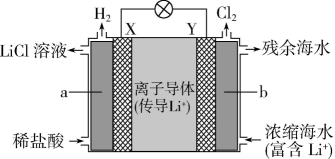 (3)、微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用如图装置处理有机废水(以含的溶液为例)。隔膜1为(填“阴”或“阳”)离子交换膜,负极的电极反应式为 , 当电路中转移0.2mol电子时,模拟海水理论上除盐g。
(3)、微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用如图装置处理有机废水(以含的溶液为例)。隔膜1为(填“阴”或“阳”)离子交换膜,负极的电极反应式为 , 当电路中转移0.2mol电子时,模拟海水理论上除盐g。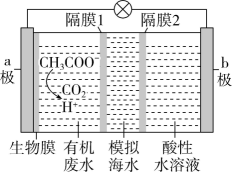
-
19、某市对大气进行监测,发现该市首要污染物为可吸入颗粒物(直径小于等于的悬浮颗粒物),其主要来源为燃煤、机动车尾气等因此,对、、等进行研究具有重要意义。
请回答下列问题:
(1)、为减少的排放,常采取的措施如下:将煤转化为清洁气体燃料。已知: ;
。
写出焦炭与水蒸气反应的热化学方程式:。
(2)、汽车尾气的转化:①NO在催化条件下分解,反应在恒温密闭容器中下进行: ;某温度下,NO平衡转化率为10.0%,该温度下的平衡常数为 , 若某时刻、、分别为2.0mol、1.0mol、0.50mol,此时反应(填序号)。
a.向逆反应方向进行
b.向正反应方向进行
c.达到平衡状态
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:。已知该反应的 , 简述该设想能否实现的依据:。
(3)、清洁能源具有广阔的开发和应用前景,可减小污染解决雾霾问题,其中甲醇、甲烷是优质的清洁燃料,可制作燃料电池,一定条件下用CO和合成: 。向体积为2L的密闭容器中充入2molCO和 , 测得不同条件下容器内的压强(P:kPa)随时间(min)的变化关系如图中Ⅰ、Ⅱ、Ⅲ曲线所示:
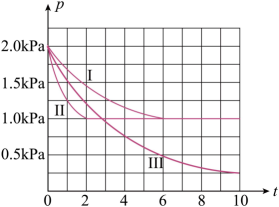
①Ⅱ和Ⅰ相比,改变的反应条件是;
②若反应Ⅰ的温度(),反应Ⅲ的温度(),则(填“小于”、“大于”或“等于”),简要说明判断依据:。
-
20、执法交警最常用的一种酒精检测仪的工作原理示意图如图所示,其反应原理为: , 被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。下列说法正确的是( )
 A、呼出气体中酒精含量越高,微处理器中通过的电流越小 B、电解质溶液中的移向a电极 C、b为正极,电极反应式为 D、a极上的电极反应式为
A、呼出气体中酒精含量越高,微处理器中通过的电流越小 B、电解质溶液中的移向a电极 C、b为正极,电极反应式为 D、a极上的电极反应式为