-
1、利用油脂厂废弃的镍(Ni)催化剂(主要含有Ni、Al、Fe及少量NiO、、)制备铁黄(FeOOH)和的工艺流程如图所示,回答下列问题:
 (1)、“碱浸”中NaOH作用有:①去除油脂;②溶解Al和 , 试写出与NaOH溶液反应的离子方程式:。(2)、“滤液2”中含有的金属阳离子除外,主要有。(3)、“转化”中加入的目的是 , 写出其离子方程式: , 可用最佳的物质(填化学式)来代替。(4)、写出生成铁黄的离子方程式:。(5)、“系列操作”包括、、过滤、洗涤、干燥得到。
(1)、“碱浸”中NaOH作用有:①去除油脂;②溶解Al和 , 试写出与NaOH溶液反应的离子方程式:。(2)、“滤液2”中含有的金属阳离子除外,主要有。(3)、“转化”中加入的目的是 , 写出其离子方程式: , 可用最佳的物质(填化学式)来代替。(4)、写出生成铁黄的离子方程式:。(5)、“系列操作”包括、、过滤、洗涤、干燥得到。 -
2、将5.6g铁粉加入一定体积的某浓度的硝酸中,加热充分反应后,铁粉完全溶解,将生成的气体和0.06mol混合通入足量水中,气体完全被水吸收并生成。下列说法错误的是A、铁粉反应后溶液中剩余的的物质的量为0.24mol B、生成的气体在标准状况下的体积一定为1.792L C、铁粉反应后溶液中既有又有 D、若向铁粉反应后溶液加入足量氢氧化钠溶液,过滤、洗涤、灼烧沉淀得到8g固体
-
3、依据下列实验操作和现象,得出的相应结论正确的是
选项
实验操作
现象
结论
A
向淀粉溶液中加入几滴稀硫酸,加热,待冷却后,加入新制的悬浊液
无砖红色沉淀
淀粉未发生水解
B
向NaBr溶液中滴入过量氯水,再加入淀粉KI溶液
先变橙色,后变蓝色
氧化性:
C
某溶液中加入溶液,待产生沉淀后,再加入稀硝酸
白色沉淀不溶解
该溶液中一定含有
D
向食用碘盐中加入食醋和KI溶液,再加入淀粉KI溶液
溶液呈蓝色
该食用碘盐中含有
A、A B、B C、C D、D -
4、如图为硫元素或氮元素的价类二维图,W为同一种可溶性正盐。下列描述正确的是
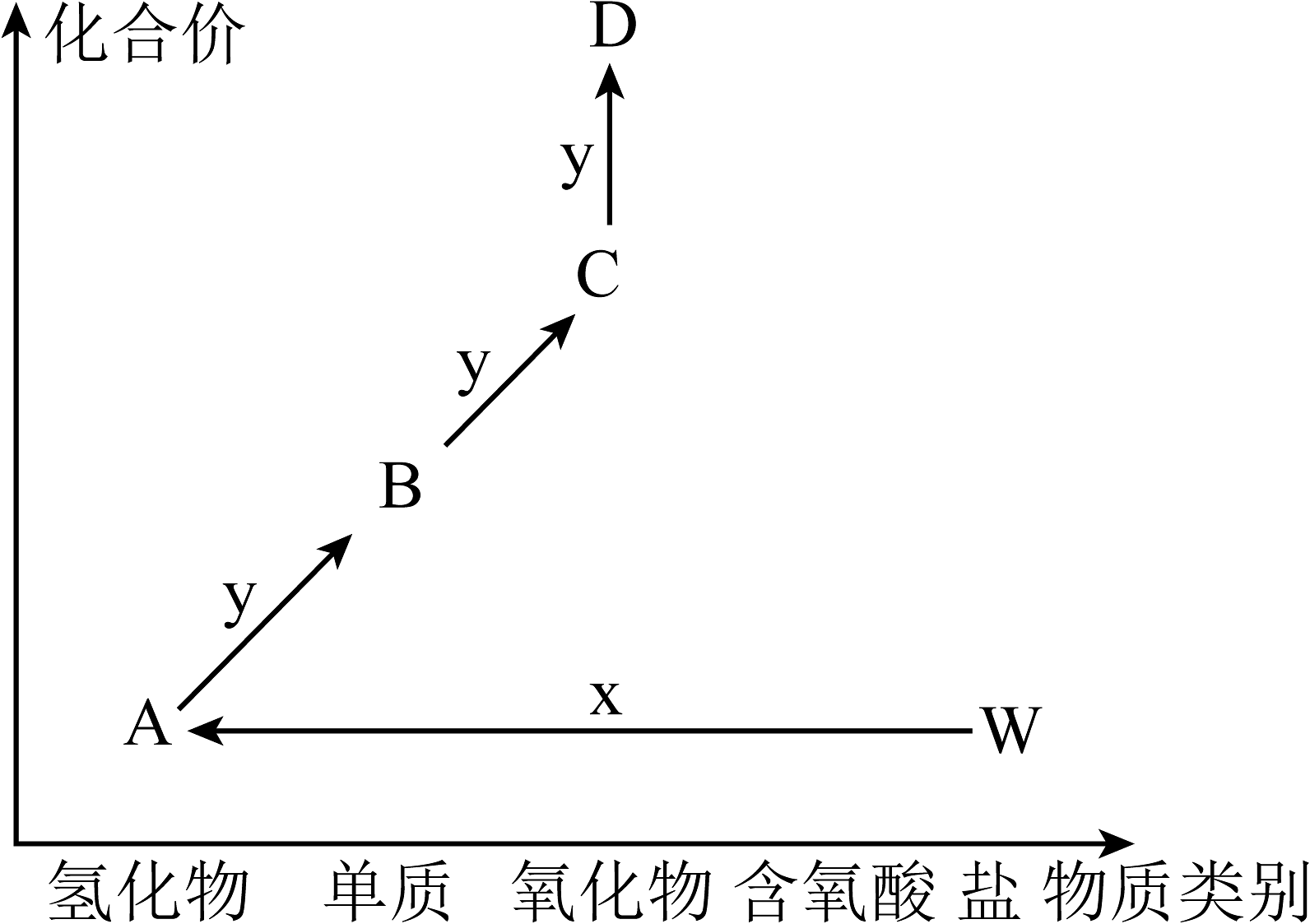 A、W为 B、若x为NaOH溶液,得到A和经催化氧化易生成B C、若x为NaOH溶液,C与D按体积比1∶1通入足量的x中不能被完全吸收 D、若x为稀硫酸,少量C与溶液反应:
A、W为 B、若x为NaOH溶液,得到A和经催化氧化易生成B C、若x为NaOH溶液,C与D按体积比1∶1通入足量的x中不能被完全吸收 D、若x为稀硫酸,少量C与溶液反应: -
5、“纳米零价铁——”体系可将烟气中难溶的NO氧化为可溶的。在一定温度下,将溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。已知催化分解产生HO• ,HO•将NO氧化为的机理如图所示。下列说法错误的是
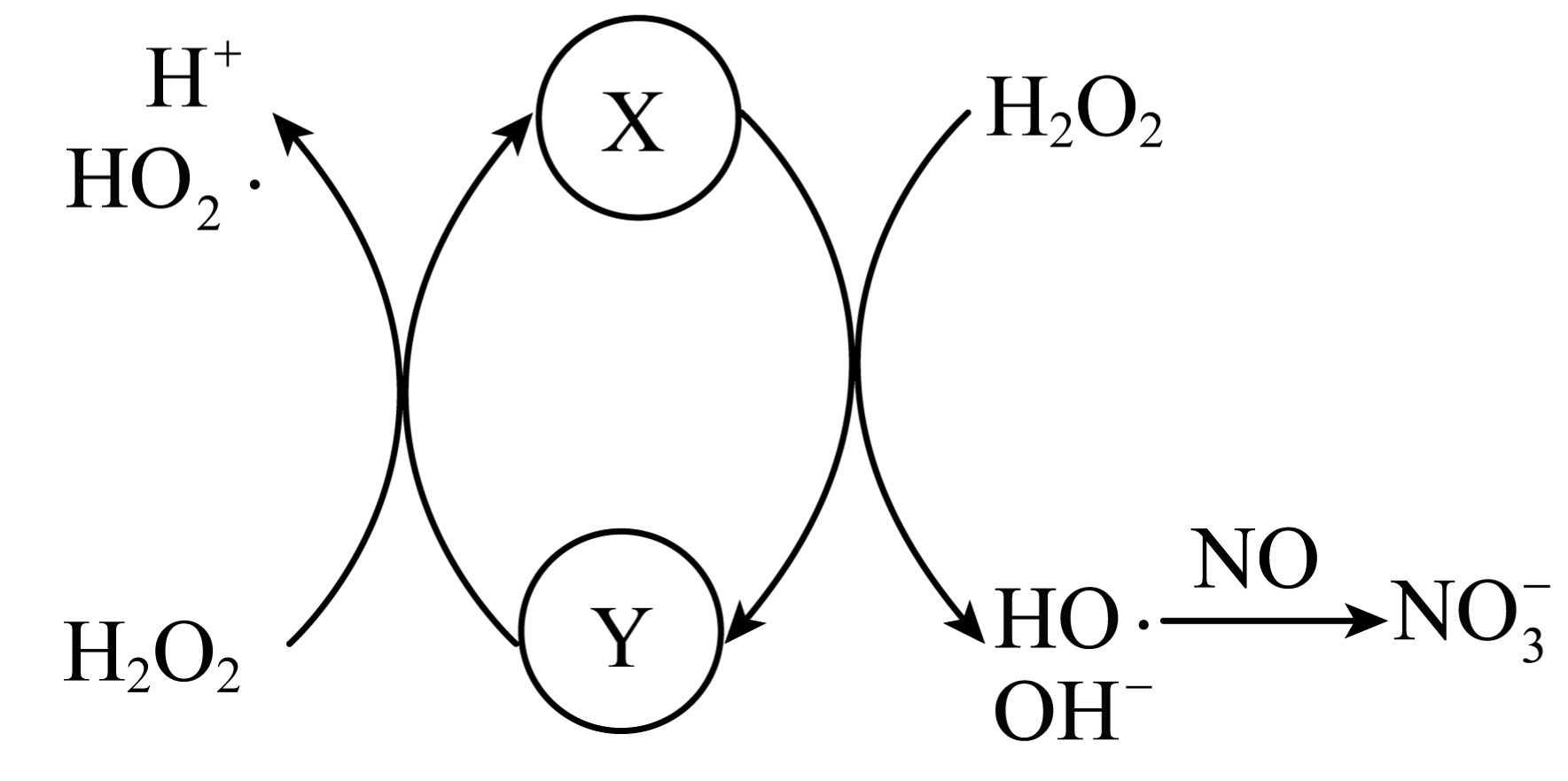 A、Y是 , 可用KSCN溶液来检验 B、温度越高,化学反应速率越快,NO脱除率会越高 C、氧化NO的总反应为: D、纳米零价铁的作用是与HCl反应生成 , 作反应的催化剂
A、Y是 , 可用KSCN溶液来检验 B、温度越高,化学反应速率越快,NO脱除率会越高 C、氧化NO的总反应为: D、纳米零价铁的作用是与HCl反应生成 , 作反应的催化剂 -
6、某化学兴趣小组利用数字传感技术测定喷泉实验中仪器内的压强变化,来进一步认识喷泉实验的原理,装置和电脑绘制的三颈烧瓶内压强变化曲线如图所示。下列说法错误的是
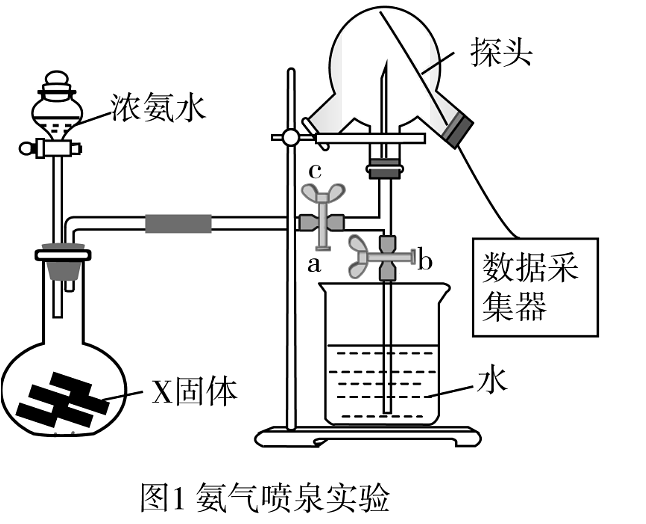
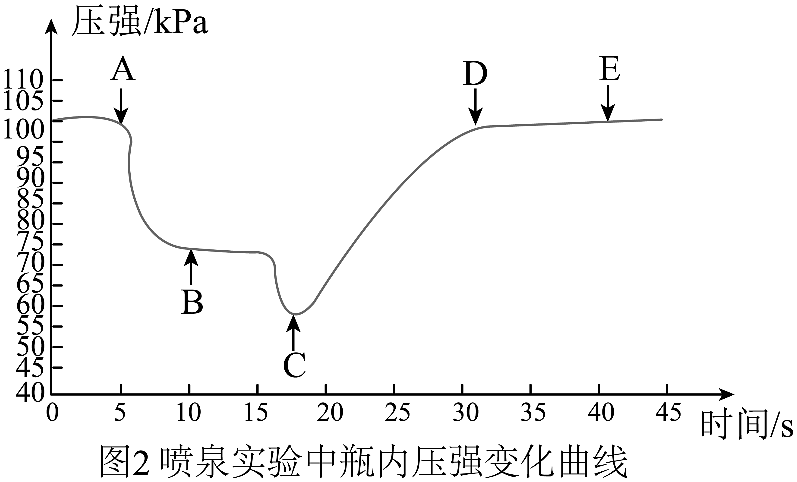 A、喷泉实验成功的关键是装置的气密性好、干燥和氨气充足 B、收集气体的操作是同时打开弹簧夹a和b C、根据曲线可知C点所对应的是喷泉最剧烈的时刻 D、根据曲线还可以得出:排空气法无法收集纯净的氨气
A、喷泉实验成功的关键是装置的气密性好、干燥和氨气充足 B、收集气体的操作是同时打开弹簧夹a和b C、根据曲线可知C点所对应的是喷泉最剧烈的时刻 D、根据曲线还可以得出:排空气法无法收集纯净的氨气 -
7、“新能源汽车、锂电池、光伏产品给中国制造增添了新亮色”。氢燃料电池被誉为氢能源汽车的心脏。某种氢燃料电池的内部结构如图所示。下列说法错误的是
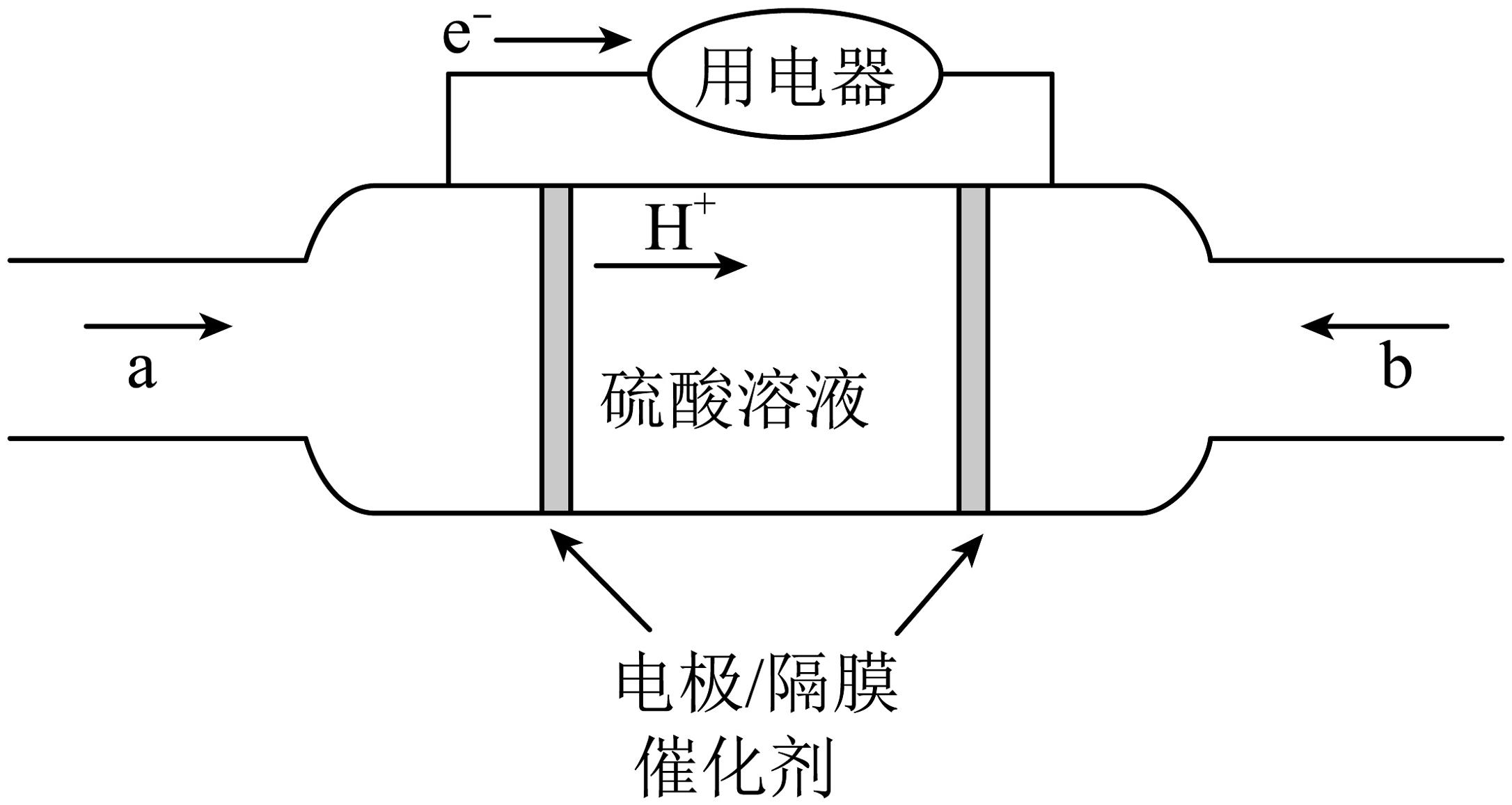 A、左侧的电极反应式为 B、电池工作一段时间后,电解质溶液中的数目会增多 C、该装置实现了化学能转化为电能 D、电解质溶液中无电子通过
A、左侧的电极反应式为 B、电池工作一段时间后,电解质溶液中的数目会增多 C、该装置实现了化学能转化为电能 D、电解质溶液中无电子通过 -
8、皮江法冶炼镁的工业流程如图所示。已知铁的沸点2750℃,镁的沸点1107℃。下列说法错误的是
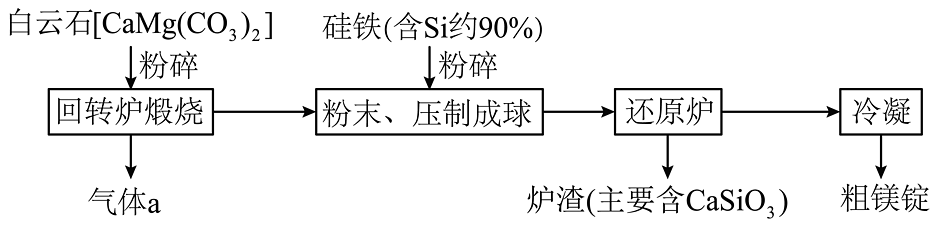 A、白云石粉碎的目的是增大固体表面积,加快化学反应速率 B、还原炉中发生的反应为 C、还原炉内可用气体a来排除空气 D、还原炉需控制温度为1200℃左右,目的是分离提纯金属镁
A、白云石粉碎的目的是增大固体表面积,加快化学反应速率 B、还原炉中发生的反应为 C、还原炉内可用气体a来排除空气 D、还原炉需控制温度为1200℃左右,目的是分离提纯金属镁 -
9、A是一种重要的有机化工原料,可生产美丽的亚克力玻璃。已知A只含C、H、O三种元素,其分子的球棍模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等)。下列有关A的说法错误的是
 A、分子式为 B、分子中所有碳原子都在同一个平面上 C、与A具有相同官能团的同分异构体只有一种 D、能发生氧化、加成、取代反应
A、分子式为 B、分子中所有碳原子都在同一个平面上 C、与A具有相同官能团的同分异构体只有一种 D、能发生氧化、加成、取代反应 -
10、X、Y、Z、M、N是原子序数依次递增的短周期主族元素。X的一种同位素原子常用于考古断代,Y与M同主族,且M的原子序数是Y的2倍,Z是短周期中原子半径最大的元素。下列说法错误的是A、最高价氧化物对应水化物的酸性:M<N B、Y的一种氢化物可能与M的氢化物反应 C、固态转变为气态,需克服分子间作用力 D、Y、Z、M形成的化合物只有两种
-
11、一定温度下在一固定容积的密闭容器中发生如下反应: 。下列有关说法正确的是A、充入2mol和2.5mol充分反应后放出热量为452kJ B、密闭容器内压强不再变化时,说明该反应达到平衡状态 C、反应物的总键能大于生成物的总键能 D、通入He,增大压强,正逆反应速率都增大
-
12、侯氏制碱法主要反应原理:。下列说法正确的是A、的电子式为
 B、在制备时,将氨气与二氧化碳同时通入
C、的分子结构模型为
B、在制备时,将氨气与二氧化碳同时通入
C、的分子结构模型为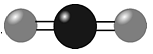 D、与盐酸反应会释放热量
D、与盐酸反应会释放热量
-
13、设为阿伏加德罗常数的值,下列说法正确的是A、标准状况下,11.2L所含的氢原子数为 B、1L 0.1mol/L的氨水中,所含的的分子数为 C、常温常压下,1mol羟基中含有的电子数为 D、0.3mol与水完全反应转移的电子数为
-
14、下列离子方程式书写正确的是A、将少量氯水加入饱和溶液中: B、向溶液中同时通入和: C、将乙酸滴入氢氧化铜悬浊液中: D、过量的与溶液反应:
-
15、各式各样的材料与生活息息相关,下列说法错误的是A、大型天线所使用的碳纤维属于无机非金属材料 B、二氧化硅具有导电性,故可以用于制作光导纤维 C、新型陶瓷的主要成分不再是硅酸盐 D、做食品保鲜袋的材料主要是聚乙烯塑料
-
16、下列各组离子在指定的溶液中,能大量共存的一组是A、无色溶液中: K+、Na+、SO、MnO B、酸性溶液中:Mg2+、Na+、SO、Cl- C、pH=11的溶液中:Zn2+、Ba2+、NO、Cl- D、含有大量Ba2+的溶液中:K+、NH、SO、NO
-
17、现代生活需要人们有一定的科学素养,下列有关化学的科学常识正确的是A、为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰 B、碳酸钠俗名小苏打,可用作糕点膨松剂 C、Na2O2吸收CO2产生O2 , 可用作呼吸面具供氧剂 D、次氯酸见光易分解,所以氯水应保存在钢瓶中
-
18、考古遗迹和历史文物是历史的见证,反映了古代人民丰富多彩的生活。下列文物属于无机非金属材料的是




铜烤炉
黄花梨云龙纹条案
三彩骑卧驼陶俑
山居图扇面
A
B
C
D
A、A B、B C、C D、D -
19、X、Y、W、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知X的一种核素的质量数为18,中子数为10,Y和Ne原子的核外电子总数相差1;W的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强。
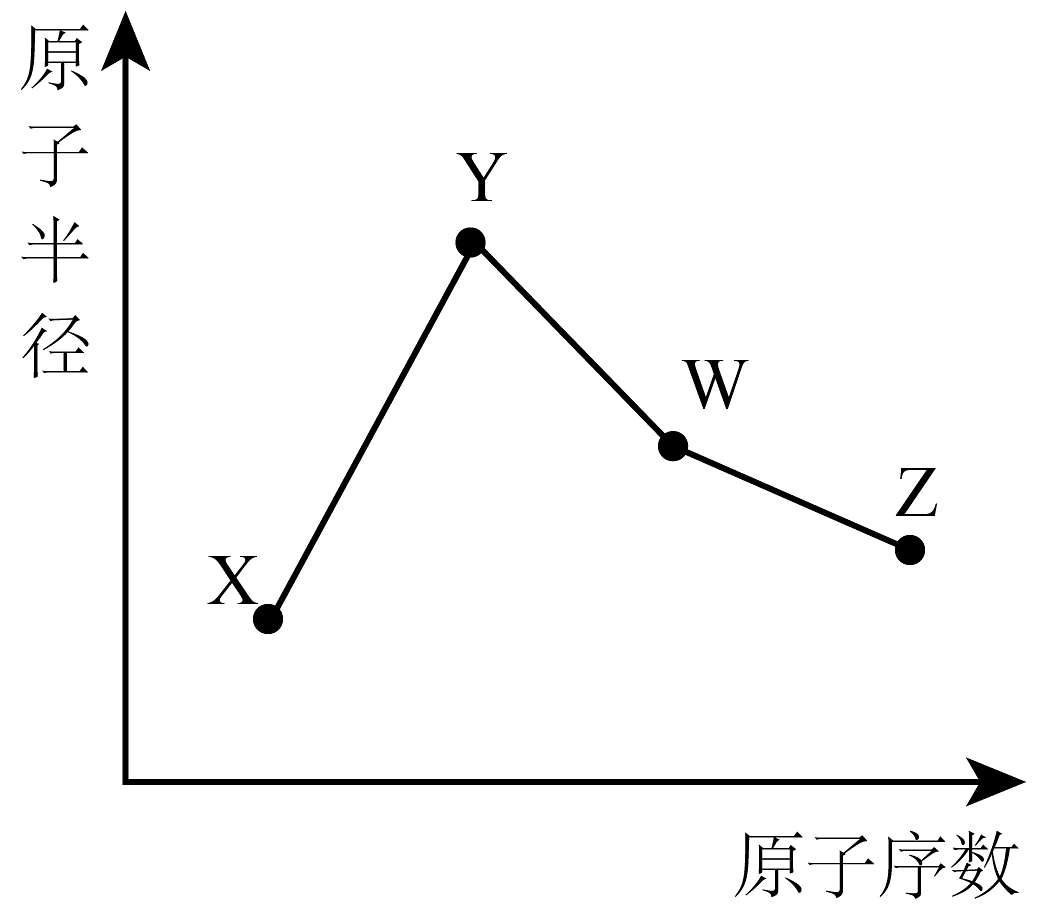 (1)、W位于元素周期表中第周期第族。画出X的阴离子的结构示意图。(2)、Z的氢化物和溴化氢相比,较稳定的是(写化学式);Z的氢化物与氟化氢相比,沸点较高的是(写化学式)。(3)、Y的金属性与Mg的金属性相比,(写化学式)的金属性强,请用实验证明它们金属性的相对强弱:。(4)、写出Y的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物发生反应的化学反应方程式:。
(1)、W位于元素周期表中第周期第族。画出X的阴离子的结构示意图。(2)、Z的氢化物和溴化氢相比,较稳定的是(写化学式);Z的氢化物与氟化氢相比,沸点较高的是(写化学式)。(3)、Y的金属性与Mg的金属性相比,(写化学式)的金属性强,请用实验证明它们金属性的相对强弱:。(4)、写出Y的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物发生反应的化学反应方程式:。 -
20、现有中学化学中常见的几种物质:。请回答下列问题:(1)、上述物质中常用作氧化剂的有填序号。(2)、在一定条件下发生反应: , 反应中硝酸体现的性质是和 , 被还原的与未被还原的的质量比为。(3)、可作为矿业废液消毒剂,可以消除采矿业废液中的氰化物如 , 其中为价 , 化学方程式为:已配平
生成物的化学式为。
用双线桥法表示该反应中电子转移的方向和数目:。
(4)、人体内所含铁元素以和的形式存在市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为 , 但在酸性条件下很容易被空气中的氧气氧化成填写离子符号。