-
1、按要求回答下列问题:(1)、用系统命名法命名:
①
 :。②
:。②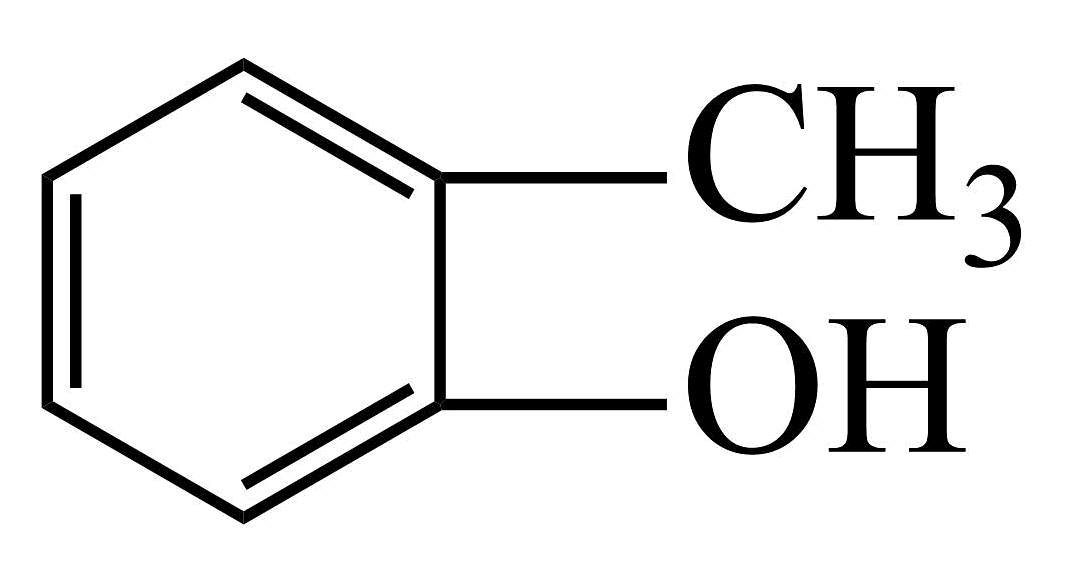 :。(2)、分子式为的芳香烃,苯环上的二氯代物有3种,其结构简式是。(3)、完成下列反应的化学方程式。
:。(2)、分子式为的芳香烃,苯环上的二氯代物有3种,其结构简式是。(3)、完成下列反应的化学方程式。①1,3-丁二烯与氯气发生1,4-加成:。
②甲苯与浓硫酸、浓硝酸的混合酸在100℃共热制得TNT:。
③向苯酚钠溶液中通入少量:。
④对苯二甲酸与乙二醇合成高分子化合物聚对苯二甲酸乙二酯:。
(4)、已知: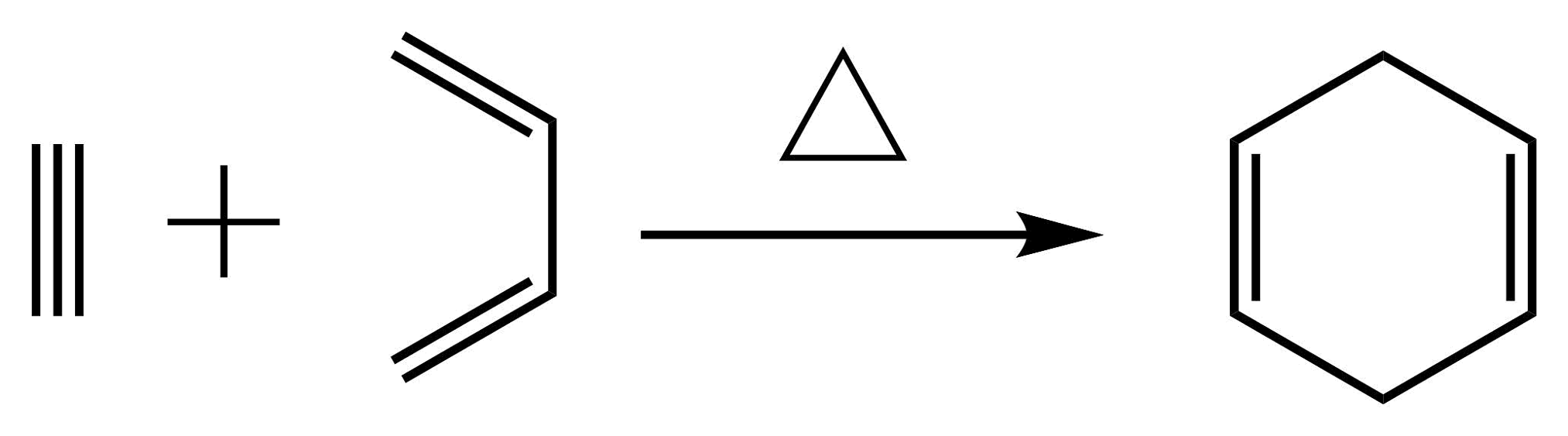 , 合成
, 合成 所用的原料是(用键线式表示)。
所用的原料是(用键线式表示)。 -
2、药品是一种免疫调节剂,其合成路线如下。下列说法正确的是
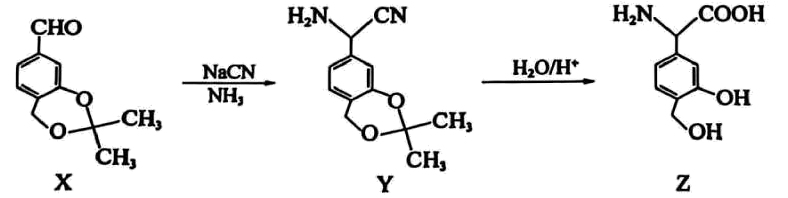 A、X分子中所有原子可能共平面 B、分子中含有2个手性碳原子 C、最多能与反应 D、可以用酸性溶液检验中是否含有
A、X分子中所有原子可能共平面 B、分子中含有2个手性碳原子 C、最多能与反应 D、可以用酸性溶液检验中是否含有 -
3、葫芦脲在超分子化学和材料科学中发挥着重要的作用。葫芦[7]脲的合成路线如下图所示,试剂和试剂均能发生银镜反应。

下列说法不正确的是
A、E与试剂a反应中二者消耗的物质的量之比为2:1 B、F、G互为同系物 C、试剂a、b的核磁共振氢谱均仅有一组峰 D、由为原料制取生成 -
4、根据下列实验操作和现象得出的结论正确的是
选项
实验操作和现象
结论
A
将少量某卤代烃与溶液混合共热,充分反应并冷却后,向溶液中加稀酸化,再滴加溶液,产生淡黄色沉淀
该卤代烃含溴元素
B
向可能含有少量苯酚的苯中滴加过量的浓溴水,未出现白色沉淀
苯中不含苯酚
C
在试管中取约溶液,加入5滴溶液,振荡后加入有机物溶液并加热,无砖红色沉淀产生
X中不含醛基
D
在试管中取少量滴有酚酞的氢氧化钠溶液,向其中滴入有机液体直至过量,溶液颜色褪去
X中含有羧基
A、A B、B C、C D、D -
5、下列有关乙酸乙酯制备实验的说法正确的是
 A、加热有利于加快反应速率,应尽可能提供较高温度 B、反应一段时间后红色溶液上方出现油状液体,其中不含密度比水大的乙酸 C、取出试管B并充分振荡后上层油状液体体积减少,部分乙酸乙酯溶解于下层溶液 D、向振荡后红色褪去的下层溶液中滴入酚酞后又出现红色,说明酚酞溶于乙酸乙酯
A、加热有利于加快反应速率,应尽可能提供较高温度 B、反应一段时间后红色溶液上方出现油状液体,其中不含密度比水大的乙酸 C、取出试管B并充分振荡后上层油状液体体积减少,部分乙酸乙酯溶解于下层溶液 D、向振荡后红色褪去的下层溶液中滴入酚酞后又出现红色,说明酚酞溶于乙酸乙酯 -
6、酸性条件下,环氧乙烷水合法制备乙二醇涉及的机理如图:
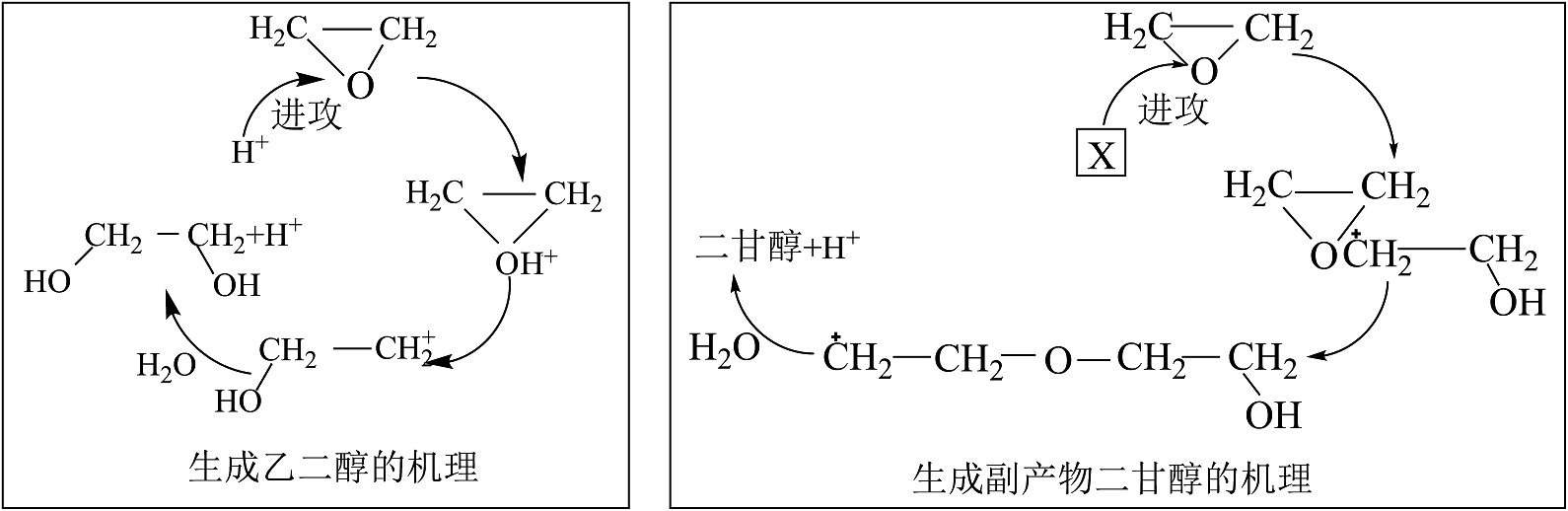
下列说法不正确的是
A、的结构简式为: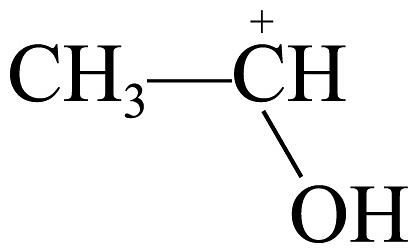 B、进攻环氧乙烷中的氧原子是因为碳氧键的共用电子对偏向氧
C、在制备乙二醇的反应中起催化作用
D、二甘醇是乙二醇发生分子间脱水反应的产物
B、进攻环氧乙烷中的氧原子是因为碳氧键的共用电子对偏向氧
C、在制备乙二醇的反应中起催化作用
D、二甘醇是乙二醇发生分子间脱水反应的产物
-
7、有机小分子通过选择性催化聚合可分别得到聚合物和 , 下列说法不正确的是
 A、X的结构简式为
A、X的结构简式为 B、Z中含有的官能团为酯基和碳碳双键
C、由生成的反应为缩聚反应
D、能在溶液中降解为小分子而不能
B、Z中含有的官能团为酯基和碳碳双键
C、由生成的反应为缩聚反应
D、能在溶液中降解为小分子而不能
-
8、按下图实验装置(部分装置略)对有机样品进行元素分析。样品完全灼烧并将所有气体产物充分吸收后,管增重管增重。质谱法测得该有机物的相对分子质量为118。下列说法正确的是
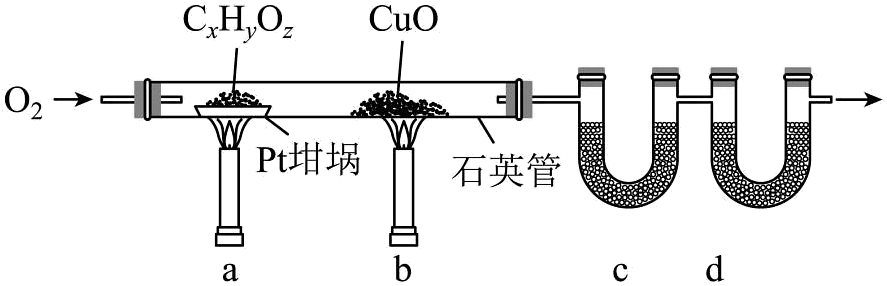 A、先通入氧气,再先后点燃a、b处煤气灯 B、中使用碱石灰吸收反应产生的 C、若撤去可能导致测得中值偏大 D、该有机物的分子式为
A、先通入氧气,再先后点燃a、b处煤气灯 B、中使用碱石灰吸收反应产生的 C、若撤去可能导致测得中值偏大 D、该有机物的分子式为 -
9、乙烯使溴水快速褪色的反应历程如图所示:

已知:①乙烯使溴的四氯化碳溶液褪色比该反应慢得多;②完全反应后两种产物含量分别为10.2%和89.8%。下列说法不正确的是
A、对乙烯与溴加成生成1,2-二溴乙烷的反应具有催化作用 B、中间产物 中所有原子最外层均达到稳定结构
C、反应Ⅱ得到两种产物含量不同的原因是溴水中浓度大于
D、乙烯与溴水反应产物应有1-溴乙醇次溴酸酯
中所有原子最外层均达到稳定结构
C、反应Ⅱ得到两种产物含量不同的原因是溴水中浓度大于
D、乙烯与溴水反应产物应有1-溴乙醇次溴酸酯
-
10、下列有机物的命名正确的是
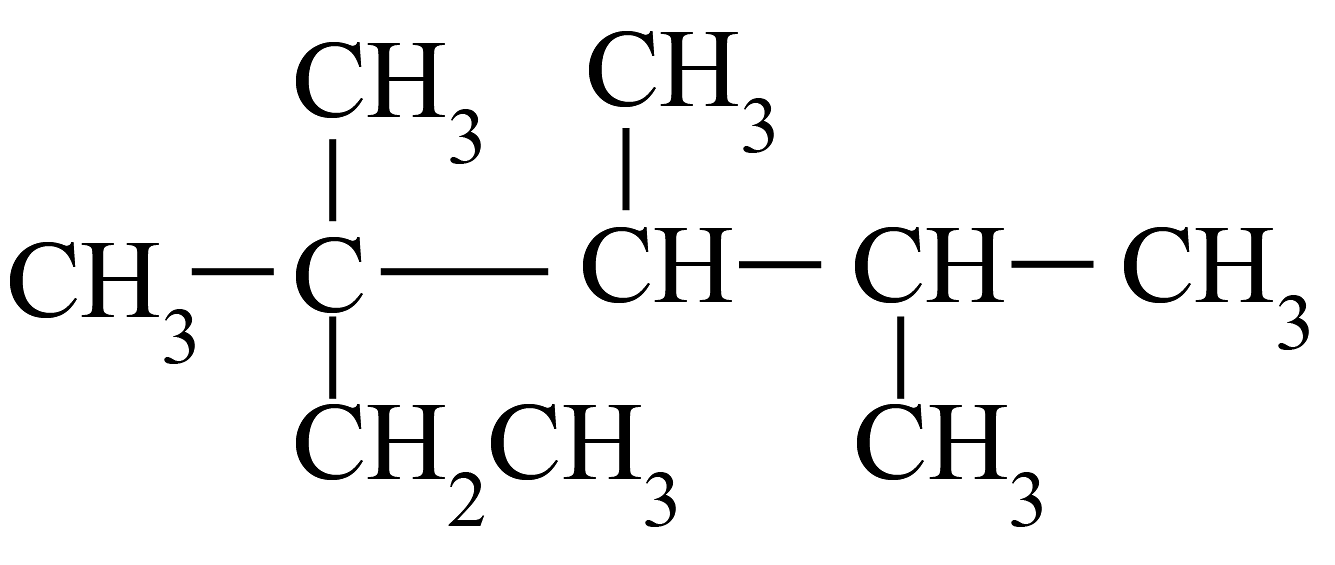

A.2,3,4-三甲基-2-乙基戊烷
B.1,3-二丙醇
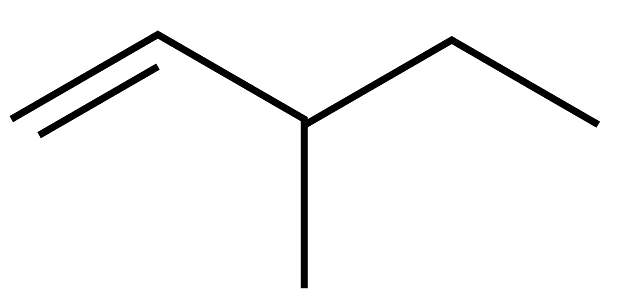
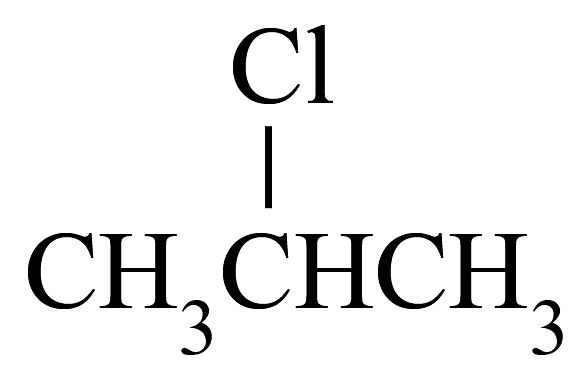
C.3-乙基-1-丁烯
D.2-氯丙烷
A、A B、B C、C D、D -
11、下列装置或操作能达到相应实验目的的是
 A、配制银氨溶液 B、比较碳酸与苯酚酸性强弱 C、制取少量乙二酸 D、分离硝基苯和苯
A、配制银氨溶液 B、比较碳酸与苯酚酸性强弱 C、制取少量乙二酸 D、分离硝基苯和苯 -
12、有关石油和煤的说法不正确的是A、石油加工可获得乙烯 B、煤加工可获得苯 C、石油的分馏、裂化裂解均为物理变化 D、煤的干馏、气化和液化均为化学变化
-
13、下列化学用语错误的是A、甲醛分子的电子式:
 B、聚丙烯的结构简式:
B、聚丙烯的结构简式: C、2-乙基-1,3-丁二烯的键线式:
C、2-乙基-1,3-丁二烯的键线式: D、丙烷分子的球棍模型:
D、丙烷分子的球棍模型: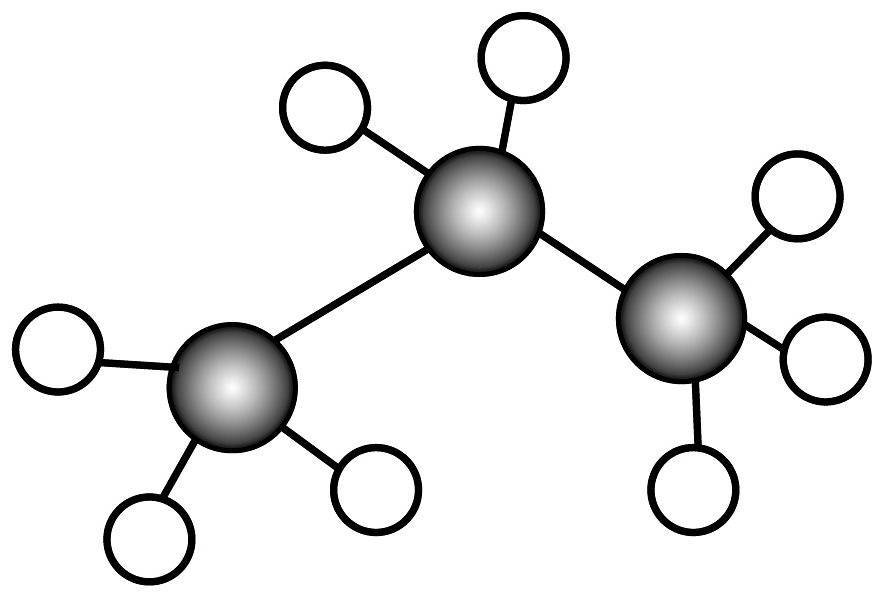
-
14、化学与生产、生活、环境等密切相关,下列说法正确的是A、推广使用可降解塑料制品是为了防止白色污染 B、医疗上用95%的酒精或福尔马林稀溶液杀菌消毒 C、“泡腾片实验”中柠檬酸与小苏打反应是因为柠檬酸具有强还原性 D、制作户外运动服装所需要高强度和耐磨性的锦纶(聚酰胺纤维)是纯净物
-
15、一种采用催化氧化法处理废气的原理如下:
。
将和分别以不同起始流速通入反应器中,在、和下反应,通过检测流出气成分绘制转化率()曲线,如下图所示(较低流速下转化率可近似为平衡转化率)。

回答下列问题:
(1)、已知的燃烧热;;
。
则催化氧化法处理废气的
(2)、该反应在温度较时(填“高”或“低”)容易自发进行,结合图像分析。(3)、图1中的a、b、c三点中,最可能到达平衡状态的是(填标号)。(4)、下列措施可提高M点转化率的是___________(填标号)。A、增大 B、降低温度 C、增大的流速 D、使用更高效的催化剂(5)、在温度为 , 初始压强为的恒容密闭容器中,按图2中的投料比进行反应,到达平衡时与N点的转化率相同,求该温度下反应的化学平衡常数。(6)、另一种以为催化剂,用氧化制的反应历程如下:第一步:;
第二步:___________;
第三步:。
写出第二步反应的化学方程式:。
-
16、从铜阳极泥(主要成分为等)中分离提取金属单质的流程如下图所示。

已知:i.溶于盐酸可以得到。
ii. 。
iii.
回答下列问题:
(1)、“浸取1”中一般控制温度为左右,原因是。(2)、“浸取2”中,盐酸的作用为①提供酸性环境;②。(3)、“浸取3”中发生反应的离子方程式为;若“浸取3”中用溶液浸取,最终回收单质的质量为(假设的回收率为),那么需要的的物质的量至少为(保留四位有效数字。已知)。(4)、“电沉积”中获得单质的是极(“正”“负”或“阴”“阳”);“电沉积”完成后,在此极区溶液中可循环利用的物质为(填化学式)(5)、“还原”中。发生反应的化学方程式为。 -
17、沙丁胺醇(F)能有效地抑制组胺等致过敏性物质的释放,防止支气管痉挛,其一种合成路线如下

已知:
i.为 , 为
 , 为
, 为
ii.

回答下列问题:
(1)、物质A的名称为。(2)、物质B的结构简式为 , C→D的反应类型为。(3)、写出D→E的化学方程式:。(4)、比D少1个碳原子的同分异构体中,同时满足下列条件的芳香族化合物有种,其中核磁共振氢谱峰面积比为的结构简式为。①苯环上含三个取代基,其中两个为 ②除苯环外不含其他环状结构
(5)、参照上述路线写出以苯甲醛为主要原料(其他试剂任选)合成 的路线:。
的路线:。 -
18、
氨基甲酸铵()是一种受热易分解、易水解的白色固体,易溶于水,难溶于 , 可用作肥料、灭火剂、洗涤剂等。某研究小组选用下列装置制备氨基甲酸铵(),并测定其纯度。反应原理为。

回答下列问题:
I.制备氨基甲酸铵
(1)装置A中盛放浓氨水的仪器名称是 , 需向装置A三颈烧瓶中加入的固体为(填名称)。
(2)上图装置连接顺序为氨气的发生装置→→ab←←e(每个装置限用一次,箭头方向为气流方向,用小写字母表示)。
(3)装置B采用冰水浴的原因是。
(4)装置B中的气球可以用(填“甲”或“乙”)装置代替,该装置的作用为。

Ⅱ.测定产品纯度
(5)甲醛法常用于测定铵盐的纯度。[已知:]
实验步骤:
样品处理:称取氨基甲酸铵样品,溶于水后定容至。
甲醛预处理:将甲醛溶液煮沸(除微量甲酸),冷却后调至中性。
反应与滴定:移取样品溶液,加入中性甲醛溶液,静置 , 以酚酞为指示剂,用标准液滴定至微红色,消耗。
①静置是甲醛滴定法中减小误差的关键步骤,除避免时间过长碳酸分解而损耗外,另一原因是。
②样品中氨基甲酸铵的纯度为。
-
19、两种同构的吡啶羧酸铜框架[和]对和具有选择性吸附行为。

回答下列问题:
(1)、中中心离子的配位数为 , 基态核外电子排布式为。配位体 与苯甲酸的酸性:
与苯甲酸的酸性: 苯甲酸(填“>”或“<”),
苯甲酸(填“>”或“<”), 中氮原子的孤电子对存在于轨道。 (2)、实验室中能合成很多含的配合物。
中氮原子的孤电子对存在于轨道。 (2)、实验室中能合成很多含的配合物。①与生成紫色物质,其结构如图所示。已知含有多个配位原子的配体与同一中心离子或原子通过螯合配位成环而形成的配合物为螯合物。该离子通过整合作用形成的配位键数目为。

②具有对称的空间结构,其中的两个被取代,得到两种不同结构的产物a和b,结构如下。a、b在水中的溶解度:ab(填“>”“<”或“=”),原因是。
 (3)、元素Q是与铜同周期且最外层电子数相等的主族元素,Q与氧元素形成的一种化合物的晶胞投影如下图所示,该化合物的化学式为;设其晶胞参数为 , 为阿伏加德罗常数的值,该晶胞的密度(用含a、的代数式表示)。
(3)、元素Q是与铜同周期且最外层电子数相等的主族元素,Q与氧元素形成的一种化合物的晶胞投影如下图所示,该化合物的化学式为;设其晶胞参数为 , 为阿伏加德罗常数的值,该晶胞的密度(用含a、的代数式表示)。
-
20、甲烷蒸汽重整是目前工业制氢的手段,主要反应如下
反应I:
反应II:
下,将的混合气体投入恒压反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。下列说法正确的是
 A、通入 , 反应速率加快 B、曲线b表示 C、时,后反应到达平衡,内 D、其他条件不变,时反应Ⅱ的平衡常数
A、通入 , 反应速率加快 B、曲线b表示 C、时,后反应到达平衡,内 D、其他条件不变,时反应Ⅱ的平衡常数