-
1、C、N、S的氧化物中许多是工业上重要的化工原料,但是当它们分散到空气中时,会带来很多环境问题。下列有关这些元素的氧化物说法不正确的是( )A、开发太阳能、水能、风能、氢能等新能源将有利于减少这些元素的氧化物的产生 B、N与S的某些氧化物能直接危害人的身体健康,引发呼吸道疾病 C、“温室效应”与二氧化碳的排放有着直接的关系 D、这些氧化物使雨水的 , 我们把的雨水称之为酸雨
-
2、下列化学用语不正确的是( )A、的原子结构示意图是:
 B、的电子式是:
B、的电子式是: C、的分子结构模型是:
C、的分子结构模型是: D、的形成过程是:
D、的形成过程是:
-
3、2023年10月1日,天安门广场举行庆祝中华人民共和国成立74周年升旗仪式。下列说法不正确的是( )A、天安门城楼所涂的红色颜料,主要成分为 B、清晨第一缕阳光光芒万丈,该现象为丁达尔效应 C、庆祝节日燃放了五彩的烟花,其色彩来自碱金属及锶、钡等金属元素的焰色 D、国旗杆材料是高碳钢无缝钢管,属于金属材料
-
4、下列古诗文或记载中隐含化学变化且不属于氧化还原反应的是( )A、熬胆矾铁釜,久之亦化为铜 B、爆竹声中一岁除,春风送暖入屠苏 C、凡炉中炽铁用炭,煤炭居十七,木炭居十三 D、千锤万凿出深山,烈火焚烧若等闲
-
5、化合物M(奥司他韦)是目前治疗流感的最常用药物之一,其合成路线如下:

已知:的结构简式为

回答下列问题:
(1)、M中不含氧的官能团的名称是。(2)、有机物C的结构简式为。(3)、E与NaOH溶液共热的化学方程式为。(4)、的核磁共振氢谱有组峰。(5)、G→H的反应类型是。(6)、B有多种同分异构体,同时满足下列条件的同分异构体共有种(不考虑立体异构)。a.分子结构中含有
b.能与溶液发生反应产生气体
(7)、参照上述合成路线,以和 为原料设计合成
为原料设计合成 的路线(其它试剂任选)。
的路线(其它试剂任选)。 -
6、实验室由安息香制备二苯乙二酮的反应式如下:
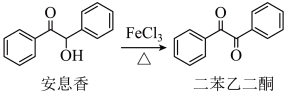
相关信息列表如下:
物质
性状
熔点/℃
沸点/℃
溶解性
安息香
白色固体
133
344
难溶于冷水
溶于热水、乙醇、乙酸
二苯乙二酮
淡黄色固体
95
347
不溶于水
溶于乙醇、苯、乙酸
冰乙酸
无色液体
17
118
与水、乙醇互溶
装置示意图如下图所示,实验步骤为:
①在圆底烧瓶中加入10mL冰乙酸、5mL水及9.0g FeCl3∙6H2O,边搅拌边加热,至固体全部溶解。②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min。
③加入50mL水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g。

回答下列问题:
(1)、仪器A中应加入(填“水”或“油”)作为热传导介质。(2)、仪器B的名称是;冷却水应从(填“a”或“b”)口通入。(3)、实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是。(4)、在本实验中,FeCl3为氧化剂且过量,其还原产物为;某同学尝试改进本实验:采用催化量的FeCl3并通入空气制备二苯乙二酮。该方案是否可行?简述判断理由。(5)、若粗品中混有少量未氧化的安息香,可用少量洗涤的方法除去(填标号)。若要得到更高纯度的产品,可用重结晶的方法进一步提纯。a.热水 b.乙酸 c.冷水 d.乙醇
(6)、本实验的产率最接近于(填标号)。a.85% b.80% c.75% d.70%
-
7、某工厂采用辉铋矿(主要成分为 , 含有、杂质)与软锰矿(主要成分为)联合焙烧法制备和 , 工艺流程如下:

已知:①焙烧时过量的分解为 , 转变为;
②金属活动性:;
③相关金属离子形成氢氧化物的范围如下:
开始沉淀
完全沉淀
6.5
8.3
1.6
2.8
8.1
10.1
回答下列问题:
(1)、为提高焙烧效率,可采取的措施为。a.进一步粉碎矿石
b.鼓入适当过量的空气
c.降低焙烧温度
(2)、在空气中单独焙烧生成 , 反应的化学方程式为。(3)、“酸浸”中过量浓盐酸的作用为:①充分浸出和;②。(4)、滤渣的主要成分为(填化学式)。(5)、生成气体A的离子方程式为。(6)、加入金属的目的是。 -
8、绿水青山就是金山银山。燃烧煤的烟气含有SO2和NOx , 直接排放会造成环境污染,排放前需要进行处理。试回答下列问题:(1)、某实验小组设想利用CO还原SO2。已知S和CO的燃烧热分别是296.0kJ·mol-l、283.0kJ·mol-l , 试写出CO还原SO2生成CO2和S(s)的热化学方程式。(2)、采用Na2SO3溶液吸收法处理SO2 , 25℃时用1mol·L-1的Na2SO3溶液吸收SO2 , 当溶液pH=7时,溶液中各离子浓度的大小关系为。(已知25℃时:H2SO3的电离常数Kal=l.3×10-2 , Ka2=6.2×10-8)(3)、采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在脱硫、脱硝过程中,反应器中一直维持下列条件:温度为298K,pH=12,NaClO2溶液浓度为5×10-3mol·L-1。通入含有SO2和NO的烟气,则反应一段时间后溶液中离子浓度的分析结果如下表。
离子
Cl-
c/(mol·L-1)
8.35×10-4
6.87×10-6
1.5×10-4
l.2×10-5
3.4×10-3
在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压pe如图所示。

①写出NaClO2溶液脱硫过程中主要反应的离子方程式。脱硫、脱硝反应的△H0(填“<”“>”或“=”)。
②已知脱硝主要反应为;4NO+3+4OH-=4+3Cl-+2H2O。由实验结果可知,脱硫反应速率大于脱硝反应速率,原因是除了SO2和NO在烟气中的初始浓度不同,还可能是(写出其中一个原因)。欲提高烟气中NO的脱硝反应速率,可以采用的措施是(写出其中一条措施)。
③脱硝主要反应的平衡表达式为: , 其中pe(NO)为平衡分压。结合题目信息,计算298K时脱硫过程主要反应的化学平衡常数:K=(只列算式代入数据,不作运算)
(4)、如果采用Ca(ClO)2替代NaClO2 , 能得到更好的烟气脱硫效果,其原因是。 -
9、25℃时,PbR(为或的沉淀溶解平衡关系图如图所示。已知 , 下列说法错误的是( )
 A、向X点对应的饱和溶液中加入少量 , 可转化为Y点对应的溶液 B、当和沉淀共存时,溶液中和的比是 C、线b表示 D、Y点溶液是的不饱和溶液
A、向X点对应的饱和溶液中加入少量 , 可转化为Y点对应的溶液 B、当和沉淀共存时,溶液中和的比是 C、线b表示 D、Y点溶液是的不饱和溶液 -
10、利用双极膜电渗析法处理废水,可实现废水的高效净化,其原理如图所示。双极膜是特种离子交换膜,它是由一张阳膜和一张阴膜制成的阴、阳复合膜。在直流电场的作用下,阴、阳膜复合层间的H2O分子解离成H+和OH-并分别通过阳膜和阴膜。下列说法正确的是( )
 A、电极X连接电源的正极,其电极反应式为4OH--4e-=O2↑+2H2O B、Z为淡水,M为H2SO4溶液,b膜为阳离子交换膜 C、理论上,每转移2mol电子,两极共产生1.5mol气体 D、该装置中,电子的转移方向为电极X→电解质溶液→电极Y
A、电极X连接电源的正极,其电极反应式为4OH--4e-=O2↑+2H2O B、Z为淡水,M为H2SO4溶液,b膜为阳离子交换膜 C、理论上,每转移2mol电子,两极共产生1.5mol气体 D、该装置中,电子的转移方向为电极X→电解质溶液→电极Y -
11、下列方案设计、现象和结论都正确的是( )
目的
方案设计
现象和结论
A
检验电解法制备的氯气
电解饱和食盐水,用湿润的碘化钾淀粉试纸检验阴极产生的气体
若试纸变蓝色,则说明有氯气产生
B
验证铁锈中含有二价铁
将铁锈溶于浓盐酸,滴入酸性溶液
若紫色褪去,则说明铁锈中含有二价铁
C
探究和HClO的Ka大小
用pH试纸分别测定浓度均为溶液和NaClO溶液的pH
若 , 则说明
D
探究有机物基团之间的相互影响
取三支试管各加入等量的己烷、苯、甲苯,分别加入几滴等量的酸性溶液(必要时可以稍稍加热),再观察现象
若加入甲苯中的溶液褪色,其他两支试管中的溶液不褪色,则说明苯环对甲基有影响,使甲基更易被氧化
A、A B、B C、C D、D -
12、一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)⇌2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:

已知:气体分压(p分)=气体总压(p总)×体积分数。下列说法错误的是( )
A、该反应△H>0 B、550℃时,充入惰性气体将使v正>v逆 C、650℃时,反应达平衡后CO2的转化率为25.0% D、925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=24.0p总 -
13、某反应分两步进行,其能量变化如图所示。下列说法正确的是( )
 A、反应①的活化能 B、该反应过程中,反应速率由反应②决定 C、总反应的热化学方程式为 D、增大的浓度,可以增大活化分子百分数,提高化学反应速率
A、反应①的活化能 B、该反应过程中,反应速率由反应②决定 C、总反应的热化学方程式为 D、增大的浓度,可以增大活化分子百分数,提高化学反应速率 -
14、下列说法错误的是( )A、在25℃和101kPa时,完全燃烧生成和时放出853kJ的热量,则燃烧热的热化学方程式为: B、在相同条件下,质量相等的两份氢气和足量的氧气充分反应,分别生成液态水(反应①)和水蒸气(反应②),反应①放出的热量多 C、中和反应的反应热测定实验中,需要其中一个反应物稍过量让反应充分进行 D、白铁(镀锌)制品比一般铁器耐腐蚀
-
15、下列叙述正确的是( )A、稀醋酸中加少量醋酸钠能增大醋酸的电离程度 B、25℃时,将盐酸稀释至1000mL,所得溶液的pH为8 C、蔗糖在水中溶解,这是熵增的过程 D、0.1molAgCl和0.1molAgI混合后加入1L水中所得溶液中
-
16、利用下列仪器、装置及药品能达到实验目的的是( )
A
B
C
D




实验室制备
检验乙炔性质
验证牺牲阳极法保护铁
制取乙二酸
A、A B、B C、C D、D -
17、常温下,向0.1mol/LHF溶液中加入少量水,下列各项增大的是( )
①pH②③HF的电离程度④⑤
A、①③⑤ B、①②④ C、①⑤ D、仅有① -
18、下列离子方程式书写正确的是( )A、向溶液中加入稀硫酸: B、大理石与醋酸反应: C、用惰性电极电解溶液: D、用过量苯酚溶液与碳酸钠溶液反应:2


-
19、设为阿伏加德罗常数的值,下列说法正确的是( )A、14g乙烯和丙烯的混合物中π键数目为 B、常温下,的氨水溶液中,发生电离的水分子数为 C、常温下,的醋酸溶液中含有的氢离子数大于 D、相同体积、相同物质的量浓度的溶液和NaCl溶液所含离子数目相同
-
20、化学是材料科学的基础。下列说法错误的是( )A、冬奥会“同心”金属奖牌属于合金材料 B、制造阻燃或防火线缆的橡胶不能由加聚反应合成 C、制造特种防护服的芳纶纤维属于有机高分子材料 D、可降解聚乳酸塑料的推广应用可减少“白色污染”