-
1、下列实验装置设计合理且能达到相应实验目的的是( )


 A、利用甲装置探究的热稳定性 B、利用乙装置制备 C、利用丙装置收集 D、利用丁装置收集
A、利用甲装置探究的热稳定性 B、利用乙装置制备 C、利用丙装置收集 D、利用丁装置收集 -
2、设为阿伏如德罗常数的值,下列说法正确的是( )A、物质的量浓度为1mol/L的溶液中,含个 B、常温常压下,含有个Cl原子 C、标准状况下,所含分子数为 D、中,阴、阳离子总数为
-
3、下列离子方程式不正确的是( )A、FeCl3溶液中加入过量的氨水:Fe3++3NH3•H2O=Fe(OH)3↓+3NH B、FeBr2溶液中通入少量Cl2:2Fe2++Cl2=2Fe3++2Cl- C、醋酸钠溶液中滴入稀硫酸:CH3COONa+H+=CH3COOH+Na+ D、澄清石灰水与过量二氧化碳气体反应:OH-+CO2=HCO
-
4、某混合溶液中所含离子的浓度如表所示,则M可能为( )
离子
M
溶液中离子个数比
2
1
2
1
A、 B、 C、 D、 -
5、下列化学用语或图示表达正确的是( )A、NaCl的电子式为
 B、的VSEPR模型为
B、的VSEPR模型为 C、电子云图为
C、电子云图为 D、基态原子的价层电子轨道表示式为
D、基态原子的价层电子轨道表示式为
-
6、下列有关说法不正确的是( )A、《杨柳歌》中:“独忆飞絮鹅毛下,非复青丝马尾垂”中“飞絮”的主要成分是蛋白质 B、《天工开物》中有“凡石灰经火焚炼为用”,其中涉及的基本反应类型是分解反应 C、《旧唐书》中有“朝坛雾卷,曙岭烟沉”,其中的“雾”是一种胶体,能产生丁达尔效应 D、《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料[主要成分为],保存《千里江山图》需控制温度和湿度
-
7、生活离不开化学,下列九种有机物与人们的生产生活紧密相关
① (防腐剂)② (化工原料)③ (打火机燃料)
④ (冷冻剂)⑤
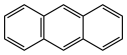 (染料)⑥
(染料)⑥  (化妆品抗酸剂)
(化妆品抗酸剂)⑦
 (定香剂)⑧
(定香剂)⑧ ⑨
⑨  (大豆黄酮)
(大豆黄酮)回答下列问题:
(1)、⑥、⑦中所含官能团的名称分别为、;(2)、与①互为同系物的是(填序号,下同),与③互为同分异构体的是;(3)、⑦的核磁共振氢谱中峰面积之比为;(4)、⑤的分子式为 , 其二氯代物有种;(5)、⑧的系统命名是;(6)、⑨的分子中含有个苯环,分子中碳原子的杂化方式为; -
8、在下列有机物①CH3CH2CH3;②CH3-CH=CH2;③;④
 ;⑤;⑥
;⑤;⑥ ;⑦
;⑦ ;⑧
;⑧ ;⑨
;⑨ , ⑩CH3CH2Cl⑪O2⑫O3⑬
, ⑩CH3CH2Cl⑪O2⑫O3⑬ ⑭
⑭ 中, (1)、属于芳香烃的是 , 互为同系物的是 , 互为同分异构体的是 , 互为同素异形体的是 , 属于同一种物质的是。(填写序号)(2)、写出有机物
中, (1)、属于芳香烃的是 , 互为同系物的是 , 互为同分异构体的是 , 互为同素异形体的是 , 属于同一种物质的是。(填写序号)(2)、写出有机物 的系统命名。 (3)、按系统命名法,
的系统命名。 (3)、按系统命名法, 的名称是。 (4)、
的名称是。 (4)、 中含有的官能团的名称为。 (5)、2,3—二甲基—4—乙基己烷(写结构简式)。(6)、支链上只有一个乙基,且式量最小的烷烃(写结构简式)。
中含有的官能团的名称为。 (5)、2,3—二甲基—4—乙基己烷(写结构简式)。(6)、支链上只有一个乙基,且式量最小的烷烃(写结构简式)。 -
9、(1)、根据核磁共振氢谱图可以确定有机物分子中氢原子的种类和数目。例如:乙醚的结构式为
 , 其核磁共振氢谱中有2个信号(如下图)。
, 其核磁共振氢谱中有2个信号(如下图)。
①下列分子中,其核磁共振氢谱中只有一种峰(信号)的物质是(填字母)。
A.CH3-CH3 B.CH3COOH C.CH3COOCH3 D.CH3COCH3
②化合物A和B的分子式都是C2H4Br2 , A的核磁共振氢谱如下图所示,则A的结构简式为 , 请预测B的核磁共振氢谱上有个峰(信号)。

③用核磁共振氢谱的方法来研究C2H6O的结构,请简要说明根据核磁共振氢谱的结果来确定C2H6O分子结构的方法是。
(2)、有机物C常用于食品行业。已知9.0gC在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2。①C分子的质谱图如图所示,从图中可知其相对分子质量是 , 则C的分子式是。

②C能与NaHCO3溶液发生反应,C一定含有的官能团名称是。
③C分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则C的结构简式是。
-
10、I.有机物M(只含C、H、O三种元素中的两种或三种)具有令人愉悦的牛奶香气,主要用于配制奶油、乳品、酸奶和草莓等型香精,是我国批准使用的香料产品,其沸点为。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:
步骤一:将粗品用蒸馏法进行纯化。
(1)、如图1所示,仪器a的名称是 , 图中虚线框内应选用右侧的(填“仪器x”或“仪器y”)。 (2)、步骤二:确定M的实验式和分子式。
(2)、步骤二:确定M的实验式和分子式。利用元素分析仪测得有机物M中碳的质量分数为54.5%,氢的质量分数为9.1%。
①M的实验式为。
②已知M的密度是同温同压下密度的2倍,则M的分子式为。
(3)、步骤三:确定M的结构简式。用核磁共振仪测出M的核磁共振氢谱如图2所示,图中峰面积之比为;利用红外光谱仪测得M的红外光谱如图3所示。

M中官能团的名称为 , M的结构简式为(填键线式)。
Ⅱ.按要求回答下列问题:
① ② ③ ④
 ⑤
⑤ ⑥
⑥ ⑦
⑦ (4)、其中,属于同系物的是;属于同分异构体的是;属于同种物质的是。
(4)、其中,属于同系物的是;属于同分异构体的是;属于同种物质的是。A.①② B.②③ C.③④⑤⑥⑦ D.①③ E.③④⑤⑦ F.④⑥
(5)、分子式为的同分异构体共有____(不考虑立体异构)A、6种 B、7种 C、8种 D、9种 -
11、A的结构简式为
 , 有关该有机物的说法正确的是( ) A、三个碳原子位于同一直线 B、二氯代物有2种 C、所有原子可能位于同一平面 D、与其互为同分异构体的化合物有3种
, 有关该有机物的说法正确的是( ) A、三个碳原子位于同一直线 B、二氯代物有2种 C、所有原子可能位于同一平面 D、与其互为同分异构体的化合物有3种 -
12、葡酚酮是从葡萄籽中提取的一种花青素类衍生物(结构简式如图),葡酚酮分子中含有手性碳原子(连有四个不同原子或基团的碳原子)的个数为( )
 A、2 B、3 C、4 D、5
A、2 B、3 C、4 D、5 -
13、有机物Q(只含C、H、O的球棍模如图所示。不同大小、颜色的小球代表不同的原子,小球之间的“棍”表示共价键,既可以表示三键,也可以表示双键,还可以表示单键。下列有关Q的推断错误的是( )
 A、Q的分子式为 B、Q与足量氢气加成产物的环上一氯代物有7种 C、Q能与溶液反应放出 D、一个Q分子中有11个碳原子一定共面
A、Q的分子式为 B、Q与足量氢气加成产物的环上一氯代物有7种 C、Q能与溶液反应放出 D、一个Q分子中有11个碳原子一定共面 -
14、下列有关
 的说法正确的是( ) A、该有机物的分子式为 B、能发生水解反应 C、该物质的所有碳原子可能共平面 D、该物质含有的含氧官能团为醚键、酯基、羟基、碳碳双键
的说法正确的是( ) A、该有机物的分子式为 B、能发生水解反应 C、该物质的所有碳原子可能共平面 D、该物质含有的含氧官能团为醚键、酯基、羟基、碳碳双键 -
15、下列说法正确的是( )A、环戊二烯(
 )分子中最多有9个原子在同一平面上
B、月桂烯(
)分子中最多有9个原子在同一平面上
B、月桂烯( )所有碳原子一定在同一平面上
C、的分子中,有4个甲基的同分异构体有3种(不考虑立体异构)
D、芳香族化合物A与
)所有碳原子一定在同一平面上
C、的分子中,有4个甲基的同分异构体有3种(不考虑立体异构)
D、芳香族化合物A与 互为同分异构体,A苯环上的一氯代物只有一种结构,则A可能的结构有5种
互为同分异构体,A苯环上的一氯代物只有一种结构,则A可能的结构有5种
-
16、下列关于有机物的说法不正确的是( )A、2-丁烯分子存在顺反异构 B、对三联苯(
 )的一氯代物有5种
C、每个抗坏血酸分子(
)的一氯代物有5种
C、每个抗坏血酸分子( )中有2个手性碳原子
D、立方烷(
)中有2个手性碳原子
D、立方烷( )经硝化可得到六硝基立方烷,其可能的结构有3种
)经硝化可得到六硝基立方烷,其可能的结构有3种
-
17、冠醚由于形似“王冠”而得名。如;(1)
 和(2)
和(2) 。下列关于冠醚的说法正确的是( ) A、冠醚属于烃类 B、(2)与葡萄糖互为同分异构体 C、冠醚能完全燃烧生成和 D、(1)和(2)互为同系物
。下列关于冠醚的说法正确的是( ) A、冠醚属于烃类 B、(2)与葡萄糖互为同分异构体 C、冠醚能完全燃烧生成和 D、(1)和(2)互为同系物 -
18、某研究人员找到了一种比二氧化碳有效倍的“超级温室气体”——全氟丙烷()。下列有关全氟丙烷的说法不正确的是( )A、分子中三个碳原子不可能处于同一直线上 B、全氟丙烷属于烃的衍生物 C、全氟丙烷的电子式为
 D、全氟丙烷分子中既有极性键又有非极性键
D、全氟丙烷分子中既有极性键又有非极性键
-
19、下列物质一定互为同系物的是( )
①
 ②
② ③
③ ④⑤⑥⑦
④⑤⑥⑦ ⑧
⑧ A、④和⑧ B、①、②和③ C、⑤、⑦和⑧ D、⑥和⑧
A、④和⑧ B、①、②和③ C、⑤、⑦和⑧ D、⑥和⑧ -
20、能够测定有机物分子结构和化学键的方法是( )
①质谱法②红外光谱法③元素分析法④核磁共振氢谱法
A、①② B、③④ C、② D、①④