-
1、豆腐是我国具有悠久历史的传统美食,它是利用盐卤等物质能使豆浆中的蛋白质聚沉的原理制成的。盐卤中含有的氯化镁、硫酸钙等都是制作豆腐常用的凝聚剂,下列说法正确的是( )A、最高正化合价: B、中中心原子的杂化方式为 C、基态Cl原子核外电子的运动状态有9种 D、为既含有离子键又含有共价键的离子化合物
-
2、回答下列问题(1)、向某体积固定的密闭容器中加入和三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。请回答:

①该密闭容器的体积为升;若 , 则内用表示反应速率;
②写出该反应的化学方程式:。
③能使该反应的速率增大的是。
A.及时分离出C气体 B.适当升高温度
C.充入He气增大压强 D.选择高效催化剂
④下列物质表示该反应的化学反应速率最快的是。
A.
B.
C.
(2)、已知断裂几种化学键要吸收的能量如下:化学键
断裂键吸收的能量
415
497
745
463
已知的结构式分别为 , , 。在中完全燃烧生成气态和气态水时放出热量。
(3)、燃料电池是一种高效、环境友好的供电装置,如图为氢气燃料电池的工作原理示意图,均为惰性电极。
①使用时,氢气从口通入(填“”或“B”)
②极的电极反应为:。
-
3、我国近代化学工业英基人侯德榜先生设计出“侯氏制碱法”,提高了食盐的转化率,缩短了生产流程,减少了对环境的污染。钢仁一中化学实验社团模拟“侯氏制碱法”开展如下项目式学习:
项目一:粗盐的提纯
粗盐中除了含有泥沙之外,还含有少量等杂质离子,粗盐提纯的流程如图所示:
 (1)、试剂分别为足量的、。(2)、操作2的名称是。(3)、“滤液”中加入足量的试剂生成气泡的离子方程式为。(4)、项目二:模拟“侯氏制碱法“利用上述实验制得的全部用于制备纯碱,工艺流程如图所示:
(1)、试剂分别为足量的、。(2)、操作2的名称是。(3)、“滤液”中加入足量的试剂生成气泡的离子方程式为。(4)、项目二:模拟“侯氏制碱法“利用上述实验制得的全部用于制备纯碱,工艺流程如图所示:
氮化和碳酸化过程在如图所示装置中进行,导管应通入的气体是(填化学式),仪器的作用是。
(5)、写出煅烧固体时发生的化学方程式:。(6)、称取了粗盐进行实验,最终制得纯碱,假设完全转化,则粗盐的纯度是。(保留2位有效数字) -
4、铜仁一中某化学兴趣小组为了探究铜与浓硫酸的反应以及产物的性质,设计了如图所示装置进行实验。回答下列问题:
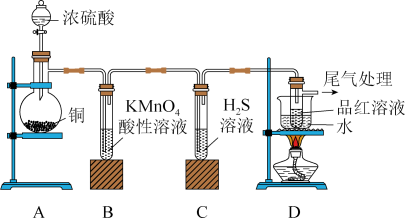 (1)、若要使装置A中反应发生还缺少的实验仪器是 , 写出装置中发生反应的化学反应方程式。(2)、装置中现象变化是。(3)、装置中发生反应的化学方程式是。(4)、装置中酒精灯的作用是。
(1)、若要使装置A中反应发生还缺少的实验仪器是 , 写出装置中发生反应的化学反应方程式。(2)、装置中现象变化是。(3)、装置中发生反应的化学方程式是。(4)、装置中酒精灯的作用是。另一个实验小组的同学认为和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的和按同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)。
(5)、尾气可采用溶液吸收。 -
5、四种易溶于水的化合物只由表中的八种离子组成,且四种化合物中阴、阳离子各不相同。
阴离子
阳离子
已知:A溶液呈强酸性,且A溶液与溶液混合均产生白色沉淀,的焰色反应呈黄色。
回答下列问题:
(1)、写出C的化学式: , 的电子式:。(2)、写出A溶液与溶液反应的离子方程式:。(3)、A中阴离子的检验操作。(4)、请选出适合存放溶液的试剂瓶的序号:
溶液
A
C
试剂瓶序号
-
6、某溶液含有下列离子中的几种: , 取该溶液进行如下实验
取该溶液与足量溶液共热产生刺激性气体
另取该溶液加入稀无明显现象,再加足量溶液得到白色沉淀
取(2)的上层清液加入溶液和稀硝酸得到白色沉淀
下列结论正确的是( )
A、一定含 , 一定不含 B、一定含 , 一定不含 C、一定含 , 可能含 D、一定含 , 可能含 -
7、由二氧化硅制高纯硅的流程如下,下列说法中错误的是( )
 A、①②③均属于氧化还原反应 B、H2和HCl均可循环利用 C、SiO2是一种坚硬难熔的固体,熔沸点都很高 D、X为CO2
A、①②③均属于氧化还原反应 B、H2和HCl均可循环利用 C、SiO2是一种坚硬难熔的固体,熔沸点都很高 D、X为CO2 -
8、下列实验操作正确的是( )A、
 B、
B、 C、
C、 D、
D、
-
9、科学研究人员提出在有机碳源和微生物的作用下,可以实现大气中的氮循环(如图所示),减少对环境的污染。下列说法正确的是( )
 A、转化成属于氮的固定 B、温度越高,越有利于转化为 C、转化过程中被氧化为 D、转化为过程中每消耗33.6L(标准状况下)则有1mol 生成
A、转化成属于氮的固定 B、温度越高,越有利于转化为 C、转化过程中被氧化为 D、转化为过程中每消耗33.6L(标准状况下)则有1mol 生成 -
10、如图,锥形瓶内盛有气体 , 滴管内盛有液体。若挤压胶头滴管,使液体滴入瓶中,振荡,过一会可见小气球鼓起。气体和液体不可能是( )
 A、是 , 是水溶液 B、是 , 是饱和溶液 C、是 , 是溶液 D、是 , 是溶液
A、是 , 是水溶液 B、是 , 是饱和溶液 C、是 , 是溶液 D、是 , 是溶液 -
11、如图是锌-铜原电池的示意图,下列说法错误的是( )
 A、作原电池的负极 B、电极上有气泡冒出 C、溶液中的向电极方向移动 D、每生成就有电子从经导线流向再经溶液流回
A、作原电池的负极 B、电极上有气泡冒出 C、溶液中的向电极方向移动 D、每生成就有电子从经导线流向再经溶液流回 -
12、X(g)+3Y(g)2Z(g) △H=-a kJ/mol(a>0)。一定条件下,将1 molX和3molY通入2L的恒容密闭容器,反应10 min,测得Y的物质的量为2.4 mol。下列说法正确的是( )A、10min内,Y的平均反应速率为0.03 mol/(L·s) B、10 min内,消耗0.2 molX,生成0.4 molZ C、第10 min时,X的反应速率为0.01 mol/(L·min) D、10min内,X和Y反应吸收的热量为0.2a kJ
-
13、能正确表示下列反应的方程式的是( )A、向澄清的石灰水中通入气体: B、单质硅溶于烧碱溶液中: C、的催化氧化反应: D、向氢硫酸中通入氯气:
-
14、是一种重要的化工原料,也是人类制备各种含氮化合物的基础原料。下列有关的描述中正确的是( )A、氨气与浓硫酸相遇会产生大量白烟 B、氨水能导电,所以氨水是一种常见的电解质 C、液氨汽化时会吸收大量的热,故液氨常用作制冷剂 D、检查输送氨气的管道是否漏气,可用湿润的蓝色石蕊试纸检验,若试纸变红则漏气
-
15、如图所示各图中,表示化学反应:能量变化的是( )A、
 B、
B、 C、
C、 D、
D、
-
16、下列关于硫及其化合物叙述正确的是( )A、硫单质在空气中燃烧可生成 B、空气中排放过量会形成酸雨,酸雨是指的雨水 C、足量铜粉与稀溶液反应,可生成标准状况下为 D、将浓硫酸加入滴有几滴水的蔗糖中,蔗糖逐渐变黑形成“黑面包”,产生有刺激性气体,体现浓硫酸的脱水性和强氧化性
-
17、化学与生活、生产密切相关,下列说法正确的是( )A、食物放进冰箱里可以减缓食物变质速率 B、面团加酵母粉后放在温度越高的地方发酵越快 C、石英玻璃、碳化硅陶瓷、水泥、石墨烯都是硅酸盐材料 D、半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅
-
18、利用金属矿渣(含有FeS2、SiO2及Cu2O)制备FeCO3的实验流程如下。已知煅烧过程中FeS2和Cu2O转化为Fe2O3和CuO。
 (1)、滤渣1的主要成分为:(写化学式),该物质是工业制备高纯度硅的原料,写出硅与氯化氢在高温条件下发生的化学方程式:。(2)、FeS2在空气中煅烧的化学方程式为。(3)、在“还原”步骤,在向酸浸后溶液加入过量铁屑,除了能将转化为外,还能。若将6 g铁粉加入200 mL 和CuSO4的混合溶液中,充分反应得到200 mL FeSO4溶液和5.2 g固体沉淀物。
(1)、滤渣1的主要成分为:(写化学式),该物质是工业制备高纯度硅的原料,写出硅与氯化氢在高温条件下发生的化学方程式:。(2)、FeS2在空气中煅烧的化学方程式为。(3)、在“还原”步骤,在向酸浸后溶液加入过量铁屑,除了能将转化为外,还能。若将6 g铁粉加入200 mL 和CuSO4的混合溶液中,充分反应得到200 mL FeSO4溶液和5.2 g固体沉淀物。①5.2 g固体沉淀物的成分为(写化学式)。
②原溶液的物质的量浓度是。
(4)、检验是否完全被还原的实验操作是。(5)、制备FeCO3 , 写出“沉铁”步骤发生反应的离子方程式:。 -
19、二氧化硫是最常见、最简单、有刺激性的硫氧化物,大气主要污染物之一,火山爆发时会喷出该气体,在许多工业过程中也会产生二氧化硫。在生活、生产中有重要用途,使用不当会造成环境污染。(1)、某同学利用如图所示装置研究二氧化硫的性质。

①仪器b的名称为 , 加入药品前需要进行的操作是:。
②装有Na2S溶液的球形干燥管中出现淡黄色浑浊,说明二氧化硫具有性,写出发生反应的化学方程式。
③装置c中的溶液(填能或不能)用澄清石灰水替换,理由是。
(2)、某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。
当注入标准状况下200mL空气时,酸性溶液恰好褪色,停止实验。发生反应的离子方程式为:。该空气中二氧化硫的体积分数为。
-
20、(1)、I.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
比较时刻,正逆反应速率大小。(填“>”“=”或“<”) (2)、若 , 计算反应开始至时刻用M的浓度变化表示的平均反应速率。(3)、时刻化学反应达到平衡,反应物的转化率为。(4)、如果升高温度,则(填“增大”“减小”或“不变”)。(5)、II.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
(2)、若 , 计算反应开始至时刻用M的浓度变化表示的平均反应速率。(3)、时刻化学反应达到平衡,反应物的转化率为。(4)、如果升高温度,则(填“增大”“减小”或“不变”)。(5)、II.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:序号
纯锌粉/g
硫酸溶液/mL
温度/℃
硫酸铜固体/g
加入蒸馏水/mL
Ⅰ
2.0
50.0
25
0
0
Ⅱ
2.0
40.0
25
0
10.0
Ⅲ
2.0
50.0
25
0.2
0
Ⅳ
2.0
50.0
25
4.0
0
①本实验待测数据可以是 , 实验Ⅰ和实验Ⅱ可以探究对锌与稀硫酸反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是 。
(6)、Ⅲ.氢气燃料电池在北京冬奥会上得到广泛应用,下图是一种氢气燃料电池的工作原理示意图:
b电极的电极反应式为 , a电极若该极改为通入 , 其电极反应式为。