-
1、短周期X、Y、Z、M、W五种主族元素,其原子半径、简单氢化物的进点分别随原子序数变化的关系如下图所示,常温时,测得、、简单氢化物的水溶液分别为11、4、1。下列说法正确的是( )
 A、的最高价氧化物的空间填充模型为
A、的最高价氧化物的空间填充模型为 B、X、Y、Z的第一电离能:
C、M、W简单离子对水的电离平衡都无影响
D、M、W最高价氧化物的水化物的酸性;
B、X、Y、Z的第一电离能:
C、M、W简单离子对水的电离平衡都无影响
D、M、W最高价氧化物的水化物的酸性;
-
2、下列实验探究方案能达到探究目的的是( )
选项
探究方案
A
向溶液中加入少量固体,振荡,溶液由蓝色变为黄绿色
中的配位键稳定性大于中的配位键
B
向溶液中滴加淀粉溶液,再通入气体,观察现象
比较与氧化性的强弱
C
向和的混合溶液中,滴加12滴溶液,观察沉淀颜色
D
向2支分别盛有不同浓度溶液的试管中,同时加入溶液
探究反应物㳖度对反应速率的影响
A、A B、B C、C D、D -
3、为阿伏加德罗常数的值。我国化学家侯德榜改进国外的纯碱生产工艺,提高了原料利用率。其主要原理为。下列说法正确的是( )A、完全分解,产生气体的分子数目为 B、分子所含价层电子对的数目为3 C、含的和的混合物中,质子总数为28 D、标准状况下含键的数目为0.2
-
4、BAS是一种可定向运动的“分子机器”,其合成路线如下。下列说法正确的是( )
 A、M的分子式为 B、M既能与酸反应又能与碱反应 C、M、BAS均有一个手性碳原子 D、BAS苯环上的一溴代物共有8种
A、M的分子式为 B、M既能与酸反应又能与碱反应 C、M、BAS均有一个手性碳原子 D、BAS苯环上的一溴代物共有8种 -
5、现代高分子材料正向功能化、智能化、精细化方向发展,与各领域的需求密切相关,下列有关高分子的说法错误的是( )A、有“塑料王”之称的聚四氟乙烯是通过四氟乙烯发生加聚反应制得的 B、利用高分子分离膜进行海水淡化,比蒸馏法耗能少 C、制造阻燃或防火线缆的橡胶是通过加聚反应制得的线型结构的合成材料 D、应用于轻型飞机、消防服的芳纶“1414”的数字指单体对苯二胺和对苯二甲酸的官能团在苯环的位置
-
6、科学技术迅速发展,离不开化学知识,下列说法正确的是( )A、“朱雀二号”遥二成为全球首枚成功入轨的液氧甲烷运载火箭,液氧和甲烷作助燃剂 B、“神舟十七号”发动机的耐高温结构材料是一种熔沸点很高的分子晶体 C、火星直升机制造过程中使用的1500多块碳纤维结构件属于无机非金属单质 D、人造卫星和深空探测器强度要求高的零部件采用钛合金或不锈钢等合金材料
-
7、阿立哌唑对精神分裂症的阳性和阴性症状均有明显疗效,G是合成阿立哌唑的中间体,其合成路线如下:

已知:i.
 ;ii.
;ii. 。
。回答下列问题:
(1)、B的分子式为 , C→D的反应类型为。(2)、E的结构简式为;D→E反应的另一种产物为。(3)、F→G反应中,有机副产物的结构简式是。(4)、写出F与过量NaOH水溶液反应的化学方程式:。(5)、F的同分异构体中同时满足下列条件的有种(不考虑立体异构),其中核磁共振氢谱有5组吸收峰,且峰面积比为1:2:2:2:2的化合物的结构简式为。i.除苯环外无其他环状结构,只有1种含氧官能团,可以与银氨溶液反应,生成单质银;
ii.苯环上有两个取代基,且氨基直接与苯环相连。
(6)、参照上述合成路线,以 和为原料,设计制备
和为原料,设计制备 的合成路线:(无机原料及有机溶剂任用)。
的合成路线:(无机原料及有机溶剂任用)。 -
8、二甲醚(DME)作为一种新兴的基本有机化工原料,在制药、燃料、农药等化学工业中有许多独特的用途,其制备方法有CO氢化法、氢化法、电化法等。回答下列问题:(1)、CO氢化法所涉及的反应如下:
反应i. ;
反应ii. ;
反应iii. 。
①反应iv。 , 利于该反应正向进行的条件是(填“高温”“低温”或“任意温度”)。
②将和充入密闭容器中仅发生反应iv,平衡体系中的物质的量分数与压强和温度的关系如图所示,关于温度和压强的关系判断正确的是(填字母)。

A. , B. ,
C. , D. ,
(2)、在某温度及压强为pMPa条件下,在密闭容器中按物质的量之比1:2充入、 , 发生反应 , 平衡时的转化率为50%。①达平衡时,MPa。
②该温度下,平衡常数 MPa-4(以平衡分压代替平衡浓度计算,分压=总压物质的量分数)。
(3)、氢化法反应原理为反应v。 。在一定压强、和的起始投料一定的条件下,发生反应iii、反应v,实验测得平衡转化率和平衡时的选择性随温度的变化如图所示。
①的选择性 , 其中表示平衡时的选择性的是曲线(填“x”或“y”)。
②温度高于300℃时,曲线y随温度升高而升高的原因是。
③为同时提高的平衡转化率和平衡时的选择性,应选择的反应条件为(填字母)。
a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
(4)、电化法工作原理如图所示:阴极电极反应式为 , 电解过程中右池溶液的质量(填“增大”“减少”或“不变”)。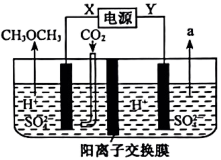
-
9、某工厂废渣的主要成分为ZnO、PbO、、CuO、等(与性质相似),以该工厂废渣为主要原料回收其中金属元素的工艺流程如图所示:

回答下列问题:
(1)、“焙烧”产生的气体是(填分子式),该气体的用途是(填一条),若发生反应,则转移(Bi元素转化为)。(2)、“氨浸”所得滤液1中的阳离子主要成分为、 , 该步骤温度不宜过高,其原因是 , “沉铜”时发生反应的离子方程式为。(3)、“滤渣4”的主要成分为(填化学式)。(4)、“滤液3”的主要溶质为 , 以惰性电极电解该滤液可以回收单质Ga,电解时阴极主要电极反应式为。(5)、“转化”时生成的同时放出能使澄清石灰水变浑浊的气体,该步骤的化学方程式为。(6)、铁酸铋具有铁电性和反铁磁性,其晶胞结构如图所示,晶胞参数为apm。
①基态O原子的核外电子排布式为。
②该晶体的密度=(为阿伏加德罗常数的值)。
-
10、氨基钠可用作有机合成的还原剂、脱水剂等。已知,i.几乎不溶于液氨,易与水、氧气等反应;ii.、、。回答下列问题:
I.制备氨基钠
 (1)、按气流从左往右的方向,上述装置合理的连接顺序为(填仪器接口字母,必要时个别装置可重复使用)。(2)、仪器x的名称为 , 装置A的作用为。(3)、装置B中制备的化学方程式为。(4)、的作用是 , 若装置D中生成1.12L(标准状况下) , 则消耗gNa。(5)、反应前装置D中需通入氨气排尽体系中空气,设计方案判断密闭体系中空气是否排尽:。(6)、II.氨基钠产品质量分数测定
(1)、按气流从左往右的方向,上述装置合理的连接顺序为(填仪器接口字母,必要时个别装置可重复使用)。(2)、仪器x的名称为 , 装置A的作用为。(3)、装置B中制备的化学方程式为。(4)、的作用是 , 若装置D中生成1.12L(标准状况下) , 则消耗gNa。(5)、反应前装置D中需通入氨气排尽体系中空气,设计方案判断密闭体系中空气是否排尽:。(6)、II.氨基钠产品质量分数测定称量2.0g氨基钠产品,溶于水配成500mL溶液;量取25mL溶液,加热除去 , 冷却至室温后,滴入2滴酚酞试液,用的HCl标准溶液进行滴定,记下达到滴定终点所消耗HCl标准溶液的体积,重复上述实验4次,滴定结果如下表。
实验数据
滴定次数
1
2
3
4
V(产品)/mL
25.00
25.00
25.00
25.00
V[HCl(标准溶液)]/mL
25.75
25.00
25.05
24.95
氨基钠的质量分数为%(保留三位有效数字)。
-
11、25℃条件下,改变亚碲酸[开始时,]溶液的pH,溶液中、、、的物质的量分数随pH的变化如图所示[已知]。下列说法错误的是( )
 A、 B、的平衡常数 C、时, D、溶液中:
A、 B、的平衡常数 C、时, D、溶液中: -
12、砷化镓是重要的半导体材料,用于制作微波集成电路、红外线发光二极管等元件,砷化镓立方晶胞结构如图所示,晶胞参数为apm。下列说法正确的是( )
 A、每个Ga周围距离最近的Ga原子个数为8 B、Ga原子与As原子的最短距离为 C、该晶胞的质量为(为阿伏加德罗常数的值) D、一个晶胞中含有4个As原子和14个Ga原子
A、每个Ga周围距离最近的Ga原子个数为8 B、Ga原子与As原子的最短距离为 C、该晶胞的质量为(为阿伏加德罗常数的值) D、一个晶胞中含有4个As原子和14个Ga原子 -
13、已知反应i. , 平衡常数;
ii. , 平衡常数;
iii. , 平衡常数 , 各反应的平衡常数的对数值随温度变化如图所示。下列说法正确的是( )
 A、反应i的 , 反应iii的 B、反应的 C、tK时,若反应ii中 , 则一定有 D、在恒容密闭容器中充入和进行反应iii,三点压强
A、反应i的 , 反应iii的 B、反应的 C、tK时,若反应ii中 , 则一定有 D、在恒容密闭容器中充入和进行反应iii,三点压强 -
14、一种捕获并将其转化为的反应历程如图所示。

下列说法正确的是( )
A、所有中间产物中均存在配位键 B、反应过程中N元素的化合价没变 C、 为催化剂
D、反应过程中存在非极性键的断裂和形成
为催化剂
D、反应过程中存在非极性键的断裂和形成
-
15、我国西沙群岛软珊瑚中存在多种朵蕾烷二萜类天然产物,结构如图所示,它们具有较强抗菌、抗肿瘤等生物活性。下列关于该二萜类化合物说法错误的是( )
 A、化合物I不属于芳香族化合物 B、化合物II能使的溶液褪色 C、化合物III不能发生水解反应 D、等物质的量的化合物I、II、III最多消耗的物质的量之比为2:2:3
A、化合物I不属于芳香族化合物 B、化合物II能使的溶液褪色 C、化合物III不能发生水解反应 D、等物质的量的化合物I、II、III最多消耗的物质的量之比为2:2:3 -
16、一种以钌矿石[主要含 , 还含少量的FeO、MgO、、CaO、]为原料制备钌(Ru)的工艺流程如图。

下列说法错误的是( )
A、“除镁”的离子方程式为 B、若“灼烧”时生成33.6L(标准状况下) , 则转移的电子数为 C、“酸浸”时,的作用是做还原剂,还原 D、从“滤液2”中可提取一种化肥,其电子式为
-
17、有机物M的结构简式如图所示。下列说法正确的是( )
 A、M的分子式为 B、M中含有三种官能团 C、1molM最多与5molH反应 D、M苯环上的二氯代物有6种(不考虑立体异构)
A、M的分子式为 B、M中含有三种官能团 C、1molM最多与5molH反应 D、M苯环上的二氯代物有6种(不考虑立体异构) -
18、锂电池中某阻燃剂的结构式如图所示,其中Y、Z、Q、W是原子序数依次增大的短周期主族元素,基态W原子核外能量不同的电子有3种,下列说法正确的是( )
 A、电负性: B、基态原子未成对电子数: C、原子半径: D、该化合物中各原子的最外层均满足8电子稳定结构
A、电负性: B、基态原子未成对电子数: C、原子半径: D、该化合物中各原子的最外层均满足8电子稳定结构 -
19、同时作为燃料和氧化剂的直接过氧化氢燃料电池(DPPFC)的工作原理如图所示(电解过程中溶液中溶质的种类不变且其质量减轻)。下列有关说法错误的是( )
 A、石墨1为负极,发生氧化反应 B、石墨2的电极反应式为 C、离子交换膜1、2分别为阴、阳离子交换膜 D、当外电路中转移时,溶液的质量减轻52.2g
A、石墨1为负极,发生氧化反应 B、石墨2的电极反应式为 C、离子交换膜1、2分别为阴、阳离子交换膜 D、当外电路中转移时,溶液的质量减轻52.2g -
20、下列实验操作、现象及得出的结论均正确的是( )
选项
实验操作、现象
实验结论
A
的溶液与的溶液等体积混合,产生白色沉淀
结合能力:
B
将补铁口服液(含维生素C)滴入酸性溶液,紫红色褪去
补铁口服液中含有
C
将久置的加入稀盐酸中,产生气泡
已经变质
D
取两份新制氯水,分别滴加溶液和淀粉-KI溶液,前者有白色沉淀,后者溶液变蓝
氯气与水的反应存在限度
A、A B、B C、C D、D