-
1、通过有机分子a可组装高度有序的聚电解质薄膜b,该薄膜具有精确可调谐的层间距和高效的离子传输。下列说法错误的是( )

 A、有机分子a中参与sp3杂化和sp2杂化的C原子数目之比为4:1 B、有机分子a中存在离子键和共价键 C、聚电解质薄膜b中相邻的有机分子a之间存在氢键 D、离子在聚电解质薄膜b中依靠正、负电荷间的静电作用传输
A、有机分子a中参与sp3杂化和sp2杂化的C原子数目之比为4:1 B、有机分子a中存在离子键和共价键 C、聚电解质薄膜b中相邻的有机分子a之间存在氢键 D、离子在聚电解质薄膜b中依靠正、负电荷间的静电作用传输 -
2、下列实验操作能达到实验目的的是( )
选项
实验目的
实验操作
A
比较Cu和Ag的金属性
将银棒和铜棒分别插入AgNO3溶液与CuSO4溶液中,并用盐桥和导线(含电流表)将二者连接组成原电池
B
验证KI溶液与FeCl3溶液之间的反应为可逆反应
取2mL0.1mol/LKI溶液,加入5~6滴FeCl3溶液充分反应,再滴入2滴淀粉溶液
C
证明苯能与液溴发生取代反应
将苯与液溴反应生成的气体直接通入AgNO3溶液中
D
证明Kh(CuSO4)随温度升高而增大
用pH计分别测量40℃和70℃时0.1mol/LCuSO溶液的pH
A、A B、B C、C D、D -
3、短周期主族元素X、Y、Z、W、M和Q的原子序数依次增大,其构成一种化合物的结构如图所示。下列说法正确的是( )
 A、上述元素均位于元素周期表的p区 B、简单氢化物的沸点:Q>W>Y C、Z的最高价氧化物的水化物可与Q的氢化物反应生成固体单质 D、简单离子半径:M>W>Z
A、上述元素均位于元素周期表的p区 B、简单氢化物的沸点:Q>W>Y C、Z的最高价氧化物的水化物可与Q的氢化物反应生成固体单质 D、简单离子半径:M>W>Z -
4、设NA为阿伏加德罗常数的值,下列说法正确的是( )A、标准状况下,11.2LCH3CHO中含有π键的数目为0.5NA B、1mol基态Ni原子中含有未成对电子数为3NA C、100mL8mol/L浓硝酸与6.4g的Cu完全反应转移的电子数目为0.2NA D、工业合成氨的反应通入14gN2和14gH2充分反应后生成NH分子的数目为NA
-
5、有机物M在一定条件下可以转化为N,下列说法正确的是( )
 A、M能与NaOH溶液发生反应 B、可利用溴水鉴别M和N C、N分子中含有1个手性碳原子 D、含2个甲基和2个醛基的N的同分异构体有4种
A、M能与NaOH溶液发生反应 B、可利用溴水鉴别M和N C、N分子中含有1个手性碳原子 D、含2个甲基和2个醛基的N的同分异构体有4种 -
6、下列关于分子结构和性质的说法正确的是( )A、H2O2和S2Cl2均为极性分子 B、Cl2O分子的键角比SCl2分子的键角小 C、BF3和NF3的VSEPR模型和分子空间构型均相同 D、C2H6和C2H4分子中形成C-Hσ键原子轨道的重叠方式相同
-
7、下列实验室药品的保存或实验安全应急措施错误的是( )A、漂白粉要避光、密封保存在阴凉处 B、浓溴水沾在皮肤上,先用大量水冲洗,再用酒精擦拭 C、AgNO3溶液应当保存在棕色细口瓶中 D、浓硫酸沾到皮肤上,先用大量水冲洗,然后涂抹稀NaOH溶液
-
8、开元寺铁佛像是世界上现存的最大古代铁佛像,开元大佛为中空铸铁件,外有泥塑涂层和贴金饰层。下列说法正确的是( )A、佛像腰部以上部位表面多呈红棕色,其主要成分为Fe3O4 B、泥塑涂层由黏土烧制而成,泥塑涂层属于硅酸盐材料 C、佛像贴金饰层所用材料为黄金金箔,金箔的制作过程属于化学变化 D、佛像中空铸铁件所用材料为生铁,生铁的含碳量比钢的含碳量低
-
9、有机物J是合成一种具有生物活性物质的中间体,其合成路线如下所示:

请回答下列问题:
(1)、I的含氧官能团名称为;J的分子式为;B的结构简式为。(2)、的名称为。(3)、写出F→G的化学反应方程式:。(4)、G→H的反应类型为。(5)、设置D→E及I→J的反应步骤的目的是。(6)、K比D的分子组成只少1个碳原子,符合下列条件的K的结构有种。(7)、ⅰ.苯环上有两个取代基;ⅱ.遇溶液显色,且能与溶液反应放出。
参照上述合成路线,以
 和
和 为原料,设计合成
为原料,设计合成 的路线:(无机试剂任选)。
的路线:(无机试剂任选)。 -
10、氮氧化物是常见的大气污染物,目前气态含氮化合物及相关转化成为科学家研究的热门问题。
Ⅰ.还原法。反应原理为:。该反应的能量变化过程如下图:
 (1)、(用图中字母a、b、c、d表示)。该反应在(填“高温”、“低温”或“任意温度”)条件下有利于自发进行。(2)、Ⅱ.氧化法。其原理为 。在T℃、条件下,向一恒压密闭容器中按物质的量之比为2:1通入和的混合气体,体系中气体的含量与时间变化关系如图所示。
(1)、(用图中字母a、b、c、d表示)。该反应在(填“高温”、“低温”或“任意温度”)条件下有利于自发进行。(2)、Ⅱ.氧化法。其原理为 。在T℃、条件下,向一恒压密闭容器中按物质的量之比为2:1通入和的混合气体,体系中气体的含量与时间变化关系如图所示。
反应达到平衡,则0~20min内的平约反应速率 , 该反应的平衡常数[对于反应为平衡物质的量分数]。
(3)、若起始条件相同,在恒容密闭容器中发生上述反应,则达到平衡时NO的含量符合上图中点(填“a”、“b”、“c”或“d”)。(4)、Ⅲ.配合物吸收法。其原理如下:
已知:对的配合能力很强,而对的配合能力极低。
与反应的和与反应的物质的量之比为。
(5)、钴氨溶液经过多次循环吸收NO后,其吸收NO的能力会降低,为了恢复钴氨溶液吸收NO的能力,需采取的方法是。(6)、Ⅳ.电解处理法。其原理为用6%的稀硝酸吸收生成亚硝酸,再将吸收液导入电解槽中进行电解,使之转化为硝酸。电解装置如右图所示。
阳极的电极反应式为。
-
11、某实验小组从某废旧锂离子电池正极活性材料(主要成分可表示为 , 还含有少量、的化合物)中分别回收处理金属元素,工艺流程如下图所示:
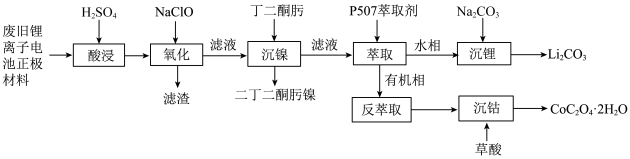
已知:①“酸浸”后滤液中主要金属阳离子为、、、;
②有关金属离子沉淀完全的见下表:
离子
9.3
3.2
9.0
8.9
③沉镍反应为

请回答下列问题:
(1)、丁二酮肟分子中杂化的碳原子个数为 , 二丁二酮肟镍中存在的化学键有(填序号)。A.链 B.氢键 C.金属键 D.配位键
(2)、“氧化”过程的操作为控制体系的在 , 加入溶液,写出反应的离子方程式。(3)、P507萃取剂(用HA表示)萃取的原理可表示为的浸出与水相的关系如图所示。分析较小时萃取率偏低的原因为。 (4)、和在空气氛围中焙烧可得到 , 该反应化学方程式为。(5)、将草酸钴晶体置于空气中加热,受热过程中固体残留率()变化如下图所示,则C点固体物质的化学式为。
(4)、和在空气氛围中焙烧可得到 , 该反应化学方程式为。(5)、将草酸钴晶体置于空气中加热,受热过程中固体残留率()变化如下图所示,则C点固体物质的化学式为。 (6)、的一种晶胞如图所示(仅标出与未标出)、该晶胞中占有O的个数为。
(6)、的一种晶胞如图所示(仅标出与未标出)、该晶胞中占有O的个数为。
-
12、葡萄糖酸钙是一种有机钙盐,主要用作食品的钙强化剂与营养剂、缓冲剂、固化剂、整合剂等。某实验小组在实验室以葡萄糖为原料制备葡萄糖酸钙的流程如下:
已知:相关物质的溶解性见下表:
物质名称
葡萄糖酸钙
葡萄糖酸
溴化钙
氯化钙
水中的溶解性
可溶于冷水,易溶于热水
可溶
易溶
易溶
乙醇中的溶解性
微溶
微溶
可溶
可溶
请回答下列问题:
(1)、实验室进行过程ⅰ时,加快其溶解的措施为。(2)、进行过程ⅱ的实验装置(加热装置已省去)如右图所示:
①写出此过程发生反应的化学方程式(有机物写出分子式即可);应采取的加热方式为。
②装置中仪器M的名称为;冷凝时冷凝水的入口为(填“a”或“b”);装置乙中倒扣漏斗的作用为。
(3)、操作为 , 其目的是;过程ⅴ加入乙醇的作用是。(4)、用电子天平称取葡萄糖酸钙(摩尔质量为)样品溶于水配制成溶液,取溶液置于锥形瓶中,加入指示剂,用的(用表示)标准溶液滴定至终点时,消耗标准溶液的体积为(已知:)。该样品中葡萄糖酸钙的质量分数为(用含有的代数式表示,不需化简)。 -
13、由、、等元素组成的钒基笼目金属在超导电性方面有广阔的应用前景,其晶胞结构如下图所示。下列说法错误的是( )
 A、钒基笼目金属的化学式为 B、分布在由构成的八面体空隙中 C、可以通过射线衍射实验测定晶体结构 D、1号、2号原子间的距离为
A、钒基笼目金属的化学式为 B、分布在由构成的八面体空隙中 C、可以通过射线衍射实验测定晶体结构 D、1号、2号原子间的距离为 -
14、饱和溶液中,随而变化,在温度下,与关系如右图所示。下列说法错误的是( )
 A、的溶度积 B、若忽略的第二步水解, C、饱和溶液中随增大而减小 D、点溶液中:
A、的溶度积 B、若忽略的第二步水解, C、饱和溶液中随增大而减小 D、点溶液中: -
15、铁铬液流电池(总反应为)实现了发电、环保一体化。某兴趣小组用该电池模拟工业处理废气和废水的装置如下图所示,下列说法正确的是( )
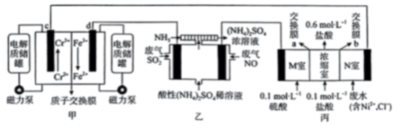 A、为正极,膜为阴离子交换膜 B、乙池中阴极的电极反应式为 C、标准状况下,若乙池中处理废气(和)的总体积为 , 则甲池有质子迁移到极 D、当浓缩室得到的盐酸时,室溶液的质量变化为(溶液体积变化忽略不计)
A、为正极,膜为阴离子交换膜 B、乙池中阴极的电极反应式为 C、标准状况下,若乙池中处理废气(和)的总体积为 , 则甲池有质子迁移到极 D、当浓缩室得到的盐酸时,室溶液的质量变化为(溶液体积变化忽略不计) -
16、用杯酚(表示为
 )分离和的过程如图甲所示,①~③各步骤在实验室中所用到的装置选择合理的是( )
)分离和的过程如图甲所示,①~③各步骤在实验室中所用到的装置选择合理的是( )
 A、①-a、②-a、③-d B、①-a、②-b、③-c C、①-b、②-a、③-d D、①-b、②-b、③-c
A、①-a、②-a、③-d B、①-a、②-b、③-c C、①-b、②-a、③-d D、①-b、②-b、③-c -
17、氨基甲铵()是化学工业中尿素生产过程的中间产物。向刚性密闭容器中加入一定量 , 在不同温度下发生反应 , 反应的压强平衡常数(用平衡时气体的分压代替平衡浓度表示的平衡常数)与反应热间存在关系式:(已知:R、C为常数,为热力学温度)。与关系的图像及相关数据如下图所示,判断下列说法正确的是( )
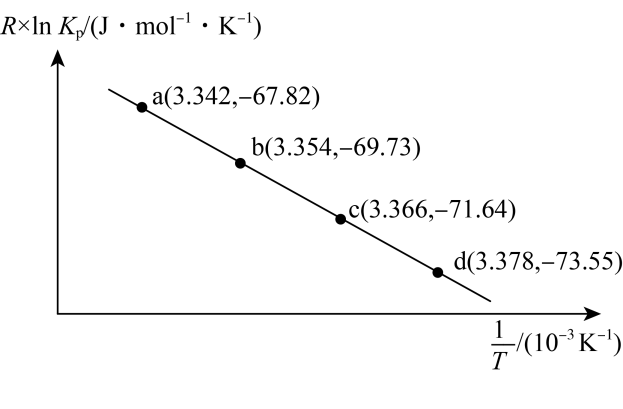 A、当容器内气体平均相对分子质量不再变化时,说明反应已经达到平衡状态 B、当温度一定时,向平衡后的容器内再加入 , 再次达到平衡时和的浓度增大 C、 D、若实验室利用与合成 , 则应选择低温环境进行
A、当容器内气体平均相对分子质量不再变化时,说明反应已经达到平衡状态 B、当温度一定时,向平衡后的容器内再加入 , 再次达到平衡时和的浓度增大 C、 D、若实验室利用与合成 , 则应选择低温环境进行 -
18、下列事实与解释相符的是( )
选项
事实
解释
A
相同条件下,乙醇与钠的反应没有水与钠反应剧烈
乙醇分子中氢氧键的极性比水分子中氢氧键的极性弱
B
与是同族元素,原子之间可以形成双键、三键,但原子之间难以形成双键或三键
易失去电子,不易形成共用电子对
C
在中的溶解度大于在水中的溶解度
是极性分子,而和均为非极性分子
D
充入氦、氖、氩等稀有气体的霓虹灯形成五颜六色的炫丽灯光
气体在外加电场激发下,形成了由电子和阳离子两种粒子组成且能导电的等离子体
A、A B、B C、C D、D -
19、某科研组研究利用碳催化烷烃脱氢反应的机理(其过程如图所示),建立起系统的非金属催化反应理论体系,切实推动了绿色非金属纳米碳催化领域的发展。下列有关碳催化烷烃脱氢过程分析正确的是( )
 A、反应中氧元素及部分碳元素价态有变化 B、生成总反应的化学方程式为 , 属于消去反应 C、
A、反应中氧元素及部分碳元素价态有变化 B、生成总反应的化学方程式为 , 属于消去反应 C、 、
、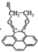 、
、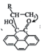 等均是反应的催化剂
D、有极性键和非极性的断裂,但只有极性键形成
等均是反应的催化剂
D、有极性键和非极性的断裂,但只有极性键形成
-
20、轻质碳酸镁是广泛应用于橡胶、塑料、食品和医药工业的化工产品,以卤块(主要成分为 , 含、等杂质离子)为原料制备轻质碳酸镁的工艺流程如图。下列说法错误的是( )
 A、在实验室进行①操作所用的仪器为玻璃棒、烧杯 B、“氧化”工序中发生反应的离子方程式为 C、②和③工序名称均为“过滤” D、“沉镁”工序控制合适的温度,产生的气体主要为和
A、在实验室进行①操作所用的仪器为玻璃棒、烧杯 B、“氧化”工序中发生反应的离子方程式为 C、②和③工序名称均为“过滤” D、“沉镁”工序控制合适的温度,产生的气体主要为和