-
1、我国计划在2060年前实现“碳中和”,彰显了大国担当,的资源化利用是实现“碳中和”的重要途径。如图是转化为甲醇的微观示意图,下列说法错误的是
 A、参加反应的、的分子个数比为 B、反应前后原子的种类和数目保持不变 C、图中共涉及到3种化合物 D、该反应为分解反应
A、参加反应的、的分子个数比为 B、反应前后原子的种类和数目保持不变 C、图中共涉及到3种化合物 D、该反应为分解反应 -
2、冬季是流感病毒肆虐的季节,“达菲”对抗流感病毒有很好的疗效,“达菲”的主要成分为莽草酸 , 下列有关莽草酸的说法正确的是A、莽草酸是由碳、氢、氧原子构成的 B、碳、氢、氧元素的质量比为 C、莽草酸分子由三种元素组成 D、莽草酸中氢元素的质量分数最小
-
3、金刚石、石墨和都是由碳元素组成的单质,下列有关碳单质的说法正确的是A、碳单质的化学性质都相似 B、石墨、金刚石和都是由碳原子直接构成 C、金刚石、石墨和都是黑色固体 D、石墨转化为金刚石的变化是物理变化
-
4、物质的性质决定其用途,下列物质性质与用途的对应关系错误的是A、氧气用于炼钢——可燃性 B、石墨用于受电弓滑板——导电性 C、食品包装中充氮气——化学性质不活泼 D、金刚石用于裁玻璃——硬度大
-
5、“春有百花秋有月,夏有凉风冬有雪”。对诗中景色变化的微观解释正确的是A、春天花香四溢——分子可以再分 B、夏天凉风习习——分子体积膨胀 C、秋天云开雾散——分子间隔变大 D、冬天白雪皑皑——分子停止运动
-
6、下列对实验现象的描述正确的是A、红磷在空气中燃烧,产生大量白雾 B、硫在空气中燃烧,发出淡蓝色火焰 C、木炭在空气中充分燃烧,生成二氧化碳 D、铁丝插入装有氧气的集气瓶中剧烈燃烧
-
7、我们生活在不断变化的物质世界中,下列变化属于物理变化的是A、粮食酿酒 B、蜡烛燃烧 C、修剪花枝 D、烹饪美食
-
8、如图所示的四个图像分别对应四种过程,其中不正确的是
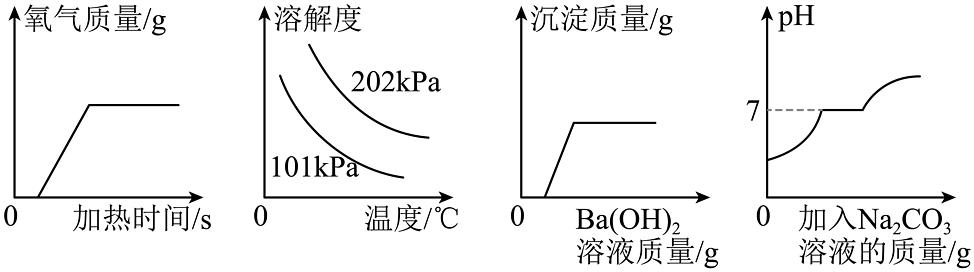 A、加热一定质量的高锰酸钾 B、某气体溶解度随温度和压强的变化 C、向一定量的硫酸钠和盐酸的混合溶液中加入Ba(OH)2溶液 D、向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液
A、加热一定质量的高锰酸钾 B、某气体溶解度随温度和压强的变化 C、向一定量的硫酸钠和盐酸的混合溶液中加入Ba(OH)2溶液 D、向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液 -
9、二氧化锰因应用广泛而备受关注,研究小组采用如图1所示装置,通过焙烧制取 , 剩余固体的质量和成分随温度的变化如“图2”所示。据此回答有关问题:
 (1)、制备应控制反应温度不超过。(2)、加热到:时,锰的氧化物会分解产生一种常见气体,这种气体的化学式为。(3)、请计算焙烧理论上可制得的质量是多少?(写出计算过程)(已知:生成的化学方程式为)(4)、如果反应温度达到时,充分反应后,剩余固体质量为。
(1)、制备应控制反应温度不超过。(2)、加热到:时,锰的氧化物会分解产生一种常见气体,这种气体的化学式为。(3)、请计算焙烧理论上可制得的质量是多少?(写出计算过程)(已知:生成的化学方程式为)(4)、如果反应温度达到时,充分反应后,剩余固体质量为。 -
10、我国科学家研制出全球首套捕集二氧化碳合成甲醇的装置,甲醇作为燃料具有安全高效、清洁、可再生的优点。在一定条件下转化成的工艺流程图,如图1所示:

查阅资料:甲醇常温下是一种无色液体,易溶于水,熔点 , 沸点。
(1)、操作1的名称是 , 若在实验室进行该操作,玻璃棒起到作用。(2)、铁和水蒸气高温条件下反应生成和 , 该反应涉及的化学方程式为 , 化学反应前后氢元素化合价(填“升高”或“不变”或“降低”)(3)、合成反应为: , 使用需过量,原因是。(4)、操作2能够将甲醇与水分离,是利用和的不同将他们分离。(5)、该流程将二氧化碳转化为甲醇的意义在于。(6)、流程中的铁粉能转化为多种铁的化合物,如图2为铁元素的价类转化二维图Ⅰ.b点对应物质的化学式为。
Ⅱ.利用一氧化碳使c转化为a,该反应中发生还原反应的物质是(写名称)。

-
11、
随着我国“资源节约型”与“环境友好型”城市的建设,城市垃圾的处理成为了一项重要工程。某校实践小组的同学们对垃圾的处理展开了项目化学习。

任务一:垃圾处理的方法:
(1)下列物质属于可回收垃圾的是(填字母)。
a.过期药品 b.果皮 c.废弃易拉罐 d.废旧电池
任务二:探究垃圾焚化产生的气体成分
某垃圾焚化产生的气体可能是中的一种或几种。
【查阅资料】ⅰ.能使红色的品红溶液褪色,也能使澄清石灰水变浑浊
ⅱ.紫红色酸性高锰酸钾溶液可与反应而褪色,常用于除去;
ⅲ.CO能使湿润的黄色氯化钯试纸变蓝。
【进行实验】
(2)分别做以下三个实验

序号
实验步骤
实验现象
实验结论
1
将待测气体通入品红溶液中
红色褪去气
体中含有
2
将待测气体通入放有③的集气瓶中
试纸变蓝色
气体中含有CO
3
将待测气体先通过图1装置后,再通入盛有澄清石灰水的试管中。
体中含有
【实验反思】
(3)实验3中,涉及检验的化学方程式为 , 检验前先将气体从(填“a”或“b”)端通入图1装置,其作用是;
(4)小组同学利用数字传感器测得焚化垃圾产生的气体中CO体积分数变化如图2所示,时间段内CO体积分数升高的原因是。
任务三:垃圾回收的宣传活动
(5)实践小组在文明小区进行了主题宣传活动,请帮他们设计一条宣传语:⑨。
-
12、
Ⅰ:的制取及性质:

(1)仪器a的名称是。
(2)组装一套能控制产生速率的发生装置,需用到图1中的仪器是(填字母),涉及反应的化学方程式为。
(3)收集一瓶并进行性质探究实验:
操作
现象
结论

细铁丝燃烧时,(填字母),生成黑色固体a.产生大量的白烟b.发出耀眼的白光c.剧烈燃烧,火星四射
具有氧化性
从安全角度分析,水的作用是。
Ⅱ.跨学科实践活动:设计鱼类运输供氧箱
任务1:选供氧剂
(4)查阅资料:过氧化钙、过氧化钠都能与反应生成 , 等质量的两种固体与足量水作用生成氧气的质量与时间的关系如图2所示。小组讨论后认为选择更好,理由是(写1条)。

任务2:设计装置
(5)为保证不同鱼类在运输中的存活率,需要监测水中溶氧量和温度。同学们在老师指导下,设计了如图3的鱼类运输供氧箱,其中微孔输氧棒的作用是。利用该装置持续供氧5分钟,数据记录如图4所示,可得出水中溶氧量随温度变化的规律为。

-
13、臭氧主要分布在臭氧层中,能吸收太阳光中绝大部分的紫外线,保护地球生物免受伤害。常温下,臭氧为淡蓝色气体,有鱼腥味,具有强氧化性,在水中能有效杀灭细菌、病毒等微生物。
制取臭氧的方法大致有紫外线法、电晕法和电解法。紫外线法为通过紫外线使空气中的氧分子电离,产生臭氧。该方法制取臭氧效率低,且对人体有一定伤害,因此应用较少。电晕法的原理如图1所示。电解法原理如图2所示,以水为原料,通过低压电解的方式获得臭氧。
使用打印机或复印机数量较多的场所容易产生高浓度的臭氧。长期暴露在臭氧超标的空气中会造成咽喉肿痛、神经

依据上文,回答下列
(1)、写出一条臭氧的化学性质。(2)、限制紫外线法大规模制取臭氧的原因是。(3)、图1中,利用制取属于(“物理”或“化学”)变化;图2中,电极a应连接电源的极。(4)、下列关于臭氧的说法,正确的是(填字母)。a.臭氧是空气污染物之一
b.臭氧可用于污水的处理
c.打印机使用频繁的场所要多开窗通风
d.长期处于臭氧浓度过高的环境中容易损害人体健康
(5)、和化学性质不同的原因是⑥。 -
14、银朱(HgS)是古代作画的红色颜料,有色泽鲜艳、久不褪色的特点,其制备过程如图所示。轻粉(氯化亚汞,化学式为)早在宋代就已入药,是一种微溶于水的白色粉末,易升华,光照易分解。
 (1)、水银属于①(填“金属”或“非金属”)单质。(2)、“研磨”时,水银与石亭脂充分反应生成银朱,化学方程式为② , 该反应属于③反应(填基本反应类型)。(3)、轻粉中汞元素的化合价是④ , 制备轻粉的反应为 , 则X的化学式为⑤。(4)、下列属于轻粉化学性质的是⑥(填字母)。
(1)、水银属于①(填“金属”或“非金属”)单质。(2)、“研磨”时,水银与石亭脂充分反应生成银朱,化学方程式为② , 该反应属于③反应(填基本反应类型)。(3)、轻粉中汞元素的化合价是④ , 制备轻粉的反应为 , 则X的化学式为⑤。(4)、下列属于轻粉化学性质的是⑥(填字母)。a.白色粉末 b.微溶于水 c.易升华 d.光照易分解
-
15、利用传感器采集蜡烛在密闭容器内燃烧过程中和体积分数的变化,以探究蜡烛熄灭的原因。实验装置如图甲所示,实验过程中采集到的数据如图乙所示,以下分析不合理的是
 A、图乙中的数据可以说明空气中的含量高于 B、蜡烛燃烧初期,的体积分数下降后又升高可能是燃烧放热引起的变化 C、蜡烛熄灭的原因可能是燃烧过程中消耗并产生一定浓度的 D、燃着的蜡烛能在浓度为和的混合气体中保持燃烧
A、图乙中的数据可以说明空气中的含量高于 B、蜡烛燃烧初期,的体积分数下降后又升高可能是燃烧放热引起的变化 C、蜡烛熄灭的原因可能是燃烧过程中消耗并产生一定浓度的 D、燃着的蜡烛能在浓度为和的混合气体中保持燃烧 -
16、同学们设计的下列实验方案(夹持装置已略去),能达到目的的是
目的
A.检验蜡烛燃烧是否生成水
B.探究不同催化剂的催化效果
C.验证质量守恒定律
D.测定空气中氧气含量
方案



 A、A B、B C、C D、D
A、A B、B C、C D、D -
17、物质的检验、鉴别和除杂是重要的化学实验技能。下列不能达到实验目的的是
选项
实验目的
实验方案
A
检验氧气是否集满
将带火星的小木条伸入集气瓶中
B
除去少量的
通过灼热的氧化铜
C
鉴别和
分别伸入燃着的木条,观察现象
D
鉴别水和过氧化氢溶液
取样,分别加入二氧化锰,观察现象
A、A B、B C、C D、D -
18、“劳动是一切幸福的源泉”,下列劳动实践与化学知识没有直接关联的是
选项
生活项目
化学知识
A
用厨余垃圾自制花肥
厨余垃圾发生缓慢氧化
B
用电吹风热风挡吹干湿衣服
温度越高,分子运动越快
C
用氮气制作氮肥
氮气在一定条件下能够发生化学反应
D
用铅笔芯制作电极
石墨质软
A、A B、B C、C D、D -
19、2023年7月12日朱雀二号成功发射,它是全球首枚以液氧液态甲烷为推进剂的运载火箭。请结合图,完成下面小题。
 (1)、下列关于“液态甲烷”的说法错误的是A、属于化合物 B、由5个原子构成 C、由碳、氢两种元素组成 D、碳、氢元素质量比为3:1(2)、液态甲烷燃烧的微观示意图如图甲所示,下列说法错误的是A、反应前后分子数目不变 B、反应前后元素种类不变 C、a分子中碳、氢原子个数比为1:4 D、反应生成c、d的质量比为22:9(3)、锗是火箭上重要半导体材料,锗元素相关信息见图乙,下列有关锗元素说法错误的是A、图中 B、属于金属元素 C、锗的中子数为32 D、锗的相对原子质量为72.64
(1)、下列关于“液态甲烷”的说法错误的是A、属于化合物 B、由5个原子构成 C、由碳、氢两种元素组成 D、碳、氢元素质量比为3:1(2)、液态甲烷燃烧的微观示意图如图甲所示,下列说法错误的是A、反应前后分子数目不变 B、反应前后元素种类不变 C、a分子中碳、氢原子个数比为1:4 D、反应生成c、d的质量比为22:9(3)、锗是火箭上重要半导体材料,锗元素相关信息见图乙,下列有关锗元素说法错误的是A、图中 B、属于金属元素 C、锗的中子数为32 D、锗的相对原子质量为72.64 -
20、下列实验操作正确的是A、
 加入块状大理石
B、
加入块状大理石
B、 读取液体体积
C、
读取液体体积
C、 连接胶塞管
D、
连接胶塞管
D、 检查装置气密性
检查装置气密性