-
1、某样品是由 Na2S、Na2SO3、Na2SO4这三种钠盐混合而成,测知该混合物中钠的质量分数为a%,则其中氧的质量分数为( ).A、 B、 C、 D、
-
2、在 FeSO4和Fe2(SO4)3的混合物中已知硫元素的质量分数为23%,则铁元素的质量分数为( ).A、36.8% B、31% C、28% D、无法计算
-
3、锌粉、铝粉、铁粉、镁粉的混合物3.8g与一定质量的溶质质量分数为25%的稀硫酸恰好完全反应,将反应后的混合物蒸发水分得固体(不含结晶水)11g,则反应中生成氢气的质量为( ).A、0.15g B、0.20g C、0.30g D、0.45g
-
4、分类、类比是学习化学变化常用的方法.(1)、初中化学有许多实验,若按照实验主要目的可将实验分为:探究化学反应前后物质的质量关系、探究物质的性质、探究物质的含量等.据此应将下列实验中的D与(填“A”“B”或“C”)归为一类,依据是.(2)、许多物质的命名与元素的化合价高低有关,如锰酸钾、高锰酸钾,其中锰元素的化合价分别为+6、+7.氯元素常见的化合价有+7、+5、+1、-1等,由此推测钠元素、氧元素和+7价氯元素三种元素组成的化合物的名称为 , 化学式为.

-
5、如图表示元素的化合价与物质类别关系,若它表示氮元素的部分关系图,则:
 (1)、A点对应的物质类别是;B点表示物质的化学式为.(2)、某化合物的化学式为 KNO3 , 它代表的点是(填字母);写出由 D 点表示的物质与水发生反应生成E 的化学方程式
(1)、A点对应的物质类别是;B点表示物质的化学式为.(2)、某化合物的化学式为 KNO3 , 它代表的点是(填字母);写出由 D 点表示的物质与水发生反应生成E 的化学方程式 -
6、如图是部分元素的离子结构示意图和元素周期表的一部分.请回答:
 (1)、图1、图2中属于阴离子的是(填序号),该元素的质子数为;13号元素原子的最外层电子数为.(2)、由表中原子序数为1、8、13的元素组成物质的化学式为.
(1)、图1、图2中属于阴离子的是(填序号),该元素的质子数为;13号元素原子的最外层电子数为.(2)、由表中原子序数为1、8、13的元素组成物质的化学式为. -
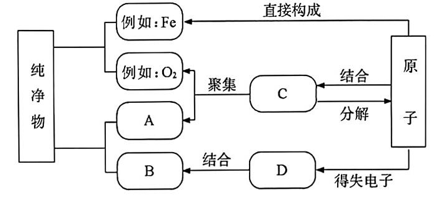
7、如图是构成纯净物的粒子间的关系图,请在A、B处填入物质的化学式,C、D处填入粒子种类名称(填“分子”“原子”或“离子”).
-
8、宏观和微观相联系是化学独特的思维方式.
 (1)、微观探究化学反应的规律是化学科学的核心任务.根据下列微观示意图回答问题:
(1)、微观探究化学反应的规律是化学科学的核心任务.根据下列微观示意图回答问题:①从微粒的角度说明图 A 反应的实质是;
②图 B所示反应中,参加反应的微粒是(写出微粒的符号).
(2)、化学上有一种能将微观粒子数目与宏观物质质量联系起来的量,叫物质的量,其单位是摩尔.1摩尔任何物质中含有构成它的微粒个数都是6.02×1023个,1摩尔任何物质的质量是以克为单位,数值上都等于该物质的相对分子质量.例如1摩尔水的各种量关系如下:
①1摩尔水中氢原子数目是个;②1摩尔水中氧元素质量为g.
-
9、物质之间存在联系,找出联系、发现规律是我们学好化学的一种基本方法.(1)、请你仿照下表中的示例,找出CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外两个规律并排序.
规律
排序
示例:标准状况下,密度由大到小
CO2、C2H4(乙烯)、C2H2(乙炔)、CH4
(2)、某气体由 CH4、C2H2、C2H4中的一种或几种组成,取该气体样品在氧气中完全燃烧,测得生成的二氧化碳和水的质量比为22:9.下列对该气体组成判断正确的是____.A、该气体中一定含有C2H4 B、该气体中一定没有CH4 C、该气体中可能含有C2H2 D、该气体不可能同时含有CH4、C2H2、C2H4 -
10、元素周期表中,同周期元素的结构和性质呈现一定的规律性变化.下表列出的是第三周期元素的原子半径及主要化合价(部分信息未列出).下列有关说法不正确的是( ).
元素
Na
Mg
①
Si
P
②
Cl
原子的最外层电子数
1
2
3
4
5
6
7
原子半径(nm)
0.186
0.160
0.143
③
0.110
0.102
0.099
最高正价最低负价
+1
+2
④
+4
-4
+5
-3
⑤
+7
-1
A、⑤处的最高正价是+6,最低负价是-2 B、③处的数值介于 0.110~0.143之间 C、第三周期元素(Na—Cl)的最高正价数等于其原子的最外层电子数 D、元素①的原子序数是13,①和②形成的化合物的化学式为 AlS -
11、有“第四类化学新材料”之称的玉米塑料是由乳酸(C3H6O3)合成的,下列有关乳酸的说法中正确的是( ).A、乳酸中碳、氢、氧三元素的质量比为3:6:3 B、1个乳酸分子中含有3个H2O分子 C、乳酸与甲醛(CH2O)中碳元素质量分数相同 D、乳酸的相对分子质量为90g
-
12、《茉莉花》是一首脍炙人口的苏南民歌.茉莉花香气的成分有多种,乙酸苯甲酯(C9H10O2)是其中的一种.下列关于乙酸苯甲酯的说法正确的是( ).A、乙酸苯甲酯的相对分子质量为150g B、乙酸苯甲酯由碳、氢、氧三种元素组成 C、乙酸苯甲酯中碳、氢、氧三种元素质量比为9:10:2 D、乙酸苯甲酯分子由碳原子、氢原子、氧分子构成
-
13、元素化合价发生改变的反应都是氧化还原反应.例如:反应前后,Fe和Cl元素的化合价发生了改变,该反应是氧化还原反应.下列反应不属于氧化还原反应的是( ).A、 B、 C、 D、
-
14、新版人民币中的防伪油墨含有一种由镁元素和氟元素(元素符号为F,化合价为-1)组成的化合物,它的化学式是( ).A、MgF B、MgF2 C、Mg2F D、Mg2F2
-
15、如图是某化学反应的微观示意图(“●”与“○”代表不同种元素的原子).

有关说法不正确的是( ).
A、甲中的一个分子由三个原子构成 B、化学反应的实质是原子的重新组合 C、该反应可能是水的电解 D、该反应前后元素的化合价不变 -
16、对于下列几种化学符号,有关说法正确的是( ).
①H ②Fe2+ ③Cu ④P2O5 ⑤Fe3+ ⑥NaCl
A、能表示一个分子的是①④⑥ B、表示物质组成的化学式是③④⑥ C、②⑤的质子数相同,化学性质也相同 D、④中的数字“5”表示五氧化二磷中有5个氧原子 -
17、含硫元素物质间发生转化:其中硫元素化合价发生变化的是( ).A、①② B、③④ C、①③ D、②④
-
18、化学物质中有一种由多个五边形和六边形组成的形似足球的笼状分子,称为“足球烯”(如右图所示),化学式(分子式)为 C60.关于C60的说法正确的是( ).
 A、属于单质 B、属于混合物 C、碳元素的化合价为+4 D、式量(分子量)为60
A、属于单质 B、属于混合物 C、碳元素的化合价为+4 D、式量(分子量)为60 -
19、下列化学用语所表达的意义正确的是( ).A、Al3+—铝离子 B、2K—2个钾元素 C、F2—2个氟原子 D、2SO3—3个二氧化硫分子
-
20、经测定,由甲醛(HCHO)、醋酸(CH3COOH)和丙酮(CH3COCH3)组成的混合物中,氢元素的质量分数为x%,则其混合物中氧元素的质量分数是( ).A、0.5x% B、1-1.5x% C、2x% D、1-7x%