-
1、某电镀厂为了减少对水的污染并节约成本,从排放的废液(主要含、和)中回收金属铜、铁以及工业原料硫酸锌,设计了如图所示的工艺流程,请据图回答下列问题:
 (1)、物质X的化学式是 , 固体 A中含有的物质是 , Y溶液中溶质的化学式是。(2)、步骤Ⅰ、步骤Ⅱ和步骤Ⅲ都是将固体和液体分离,操作名称是 , 此操作中除玻璃棒、烧杯外,还需使用的玻璃仪器是。(3)、请写出步骤Ⅲ中生成Fe的化学方程式:。(4)、请写一条保护金属资源的有效途径:。
(1)、物质X的化学式是 , 固体 A中含有的物质是 , Y溶液中溶质的化学式是。(2)、步骤Ⅰ、步骤Ⅱ和步骤Ⅲ都是将固体和液体分离,操作名称是 , 此操作中除玻璃棒、烧杯外,还需使用的玻璃仪器是。(3)、请写出步骤Ⅲ中生成Fe的化学方程式:。(4)、请写一条保护金属资源的有效途径:。 -
2、我国是世界上最早掌握冶炼铜和冶炼铁技术的国家之一。(1)、冶炼铜:一种方法是将孔雀石【主要成分是碱式碳酸铜】和木炭放入冶炼炉内,易受热分解: , X的化学式是。然后, CuO与木炭或与木炭不充分燃烧产生的CO反应冶炼出铜,请写出一个冶炼铜反应的化学方程式:。(2)、制青铜及青铜的应用:将铜与锡按照一定比例混合熔和而成青铜。青铜的熔点比铜的熔点 , 铸造性好,并且青铜的硬度比纯铜 , 所以青铜应用于制作货币、铜镜、农具、兵器和祭祀的礼器等等。(3)、冶炼铁:《天工开物》中有古代炼铁的记载,炼铁的主要原理是一氧化碳与氧化铁反应,其化学方程式为。
-
3、化学与生产、生活息息相关。请回答下列问题:(1)、为了除去冰箱中的异味,可放入活性炭包,利用了活性炭具有性。(2)、新型净水剂高铁酸钠中铁元素的化合价是。(3)、为了高质量的实现“双碳”目标,应充分开发利用太阳能、、水能、地热能、潮汐能等可再生能源。(4)、在冬季多雾天气,为了使提高大棚蔬菜的产量,要打开棚内的LED灯补充光照,并通入气体,使蔬菜进行光合作用。
-
4、下列图像不能正确反映其对应变化关系的是
 A、甲图:煅烧石灰石制生石灰 B、乙图:一定温度下,向饱和的硝酸钾溶液中,不断加入硝酸钾固体 C、丙图:向等质量的镁和铁中分别加入足量等浓度的稀盐酸 D、丁图:等质量、等质量分数的过氧化氢溶液完全分解
A、甲图:煅烧石灰石制生石灰 B、乙图:一定温度下,向饱和的硝酸钾溶液中,不断加入硝酸钾固体 C、丙图:向等质量的镁和铁中分别加入足量等浓度的稀盐酸 D、丁图:等质量、等质量分数的过氧化氢溶液完全分解 -
5、下列探究实验能达到实验目的的是A、
 验证质量守恒定律
B、
验证质量守恒定律
B、 探究甲烷燃烧产物有水生成
C、
探究甲烷燃烧产物有水生成
C、 木条熄灭,说明此气体肯定是
D、
木条熄灭,说明此气体肯定是
D、 探究不种溶质在同种溶剂中溶解性不同
探究不种溶质在同种溶剂中溶解性不同
-
6、为了缓解碳排放引起的温室效应,我国科学家成功合成新型催化剂,将二氧化碳转化为某可燃物,该过程的微观示意图如图。下列说法正确的是
 A、该反应属于置换反应 B、化学反应前后原子的种类不变 C、甲、乙反应时的质量比是1:22 D、丁物质中氢元素和碳元素的质量比是4:1
A、该反应属于置换反应 B、化学反应前后原子的种类不变 C、甲、乙反应时的质量比是1:22 D、丁物质中氢元素和碳元素的质量比是4:1 -
7、生活中区别食醋和酱油,可用闻气味的方法。下列实验方案不能达到实验目的的是A、区别溶液和溶液——观察溶液的颜色 B、区别红色粉末:铜粉和红磷——分别取少量放在燃烧匙上灼烧,观察现象 C、除去溶液中混有的溶液——加入足量铁粉,过滤 D、鉴定某金饰品是否是黄铜假冒的———在酒精灯上灼烧或测定密度
-
8、成人缺碘会引起甲状腺肥大,儿童缺碘影响生长和智力发育。如图为碘元素在元素周期表中的相关信息及其原子结构示意图。下列说法错误的是
 A、碘的原子序数是是53 B、碘的相对原子质量是126.9g C、碘元素属于非金属元素 D、碘原子在化学反应中容易得到电子
A、碘的原子序数是是53 B、碘的相对原子质量是126.9g C、碘元素属于非金属元素 D、碘原子在化学反应中容易得到电子 -
9、分类法是学习化学的一种方法,下列对各组的分类正确的是A、非金属元素:硅、磷、氢 B、氧化物:碳酸钙、一氧化碳CO、臭氧 C、纯净物:矿泉水、冰水、氧气 D、化石燃料:煤、石油、沼气
-
10、食醋是生活中常用的调味品,食醋中含有醋酸(化学式是)。下列关于醋酸的说法正确的是A、含有2个氧原子 B、碳元素和氢元素的质量比是1:4 C、氢元素的质量分数最大 D、相对分子质量是60
-
11、化学用语是学习化学的重要工具,下列化学用语所表达的意义正确的是A、2H——2个氢原子 B、——2个氧原子 C、——铁元素的化合价是 D、Mg——1个镁元素
-
12、“宏微结合”是化学学科的重要思想之一。对下列宏观事实的微观解释错误的是A、水和过氧化氢化学性质不同——分子构成不同 B、“遥知不是雪,为有暗香来”——分子在不断运动 C、干冰升华,体积变大——二氧化碳分子的体积变大 D、电解水生成氢气和氧气——在化学变化中,分子种类发生改变
-
13、水是生命之源。下列关于水的说法正确的是A、生活中常用煮沸的方法降低水的硬度 B、软水中不含、 C、河水经自来水厂净化后是纯净物 D、沉降、吸附、过滤、蒸馏中,“过滤”是单一净化水程度最好的方法
-
14、近几年河北省环境明显改善,“天更净、水更美”。下列说法错误的是A、植树种草既能改善环境,又能减缓“温室效应” B、使用脱硫煤减少的排放和酸雨的发生 C、废弃电池深埋,农作物秸秆一烧了之 D、合理使用农药和化肥,减少对水体的污染
-
15、物质的性质决定其用途。下列物质的用途主要由其化学性质决定的是A、石墨作电极 B、氧气用于医疗急救 C、金刚石作钻头 D、稀有气体可做霓虹灯光源
-
16、科学家经过多年研究证明,有一些同学爱吃的小包装零食中,含一定量的有毒、有害、致病的化学物质,如某些油炸食品中含有致癌物质丙烯酰胺(C3H5NO)。请你根据丙烯酰胺(C3H5NO)的化学式计算后填写:(1)、丙烯酰胺由种元素组成;一个丙烯酰胺分子中共有个原子。(2)、丙烯酰胺的相对分子质量为。(3)、丙烯酰胺中碳元素和氧元素的质量比是(最简整数比)。(4)、丙烯酰胺中碳元素的质量分数是(结果精确到0.1%)。(5)、142g丙烯酰胺中含氮元素的质量为g。
-
17、
关于催化剂的研究是一项重要的课题,某小组以“探究催化剂的奥秘”为题展开了项目式学习。
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,下列说法正确的是_________(填字母)。
A. 不加入催化剂化学反应就不能发生 B. 在化学反应前后催化剂的化学性质不发生改变 C. 用作催化剂的物质不可能是其他反应的反应物或生成物 D. 一个反应的催化剂可能有多种 【任务二】探究催化剂
查阅资料发现氧化铜也可以作为过氧化氢分解的催化剂,于是进行相应探究。称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行如图所示实验。

(2)填写如表:
步骤①现象
步骤⑥结果
步骤⑦现象
实验结论
试管中有极少量气泡产生,带火星的木条没有复燃
称得氧化铜的质量为________
产生大量气泡、带火星的木条复燃
氧化铜是过氧化氢分解反应的催化剂
(3)步骤①③对比可以说明________。
(4)该反应的文字或符号表达式为________。
【任务三】探究催化剂的催化效果
分别取10mL5%过氧化氢溶液、1g二氧化锰、1g氧化铜,按图1所示装置进行实验,实验时倾斜锥形瓶使过氧化氢溶液与催化剂完全接触,测得相同条件下瓶内气压的变化如图2所示。
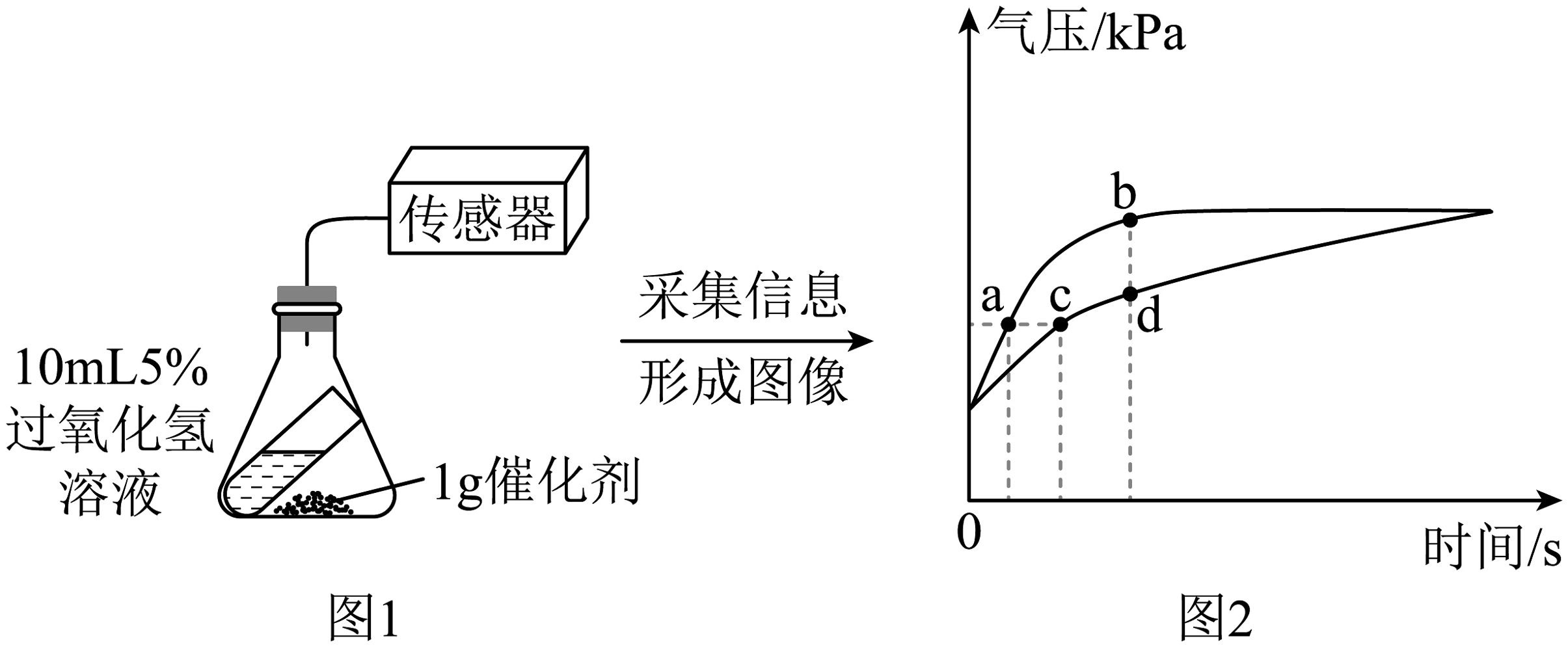
(5)对比分析图2中的________(填字母)点,可知化学反应速率与催化剂的种类有关。
(6)请从催化剂的角度解释在实验过程中,上述两个反应虽化学反应速率不同,但完全反应后两个装置内压强相同的原因________。
-
18、如图是实验室常用的实验装置。
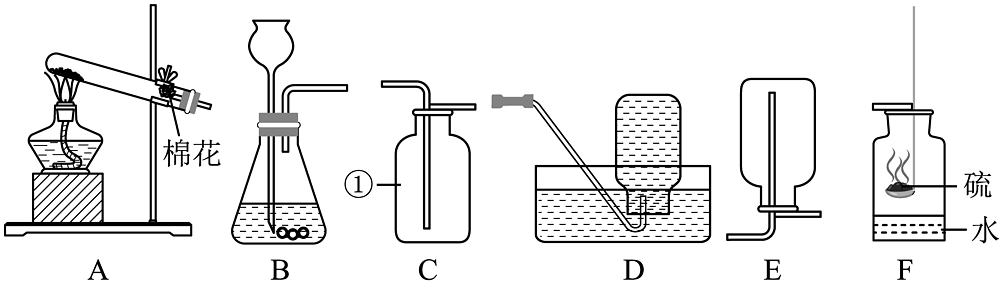 (1)、仪器①的名称是。(2)、若用高锰酸钾制取并收集较干燥的氧气选取的装置是(填字母),出该应的文字/符号表达式。(3)、能用D装置收集氧气是因为氧气具有且不与水反应的性质。(4)、将收集的氧气用作性质实验,如图F所示,水的作用是。(5)、写出F装置中发生反应的文字/符号表达式。
(1)、仪器①的名称是。(2)、若用高锰酸钾制取并收集较干燥的氧气选取的装置是(填字母),出该应的文字/符号表达式。(3)、能用D装置收集氧气是因为氧气具有且不与水反应的性质。(4)、将收集的氧气用作性质实验,如图F所示,水的作用是。(5)、写出F装置中发生反应的文字/符号表达式。 -
19、氧气是参与“氧循环”的重要物质。
 (1)、图1中,红磷燃烧的现象是。(2)、该反应的文字/符号表达式为。(3)、利用图1装置测定空气中氧气含量并结合传感器技术,测得实验过程中容器内气体强、温度的变化趋势如图2所示。请结合实验原理,解释引起DE段气体压强变化的操作是:。(4)、分别用红磷和木炭按图1装置实验,测得压强结果如图3、图4,造成两图结果不同的原因是。
(1)、图1中,红磷燃烧的现象是。(2)、该反应的文字/符号表达式为。(3)、利用图1装置测定空气中氧气含量并结合传感器技术,测得实验过程中容器内气体强、温度的变化趋势如图2所示。请结合实验原理,解释引起DE段气体压强变化的操作是:。(4)、分别用红磷和木炭按图1装置实验,测得压强结果如图3、图4,造成两图结果不同的原因是。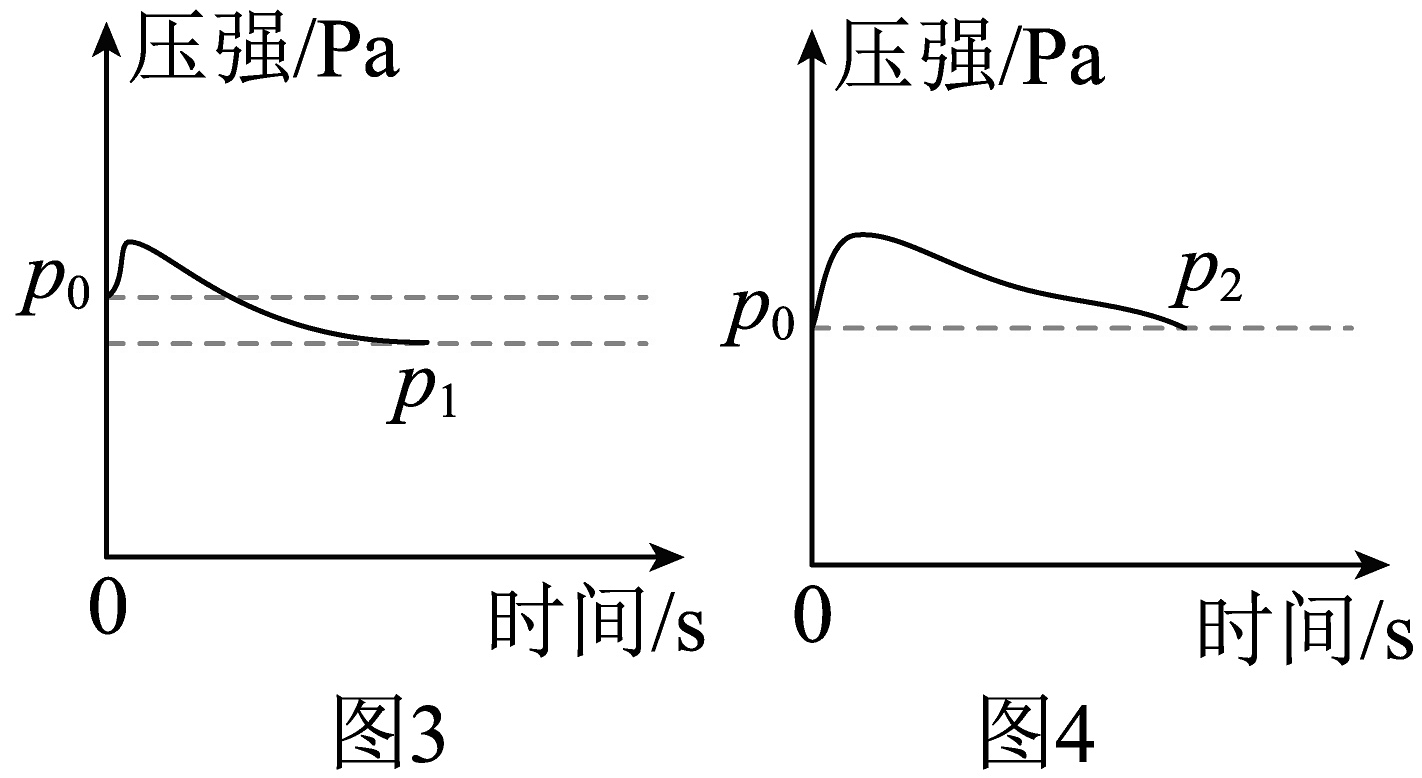
-
20、金属镓(Ga)可用于制作半导体,镓元素在元素周期表的信息以及Ga、A、B、C、D、E的微粒结构示意图如图所示。元素周期表中,金属元素、非金属元素和稀有气体元素常用不同颜色区分。

回答下列问题:
(1)、镓元素位于元素周期表第周期。(2)、在元素周期表中,镓元素与A元素所占方格颜色(选填“相同”或“不同”)。(3)、如图A~E中,一共涉及种元素。(4)、E(属于铝元素)失去3个电子,形成阳离子,该离子符号为。(5)、Ga与B(属于氧元素)形成化合物的化学式为。