-
1、辣椒炒肉是湘菜中的一道经典名菜,其中辣椒的辣味主要来源于辣椒素(化学式为)。下列关于辣椒素说法正确的是A、氢元素的质量分数最大 B、辣椒素中碳、氢元素质量比为 C、辣椒素由碳、氢、氧、氮四种元素组成 D、辣椒素由18个碳原子、27个氢原子、1个氮原子、3个氧原子构成
-
2、2025年2月7日晚,第九届亚洲冬季运动会在中国哈尔滨隆重开幕。冰雪运动中,人造雪被广泛使用。造雪机工作原理是将水雾化后喷入寒冷空气中,使其迅速凝固成雪。水由液态变为固态的过程中,下列说法正确的是A、水分子的体积变小 B、水分子的种类改变 C、水分子的间隔改变 D、水分子停止运动
-
3、2025年初,美国洛杉矶多地连续突发山火,当地消防员采用多种方式灭火。下列灭火措施对应原理正确的是A、砍伐货场周围树木形成隔离带——隔绝氧气 B、直升机投掷干粉灭火弹——降低可燃物温度至着火点以下 C、使用高压水枪喷洒火场——移除可燃物 D、空中喷洒阻碍剂覆盖燃烧物——隔绝氧气
-
4、近日,我国科学家研究发布目前最高水准超导量子计算机——“祖冲之三号”体现我国科学技术的不断进步。计算机用到的芯片成分之一是硅,下图是硅元素在元素周期表中的相关信息,下列说法正确的是
 A、硅元素是金属元素 B、硅元素的原子序数为14 C、硅元素的相对原子质量为28.09g D、硅元素是地壳中含量最高的元素
A、硅元素是金属元素 B、硅元素的原子序数为14 C、硅元素的相对原子质量为28.09g D、硅元素是地壳中含量最高的元素 -
5、我们知道“物质的性质决定物质的用途”。下列物质的性质与所对应的用途描述正确的是A、稀有气体通电时能发出不同颜色的光——作保护气体 B、金刚石是是天然存在最硬的物质——可用来切割金属、大理石等物质 C、焦炭具有还原性——可用于吸附水中的色素 D、钛和钛合金的抗腐蚀能力非常好——可用来制造人造骨
-
6、化学是一门以实验为基础的学科,正确的实验操作以及准确的现象记录对于实验至关重要。回答下列小题。(1)、规范的操作方法是实验安全和成功的重要保证。下列实验操作规范的是A、
 B、
B、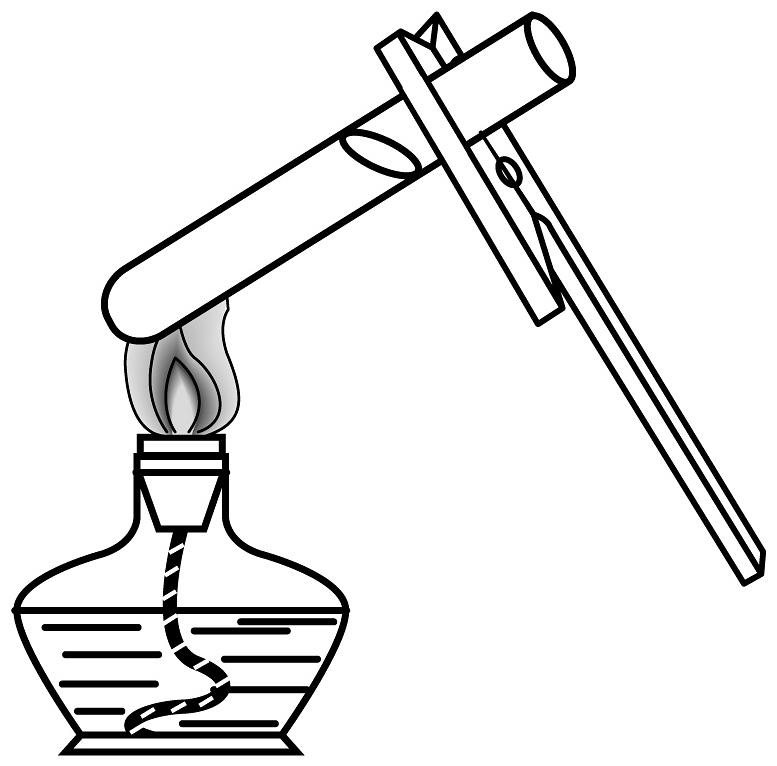 C、
C、 D、
D、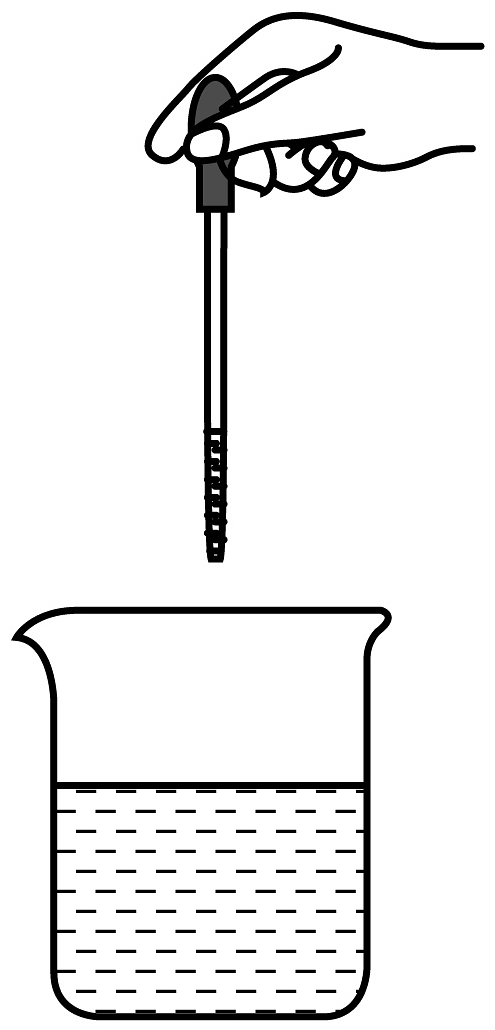 (2)、化学学习需要关注物质变化的现象,并根据现象得出结论,下列结论中正确的是
(2)、化学学习需要关注物质变化的现象,并根据现象得出结论,下列结论中正确的是选项
实验操作
现象
结论
A
将燃着的木条伸入盛有无色气体的集气瓶中
木条熄灭
该气体一定是
B
将打磨后的铝丝浸入硫酸铜溶液中
铝丝上附着红色固体
铝的金属活动性比铜强
C
向稀盐酸中加入某固体
有气泡产生
该固体一定是活泼金属
D
向镁粉中加入稀盐酸
产生大量气泡
该反应放出热量
A、A B、B C、C D、D -
7、以中国传统神话故事为原型的春节档电影《哪吒之魔童闹海》票房突破145亿,向世界展示了中国文化,也加深了我们的文化自信。电影情节中包含许多化学知识,请你结合所学知识回答下列小题。(1)、下列情节中体现的是化学变化的是A、敖丙将水凝结成冰作为自己的武器进行战斗 B、哪吒的风火轮在使用时都伴随着熊熊燃烧的烈火 C、太乙真人将莲藕拼接重塑哪吒肉身 D、申公豹的袍子被哪吒撕破(2)、电影中魔气污染海水的情节,是映射现实当中有人破坏水资源的行为,下列做法能起到保护水资源的作用的是A、工业污水进行分级净化处理后重新作为灌溉用水使用 B、生活废水直接排放到江河中 C、将生活垃圾收集投海 D、大肆使用农药和化肥(3)、哪吒所使用的火尖枪是由金属铁制作而成,以下做法不能有效防止火尖枪生锈的是A、在枪身上涂油进行保养 B、在枪头镀一层耐腐蚀的铬 C、将铁质枪身换成不锈钢 D、用湿布包裹后存放在山洞中
-
8、小王发现厨房所用炉具清洁剂的有效成分是氢氧化钠,为测定该炉具清洁剂中氢氧化钠的质量分数,他进行了如下实验:取100g该炉具清洁剂于烧杯中,加入50g溶质质量分数为9.8%的稀硫酸恰好完全反应。(炉具清洁剂中的其他成分不与稀硫酸反应)(1)、计算该炉具清洁剂中氢氧化钠的质量分数(请写出计算过程)。(2)、炉具清洁剂在不用时需密封保存的原因是________。
-
9、金属蚀刻画是我国一项高超的艺术制作技艺,化学探究学习兴趣小组想利用废弃的金属片亲手制作简单的金属蚀刻画,请你参与进来一起完成本次探究活动。(1)、任务一:筛选金属底板
【提出问题】
I.选择金属考虑哪些问题?
II.金属的选择和蚀刻反应液之间存在什么关系?
【讨论】
I.要考虑金属活动性,选择容易反应的金属片,不能选择铜等活动性较稳定的金属。
II.反应在常温下进行,考虑金属与酸反应、金属与盐溶液发生反应等易于进行操作。
【实验操作】
I.同学们利用化学知识,选择金属活动性较强的金属用于实验。
II.最后,选择了铝片和铁片。区分铝片和铁片的物理方法是________(写一种)。
(2)、任务二:预处理金属底板和选择蚀刻液进行蚀刻【提出问题】
I.如何让金属只与反应液反应,而其他部分不参与反应?
II.选择什么蚀刻液进行实验?
【讨论】
I.通过课外知识,同学们讨论使用石蜡作为保护金属片的物质,因为石蜡在常温下难与酸和盐溶液发生化学反应。
II.同学们经过讨论,决定选择酸和盐溶液进行蚀刻反应。
【实验操作及现象】
I.用砂纸打磨铝片和铁片表面,去除氧化膜。这样处理的目的是。
II.用融化的石蜡均匀地覆盖在铝片和铁片上,待石蜡固化后用尖利的刀子划破石蜡,在铝片上画刻出“中国梦”的字样,在铁片上刻画出一朵小花。
III.随后将铝片浸入足量的甲蚀刻液中,将铁片浸入足量的乙蚀刻液中,一段时间后取出,小心去除金属表面的石蜡。
IV.铝片上“中国梦”字迹凹陷,没有附着物;铁片上的小花图案呈突起的红色。则他们选择的甲蚀刻液、乙蚀刻液分别是下列中的、(填序号)。
①硫酸铜溶液 ②硝酸银溶液 ③稀盐酸 ④氯化亚铁溶液 ⑤氯化钠溶液
其中,铁片上发生反应的化学方程式为。
(3)、任务三:讨论如何进行废液回收利用【讨论及分析】
铝片蚀刻废液处理,可加入足量铝片,得到的溶液中的溶质为________,回收保存。
【结果】通过大家分析,一直通过讨论分析的可行性评价,可以实施。
【反思】化学学习不但激发我们对物质世界的好奇心,还能发展科学思维、创新精神与实践能力,促进我们对物质世界深层次认识,培养我们科学态度和社会责任。
-
10、化学是一门以实验为基础的学科,某小组利用如图装置制备气体。回答下列问题。
 (1)、检查B装置气密性的方法是________。(2)、实验室用A装置制取氧气,发生反应的化学方程式为 , 若用C装置收集氧气,氧气应从(填“m”或“n”)端通入。(3)、若用D装置收集氧气,集气瓶内装35%的水(其余部分为空气),收集的气体恰好能使带火星的木条复燃,则能使带火星木条复燃的氧气最低含量为________%(用体积分数表示)。
(1)、检查B装置气密性的方法是________。(2)、实验室用A装置制取氧气,发生反应的化学方程式为 , 若用C装置收集氧气,氧气应从(填“m”或“n”)端通入。(3)、若用D装置收集氧气,集气瓶内装35%的水(其余部分为空气),收集的气体恰好能使带火星的木条复燃,则能使带火星木条复燃的氧气最低含量为________%(用体积分数表示)。 -
11、中国芯,湖南造。现代科技的发展离不开芯片,硅是芯片的重要基材。如图是工业上以四氯硅烷(SiCl4)为原料制取高纯硅的微观示意图。
 (1)、保持乙的化学性质的最小粒子是________。(2)、该反应的化学方程式为 , 该反应属于(填基本反应类型)。(3)、参加反应的乙与生成物丙的质量比是________。
(1)、保持乙的化学性质的最小粒子是________。(2)、该反应的化学方程式为 , 该反应属于(填基本反应类型)。(3)、参加反应的乙与生成物丙的质量比是________。 -
12、阅读下面文章。
随着全球能源危机、气候变暖等环境问题的日益突出,“低碳”已经成为世界关注的焦点。高能耗、高排放的钢铁行业降低成本、节能与环保愈加重要,将生物质这种可再生碳源合理应用于钢铁生产,必会带来巨大的经济效益、环境效益和社会效益。
生物质是一切生命体新陈代谢产生的有机物质,如秸秆、锯末、牛粪等。生物质能本质上是太阳能的一种表现形式,具有可再生性、清洁性、丰富性和可替代性等特点。
生物质能替代化石能源用于钢铁生产成为研究和关注的热点,生物质碳化技术工艺如图所示。

研究发现,利用生物炭部分替代煤炭炼焦进行炼铁时,可使高炉的温室气体排放量降低23.5%左右。制备出的生物炭具有管状结构,有较高的比表面积,其燃烧性能以及与CO2气化反应性能均优于煤炭。
目前,我国已将生物质能开发列入国家“十二五”能源发展规划,未来在钢铁生产中的潜力巨大。
(1)、生物质能理论上可达到碳的零排放,原因是________。(2)、生物炭与CO2气化反应的化学方程式为________。(3)、生物炭燃烧性能优于煤炭的原因是________。 -
13、宣纸是我国传统的古典书画用纸,其制作工艺被列入首批国家级非物质文化遗产。以檀树茎皮和稻草等为原料生产宣纸的部分流程如图所示,请分析思考,解答问题:
 (1)、抄纸是用多孔的竹帘将纸浆捞出,其原理与实验基本操作________相同。(2)、晒纸时,在阳光下比阴凉处干得快,其微观解释为________。(3)、博物馆里一般把贵重字画保存在充满氮气的圆桶中,以防止宣纸蛀虫和氧化变黄,原因是________(写一点)。
(1)、抄纸是用多孔的竹帘将纸浆捞出,其原理与实验基本操作________相同。(2)、晒纸时,在阳光下比阴凉处干得快,其微观解释为________。(3)、博物馆里一般把贵重字画保存在充满氮气的圆桶中,以防止宣纸蛀虫和氧化变黄,原因是________(写一点)。 -
14、天气瓶可用来预测天气变化,瓶内液体结晶的形态会随温度而发生改变。制作天气瓶需用到硝酸钾和氯化铵固体,下图是两种物质的溶解度曲线。
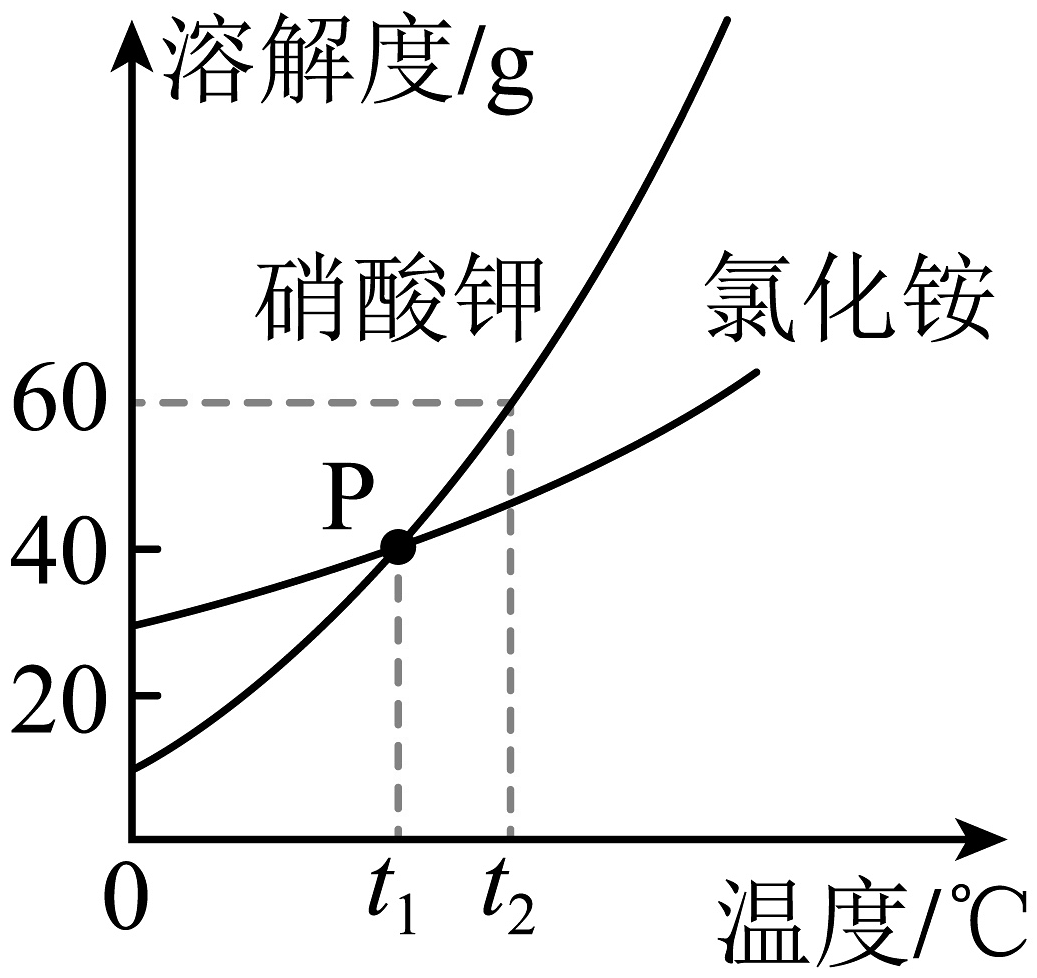 (1)、当温度小于________℃时,氯化铵的溶解度大于硝酸钾。(2)、时,50g硝酸钾加入到50g水中,充分溶解后所得溶液的质量为________g。(3)、时,分别将等质量的硝酸钾、氯化铵的饱和溶液升温到 , 硝酸钾溶液中溶质的质量________(填“大于”“等于”或“小于”)氯化铵溶液中溶质的质量。
(1)、当温度小于________℃时,氯化铵的溶解度大于硝酸钾。(2)、时,50g硝酸钾加入到50g水中,充分溶解后所得溶液的质量为________g。(3)、时,分别将等质量的硝酸钾、氯化铵的饱和溶液升温到 , 硝酸钾溶液中溶质的质量________(填“大于”“等于”或“小于”)氯化铵溶液中溶质的质量。 -
15、化学与生活、生产息息相关,请运用化学知识回答下列问题:(1)、小苏打不仅能用于焙制糕点,还能用于治疗胃酸过多症,其化学式为________。(2)、长沙臭豆腐起源于湘阴油炸豆腐,是皮酥内软口感极佳的小吃,臭豆腐可提供的主要营养素是________。
-
16、下列关于溶液的说法正确的是A、溶液都是无色透明的液体 B、气体、液体、固体都可以作为溶液的溶质 C、溶液由溶质和溶剂组成,所以溶液的质量和体积等于溶质和溶剂的质量和体积 D、溶液具有均一性、稳定性,所以具有均一性、稳定性的液体都是溶液
-
17、小组同学用如图装置探究可燃物燃烧的条件,向上提拉燃烧匙,直至a处白磷、b处红磷露出水面,观察到仅a处的白磷燃烧(已知白磷、红磷的着火点分别为40℃、60℃),下列说法正确的是
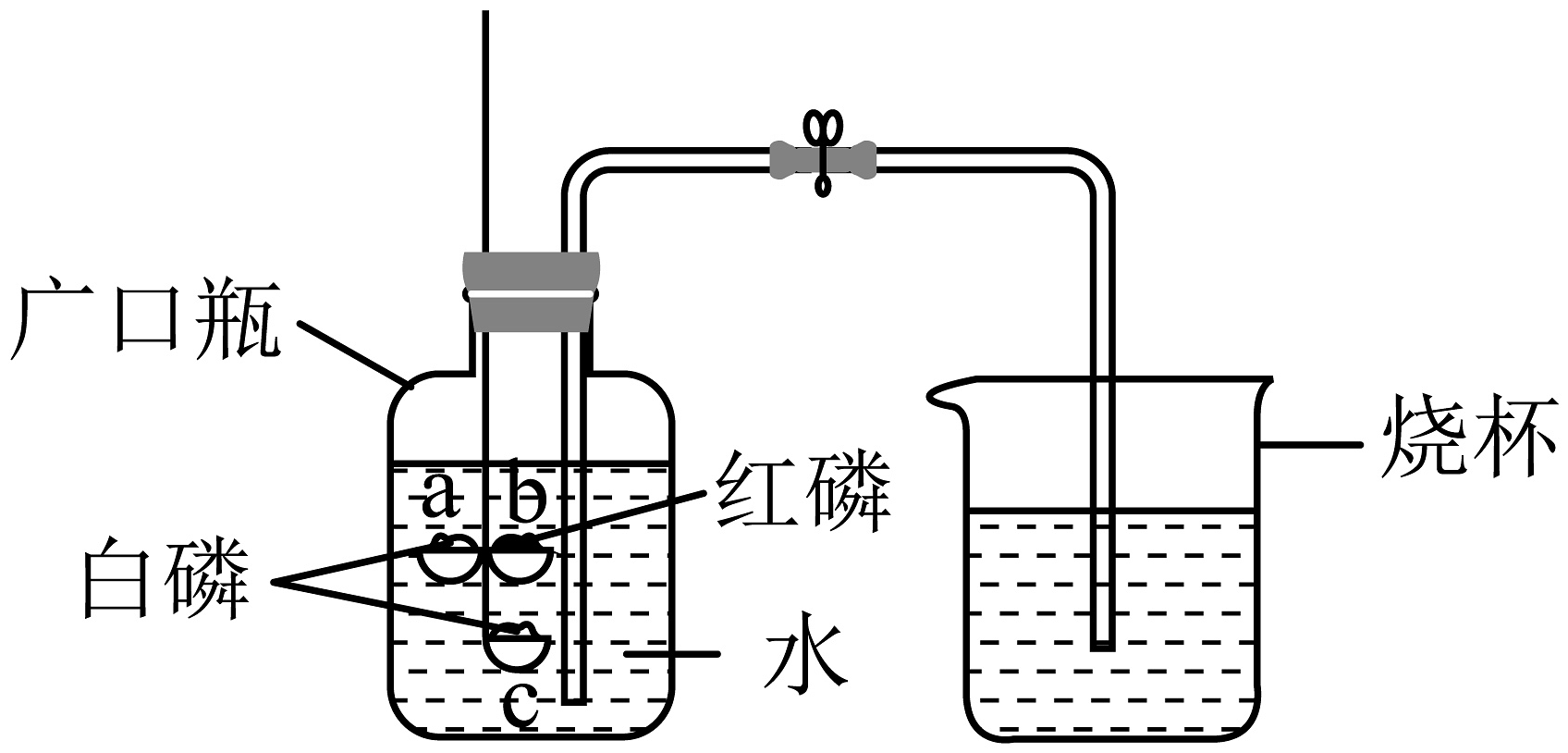 A、广口瓶内水的温度可能是30℃ B、实验中红磷不燃烧,说明红磷不是可燃物 C、对比a、c处的现象,证明燃烧需要与氧气接触 D、冷却至室温后打开弹簧夹,广口瓶内的水流至烧杯中
A、广口瓶内水的温度可能是30℃ B、实验中红磷不燃烧,说明红磷不是可燃物 C、对比a、c处的现象,证明燃烧需要与氧气接触 D、冷却至室温后打开弹簧夹,广口瓶内的水流至烧杯中 -
18、下列物质性质和用途对应关系不正确的是A、活性炭有吸附性,可用作除味剂 B、熟石灰有碱性,可用于治疗胃酸过多 C、油脂能溶于汽油,可用于除油污 D、铁粉能与氧气和水反应,可用作食品干燥剂
-
19、某中学考查通过实验检验生活中常见物质的酸碱性,下列物质中呈酸性的是A、食盐水 B、蒸馏水 C、肥皂水 D、白醋
-
20、合理使用化肥对“发展粮食产业,助力乡村振兴”具有重要意义。下列化肥属于复合肥的是A、KNO3 B、K2SO4 C、CO(NH2)2 D、NH4HCO3