-
1、4%硼酸洗液在生活中有广泛用途,进行如下实验配制4%硼酸溶液(右表为硼酸的溶解度)。
实验步骤
实验操作
实验结果
温度(℃)
硼酸的溶解度(g/100g水)
I
10℃时,取4.0g硼酸,加入46mL水
硼酸部分溶解
10
3.65
Ⅱ
升温至40℃
硼酸完全溶解
20
4.87
Ⅲ
继续加入50mL水
配置完成
40
8.90
下列说法正确的是
A、硼酸的溶解度为3.65g/100g水 B、可通过充分搅拌使步骤Ⅰ中的硼酸完全溶解 C、步骤Ⅱ中所得溶液的浓度为8% D、所得溶液在20℃时会析出固体,浓度减小 -
2、铁在空气中会产生铁锈,铁锈中含Fe2O3和Fe(OH)3 , 下列说法正确的是A、铁锈的成分都属于氧化物 B、铁锈的成分中铁元素的化合价相同 C、氧气一定参与了反应 D、水蒸气可能参与了反应
-
3、过氧化氢溶液与二氧化锰粉末混合,反应前后不变的是A、氢元素的质量 B、二氧化锰的质量 C、过氧化氢的浓度 D、水的质量
-
4、下表实验能说明影响物质溶解性的因素是
实验编号
温度
固体
液体
固体和液体混合并振荡后的现象
1
20℃
1g碘
5g水
有固体剩余
2
20℃
1g碘
5g汽油
无固体剩余
3
30℃
1g碘
5g水
有固体剩余
4
30℃
1g碘
10g水
有固体剩余
A、溶剂种类 B、溶质种类 C、溶剂质量 D、温度 -
5、属于分解反应的是A、 B、 C、 D、
-
6、能使一氧化碳充分燃烧的措施是A、使一氧化碳转化为固体 B、不断鼓入新鲜空气 C、使用足量的一氧化碳 D、按2:1的比例通入空气
-
7、点燃一氧化碳,再把一只内壁涂有澄清石灰水的烧杯罩在火焰上方,关于该实验的说法错误的是A、点燃一氧化碳前需要验纯 B、能观察到蓝色火焰 C、澄清石灰水变浑浊 D、证明一氧化碳是由碳元素和氧元素组成的
-
8、干冰是固态二氧化碳,对干冰和一氧化碳的描述正确的是A、互为同素异形体 B、是同一种物质 C、由同种元素组成的不同种化合物 D、由不同种元素组成的同种化合物
-
9、一氧化碳是一种常见的燃料,它的化学式为A、O1C B、C1O1 C、CO D、OC
-
10、气体肥料的优点是扩散性强,其原因是A、分子之间有间隙 B、分子在不断运动 C、分子是保持物质化学性质的一种微粒 D、分子体积很小
-
11、能与稀盐酸反应制备CO2的试剂为A、CaCO3 B、Na2SO3 C、FeS D、Mg
-
12、向滴有石蕊的水中通入CO2 , 能观察到A、溶液由红色变为紫色 B、溶液由红色变为蓝色 C、溶液由紫色变为红色 D、溶液由紫色变为蓝色
-
13、能与CO2发生反应的是A、O2 B、N2 C、He D、C
-
14、一个二氧化碳分子中含有A、碳和氧气 B、碳原子和氧分子 C、一个碳原子和一个氧分子 D、一个碳原子和两个氧原子
-
15、属于纯净物的是A、液态二氧化碳 B、矿泉水 C、碳酸饮料 D、空气
-
16、CO2中碳元素存在的形态是A、游离态 B、化合态 C、固态 D、液态
-
17、CO2是一种常用的气体肥料。在温室中施用CO2可提高作物光合作用的强度和效率,促进根系发育,提高产品品质,并大幅度提高作物产量。不属于CO2气肥优点的是A、提高作物产量 B、可溶于水 C、促进光合作用 D、提高产品品质
-
18、“化学氧呼吸自救器”是人在缺氧环境或出现高浓度有毒有害气体环境中使用的一种安全防护装置,内部装有颗粒状黄色固体超氧化钾(KO2)作为“制氧剂”(如图1所示),其反应原理是利用超氧化钾与人体呼出的二氧化碳反应(4KO2+2CO2=2X+3O2)。
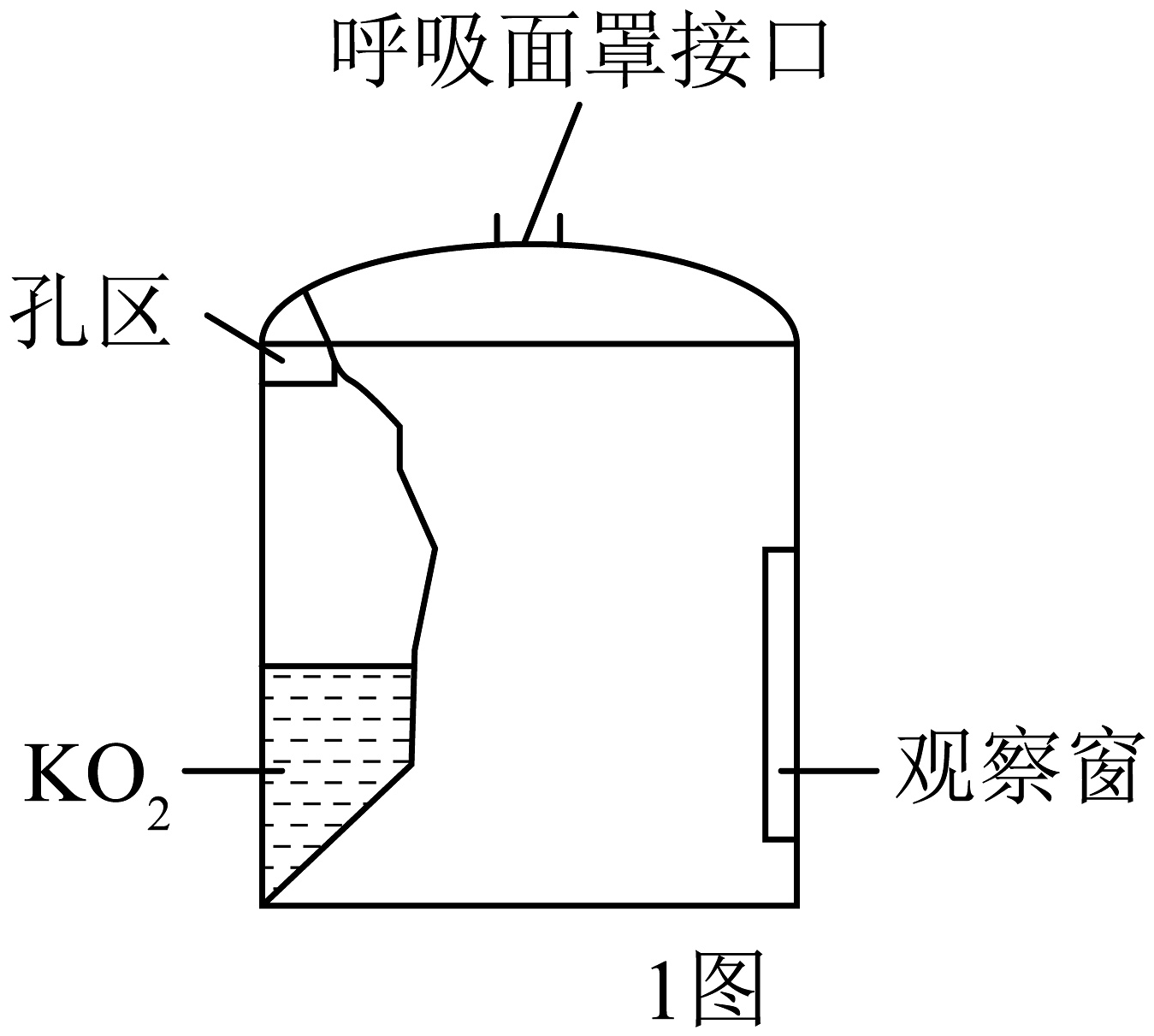 (1)、使用化学氧呼吸自救器一段时间后,当观察到生氧剂(填颜色变化),则基本失效。(2)、X的化学式为 , 超氧化钾中钾、氧元素的质量比为。(3)、工作人员使用该化学氧呼吸自救器时,加入710g超氧化钾,若每分钟消耗8g氧气,计算产生的氧气可提供自救的时间(写出计算过程)。(4)、正常呼吸需要制氧剂的生氧速率不低于1L•min-1 , 相同质量的超氧化钾利超氧化钠(NaO2)的生氧性能如图2所示。其中选取KO2要优于NaO2 , 原因是。
(1)、使用化学氧呼吸自救器一段时间后,当观察到生氧剂(填颜色变化),则基本失效。(2)、X的化学式为 , 超氧化钾中钾、氧元素的质量比为。(3)、工作人员使用该化学氧呼吸自救器时,加入710g超氧化钾,若每分钟消耗8g氧气,计算产生的氧气可提供自救的时间(写出计算过程)。(4)、正常呼吸需要制氧剂的生氧速率不低于1L•min-1 , 相同质量的超氧化钾利超氧化钠(NaO2)的生氧性能如图2所示。其中选取KO2要优于NaO2 , 原因是。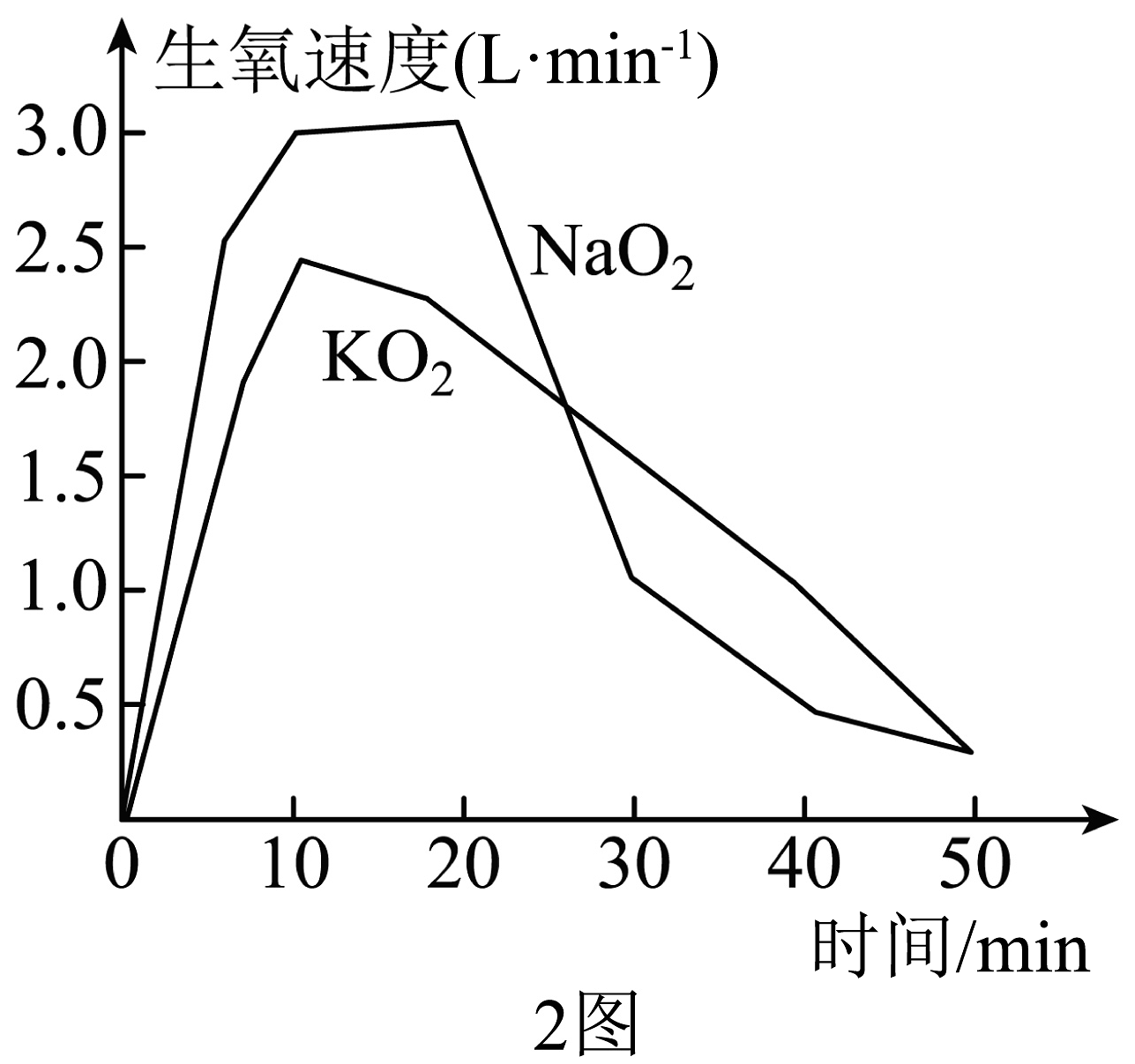
-
19、氢氧化镁是一种新兴的环保型无机阻燃剂。工业上以白云石(主要成分为MgCO3、CaCO3)为原料制备Mg(OH)2的一种流程如图1所示。
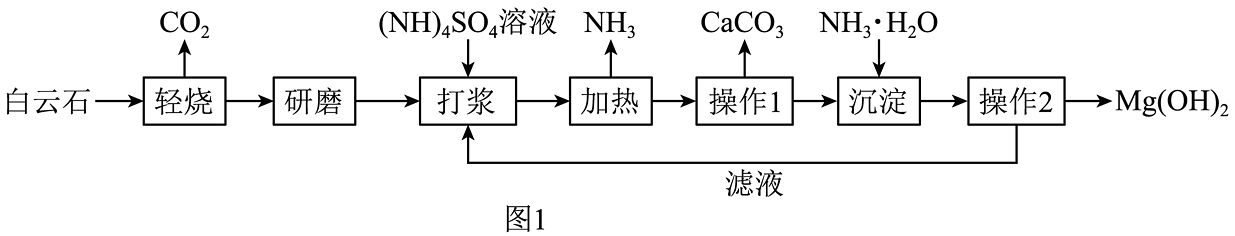
【资料】白云石轻烧的主要产物是MgO、CaCO3。
(1)、白云石“轻烧”除防止CaCO3分解外,还具有的优点是。(2)、对“轻烧”后的固体进行研磨的目的是。(3)、操作1和操作2的名称是 , 实验室进行该操作需要用到的玻璃仪器有烧杯、和玻璃棒。(4)、加热过程中,MgO和(NH4)2SO4发生反应,其反应的化学方程式是。(5)、加热时,在50℃、70℃和90℃的溶液中(NH4)2SO4的利用率与时间的关系如图2所示。据图可知,工业生产中一般采用90℃的加热温度,其原因是。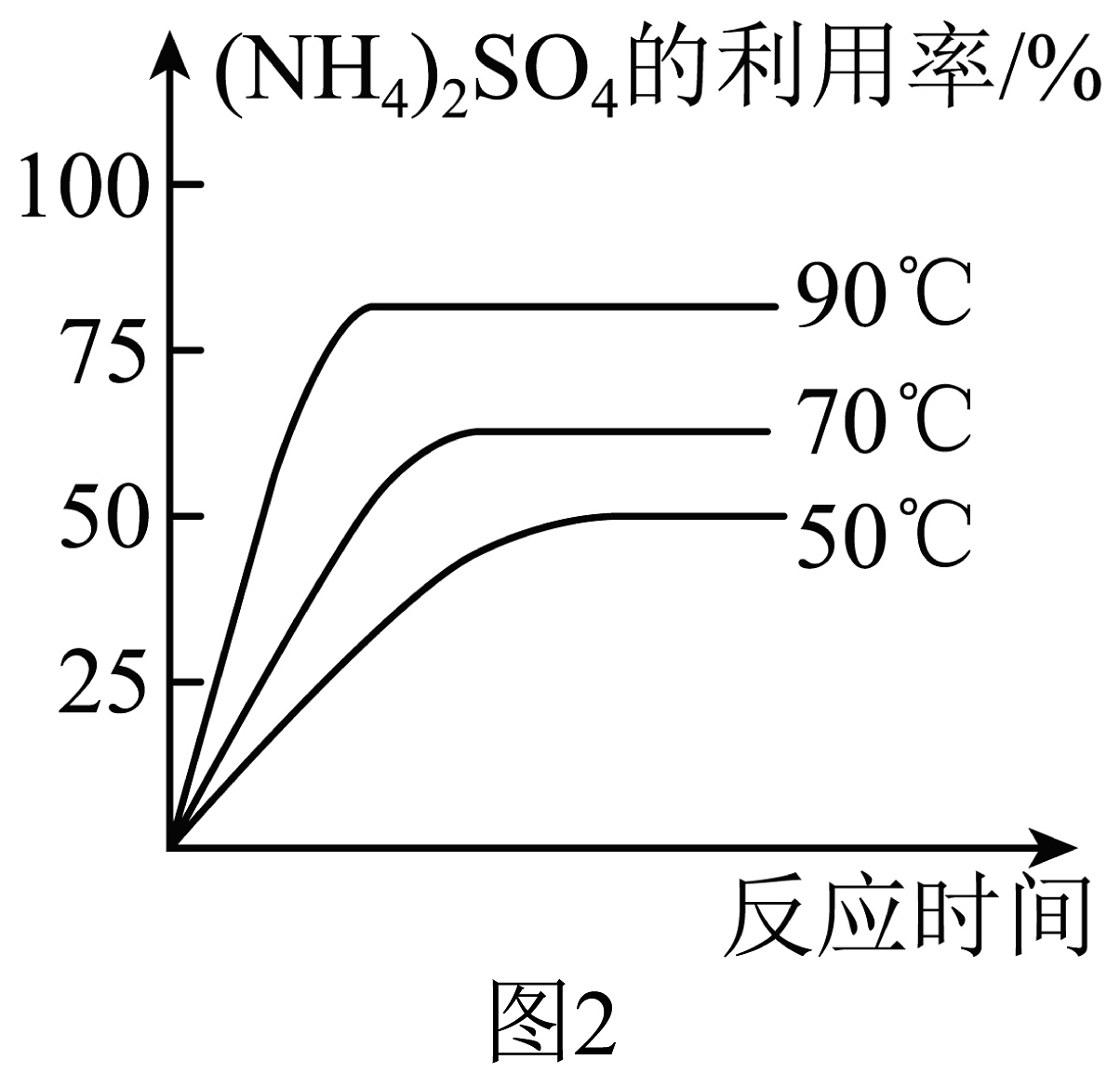 (6)、该流程中可循环利用的一种物质的化学式是。(7)、添加了氢氧化镁的沥青有阻燃作用,取等质量的基质沥青和添加了一定量氢氧化镁的阻燃沥青进行加热,结果如图3所示。其中表示阻燃沥青的是(选填“虚线”或“实线”),氢氧化镁的阻燃作用是利用氢氧化镁在该过程中发生分解反应,(选填“吸收”或“放出”)热量。
(6)、该流程中可循环利用的一种物质的化学式是。(7)、添加了氢氧化镁的沥青有阻燃作用,取等质量的基质沥青和添加了一定量氢氧化镁的阻燃沥青进行加热,结果如图3所示。其中表示阻燃沥青的是(选填“虚线”或“实线”),氢氧化镁的阻燃作用是利用氢氧化镁在该过程中发生分解反应,(选填“吸收”或“放出”)热量。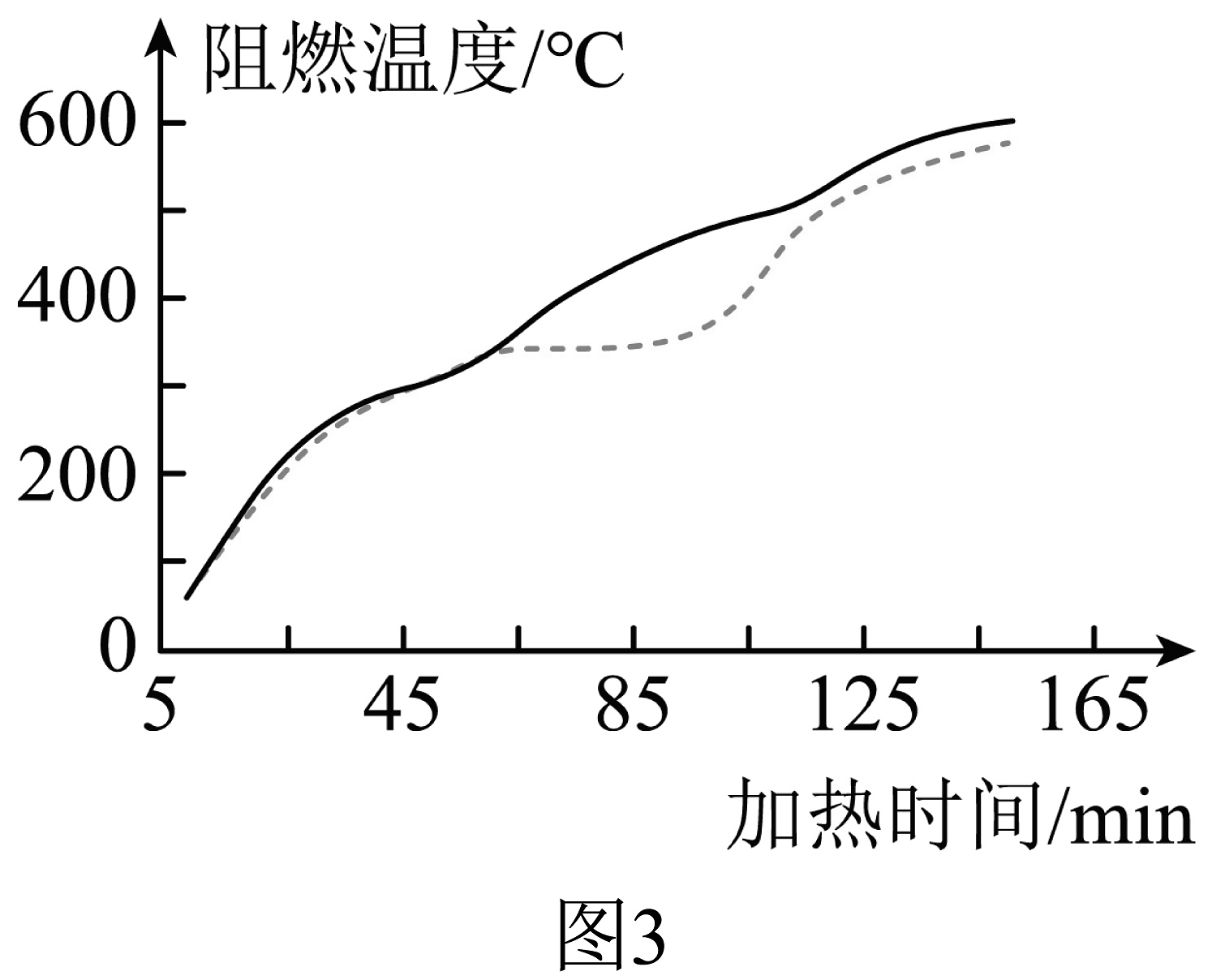
-
20、
金属蚀刻是通过曝光制版、显影后,将要金属蚀刻区域的保护膜去除,在金属蚀刻时接触化学溶液,达到溶解、腐蚀的作用,形成凹凸或者镂空成型的效果,最早可用来制造铜版、锌版等印刷凹凸版。
任务一:了解金属蚀刻画的制作原理
【查阅资料】金属蚀刻画所用的材料可以是金、银、铜、不锈钢、铝等金属。在金属蚀刻过程中,使用强酸溶液或某些盐溶液作腐蚀剂从而在金属表面留下痕迹。酸液温度稍高,可以提高金属溶解的速率,缩短蚀刻时间。但酸液温度过高容易使防护的涂层或耐蚀油墨软化甚至溶解,影响蚀刻画的效果。
(1)如果使用银板,则不能选择稀硫酸作蚀刻液,原因是。
任务二:模拟制作金属蚀刻画
【进行实验】根据制作金属蚀刻画的原理,化学兴趣小组同学设计了如图所示两个实验进行制作。
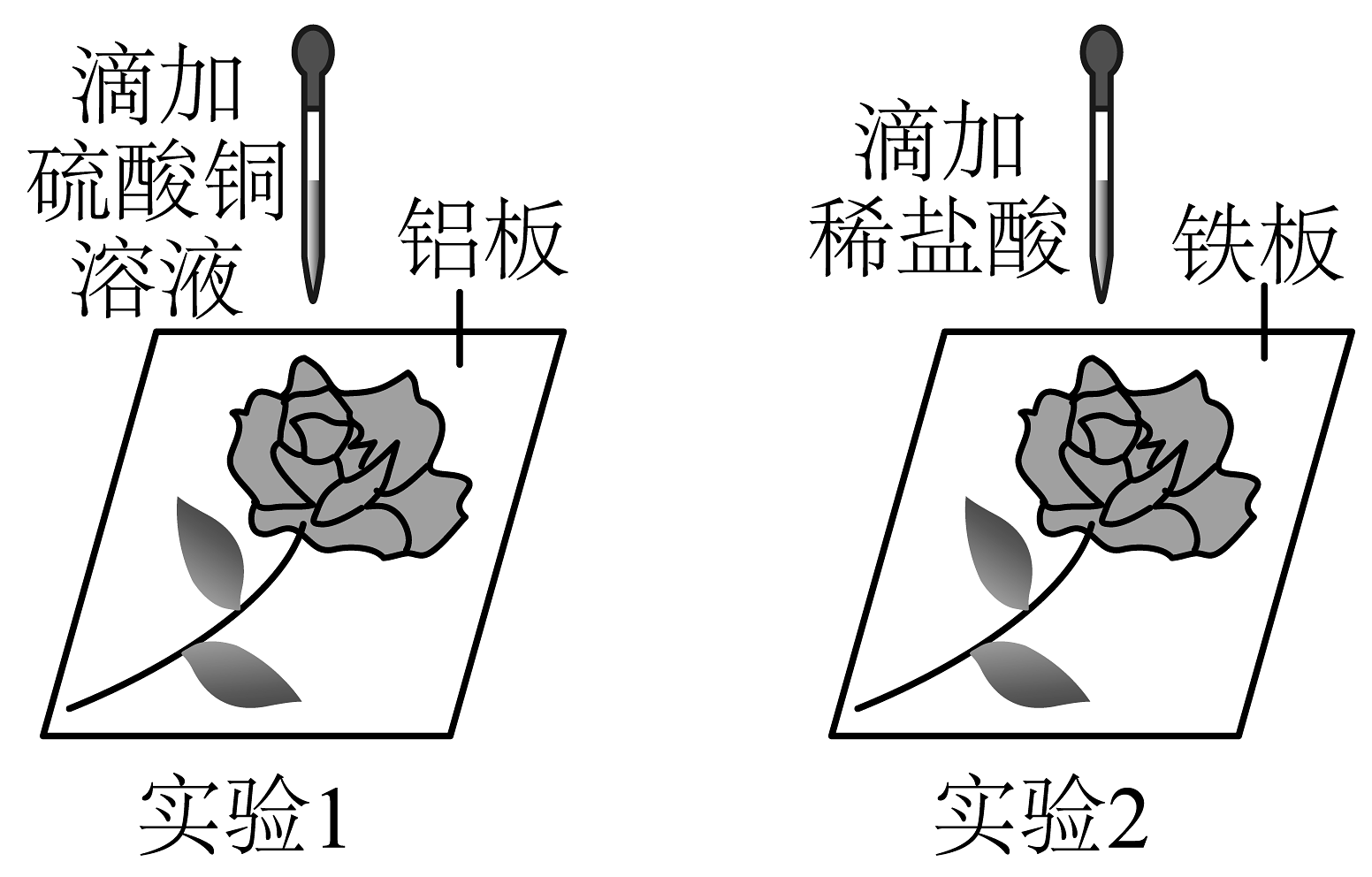
(2)实验1首先要对铝板进行打磨,其目的是;所得铝板蚀刻画中“玫瑰花”的颜色为。
【提出问题】实验2中清洗铁板后的废液的溶质成分是什么?
【作出猜想】
(3)废液的溶质中一定含有(填化学式),可能含有HCl。
【实验探究】
(4)化学兴趣小组设计了如下方案进行探究:
实验操作
实验现象
实验结论
①取少量红棕色氧化铁粉末于试管中,向其中加入足量废液
红棕色固体消失
废液中含有HCl
②另取少量废液于试管中,滴加几滴硝酸银溶液
废液中含有稀盐酸
【反思评价】
(5)操作①中发生反应的化学方程式为。
(6)老师对操作②结论的严谨性提出疑问,理由是。
【拓展与延伸】
(7)成功制作金属蚀刻画除了选择合适的材料和蚀刻液种类之外,还要注意控制的条件是(写一点即可)。