-
1、建立宏观、微观和符号之间的相互联系是化学学科的特点。
 (1)、图1表示锂原子与乙原子形成化合物丙的微观过程。
(1)、图1表示锂原子与乙原子形成化合物丙的微观过程。①该过程中锂原子通过(填“得到”或“失去”)电子形成锂离子。
②若乙原子核内质子数为17,写出化合物丙的化学式。
(2)、图2表示水、二氧化碳和氧气的循环图。从宏观角度看,图中三种物质的组成中都含有 , 从微观角度看,图中三种物质都是由(填“分子”、“原子”或“离子”)构成的。(3)、图3是铟元素在元素周期表中的部分信息,铟原子核外电子数是 , 铟在周期表中位于第周期元素。 -
2、化学与我们的生活有着密切的联系。现有①氧气;②氮气;③酒精;④二氧化硫;⑤稀有气体;⑥澄清石灰水;从中选择恰当的物质填空(填序号)。(1)、可用作燃料的是________;(2)、可用于检验二氧化碳气体的是________;(3)、可用于生产氮肥的是________;(4)、可用于医疗急救的是________;(5)、属于空气污染物的是________;(6)、可用于制作霓虹灯的是________。
-
3、化学用语是学习化学的重要工具。请用化学用语表示。(1)、氖元素________;(2)、汞原子________;(3)、两个氮分子________;(4)、碳酸根离子________;(5)、五氧化二磷________;(6)、标出水中氧元素的化合价________。
-
4、下列图像能正确反映对应变化关系的是
 A、用等质量的过氧化氢溶液制取氧气 B、密闭装置中一定质量的硫在过量的氧气中燃烧 C、在密闭容器中用过量红磷测定空气中氧气的含量 D、水的电解
A、用等质量的过氧化氢溶液制取氧气 B、密闭装置中一定质量的硫在过量的氧气中燃烧 C、在密闭容器中用过量红磷测定空气中氧气的含量 D、水的电解 -
5、下列实验方案合理的是
选项
实验目的
实验方案
A
鉴别和
用点燃的木条伸入气体中
B
实验室鉴别食盐水和白糖水
尝味道
C
证明蜡烛燃烧产物中有水
在蜡烛燃烧的火焰上方罩一个干冷的小烧杯
D
检验氧气是否集满
将带火星的木条伸入集气瓶内,观察是否复燃
A、A B、B C、C D、D -
6、逻辑推理是化学学习中常用的思维方法,下列推理正确的是A、阴离子是带负电荷的粒子,则带负电荷的粒子一定是阴离子 B、同种元素原子含有相同质子数,故质子数相同的粒子一定是同种元素的原子 C、化合物中金属元素显正价,则非金属元素一定显负价,且化合价的代数和为零 D、化学变化中分子种类发生改变,则分子种类发生改变的变化一定是化学变化
-
7、如图是铜元素和硫元素常见的化合价坐标图,C处表示的化合物的化学式是
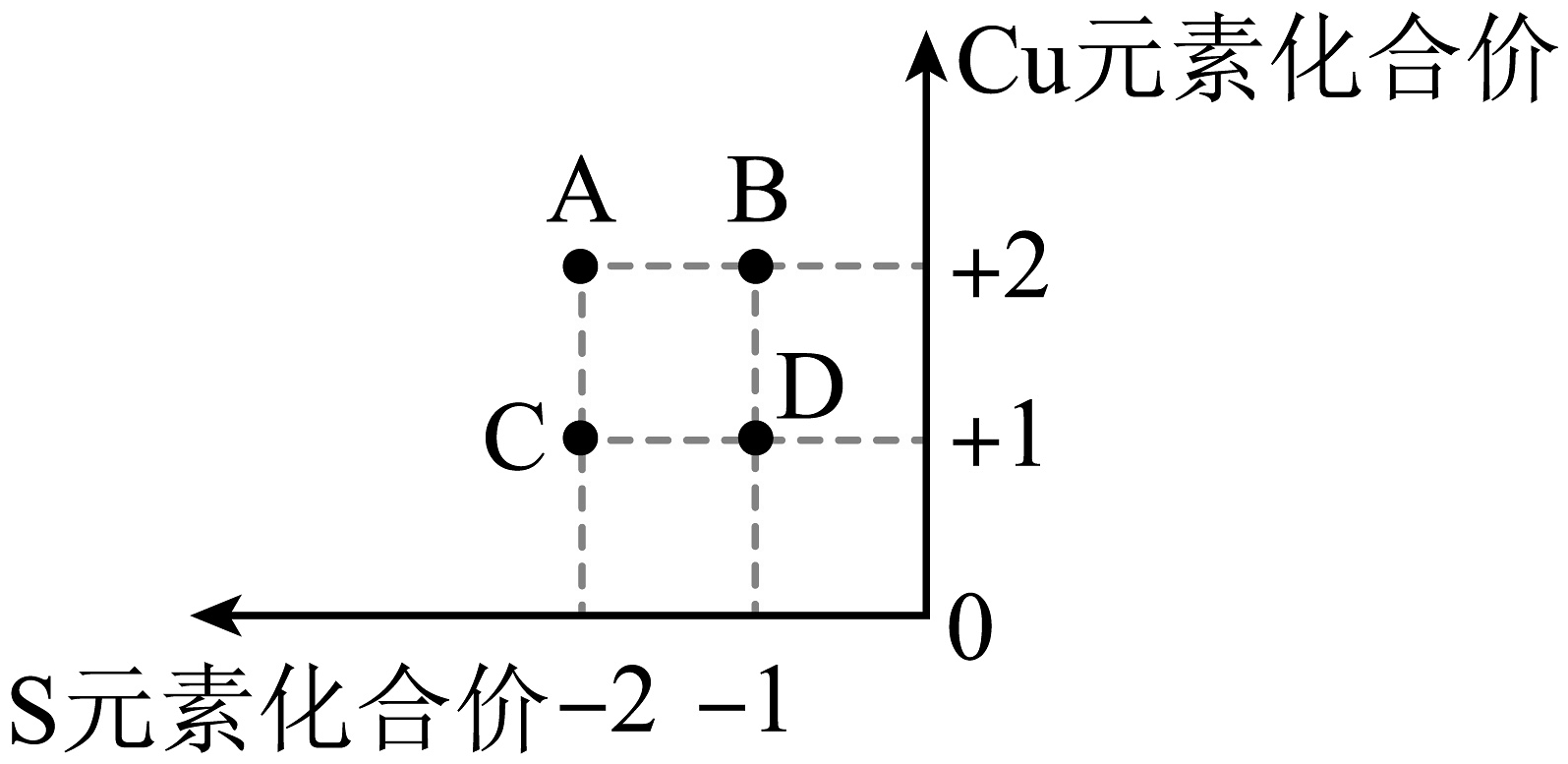 A、CuS B、Cu2S C、CuS2 D、Cu2S2
A、CuS B、Cu2S C、CuS2 D、Cu2S2 -
8、如下图为某反应的微观示意图,关于该反应的说法错误的是
 A、该反应中元素化合价没有发生改变的 B、反应前后原子的种类和数目没有改变 C、反应前后催化剂质量和化学性质不变 D、生成物丙和丁都属于氧化物
A、该反应中元素化合价没有发生改变的 B、反应前后原子的种类和数目没有改变 C、反应前后催化剂质量和化学性质不变 D、生成物丙和丁都属于氧化物 -
9、下列各组物质中,前者属于混合物,后者属于纯净物的是A、氮气、 B、冰水共存物、氧化汞 C、液氧、纯净的矿泉水 D、澄清石灰水、高锰酸钾
-
10、下列有关实验现象的描述中,错误的是A、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 B、硫在氧气中燃烧,产生淡蓝色火焰,生成二氧化硫 C、测定空气中氧气含量的实验里,红磷燃烧产生大量白烟 D、氢气在空气中燃烧产生淡蓝色火焰,在火焰上方罩一干冷烧杯,内壁出现水雾
-
11、下列符号能表示单质,又能表示元素,还可以表示一个原子的是A、H B、3Fe C、Cu D、
-
12、生命至上,安全第一。下列说法正确的是A、加热后的试管,立即用冷水冲洗 B、闻气体气味时,将鼻孔凑近集气瓶口 C、点燃氢气前应检验其纯度,点燃其他可燃性气体也需要检验纯度 D、不慎碰倒了酒精灯,酒精在实验台上燃烧起来,应立即用水浇灭
-
13、铁、铜是两种不同的元素,那么决定元素种类的是A、质子数 B、中子数 C、电子数 D、最外层电子数
-
14、物质的性质决定其用途,下列物质的用途只是利用其物理性质的是A、煤气做燃料 B、氧气用于气割 C、活性炭用于吸附色素 D、过氧化氢用于制取氧气
-
15、“空气炸锅”的工作原理是将锅内空气加热后循环吹向食物,则得环气体中含量最高的是A、 B、 C、 D、
-
16、我国向全世界宣示,二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和。下列不利于碳中和的做法的是A、直接焚烧秸秆 B、出行乘坐公共交通 C、节约用纸 D、随手关灯
-
17、水是地球上最常见的物质之一。(1)、自来水厂生成过程中,常用消毒剂(如等)杀菌消毒,家用净水器中选用活性炭来水中异味。(2)、在干燥的烧杯中进行如图所示实验,观察到________。
 (3)、电解水的实验中产生了氢气和氧气的体积比为。可以计算每电解产生4g氢气,生成mol氧气。(4)、将足量水蒸气通入灼热的铁中,最终铁全部转化为一种含铁的氧化物M,并生成H2。设计实验确认M的化学式,需获取的实验数据及计算所需数据有________。
(3)、电解水的实验中产生了氢气和氧气的体积比为。可以计算每电解产生4g氢气,生成mol氧气。(4)、将足量水蒸气通入灼热的铁中,最终铁全部转化为一种含铁的氧化物M,并生成H2。设计实验确认M的化学式,需获取的实验数据及计算所需数据有________。 -
18、为探究碳粉和氧化铜反应时最佳质量比,取不同质量比的干燥混合物进行系列实验。
序号
碳粉与氧化铜的质量比
充分反应后,生成物的颜色、状态
Ⅰ
1:10
生成有金属光泽的红色固体
混有少量___________物质
Ⅱ
1:11
混有极少量黑色物质
Ⅲ
1:12
无黑色物质
Ⅳ
1:13
混有较多黑色物质
(1)、补全化学方程式;C+CuO+CO2↑。
(2)、补全实验I的实验现象:混有少量物质,该物质的主要成分为。(3)、最佳质量比为 , 没有必要进行质量比为1:14的实验,理由是。 -
19、生活、生产中有时需要用到高浓度O2。(1)、氧气瓶中的O2 , 一般利用物质的沸点差异,从液态空气中分离出O2 , 这是利用了物质的________(选填“物理性质”或“化学性质”)。(2)、实验室常用加热氯酸钾和二氧化锰的混合固体来制取氧气,该反应的化学方程式是 , 试管口应 , 可选用一种氧气的收集方法是(选填“向上排气法”、“向下排气法”或“排水集气法”),这是应用了氧气物理性质中的。(3)、家庭制氧机如图所示。将A(过碳酸钠白色固体)和B(二氧化锰黑色粉末)放入水中产生氧气。反应时放热,反应仓内黑色粉末翻腾。反应仓中过碳酸钠(2Na2CO3·3H2O2)易溶于水,在水中会生成Na2CO3和H2O2 , H2O2在MnO2的作用下产生O2 , 反应后Na2CO3溶液的pH(选填“>”、“<”或“=”)7,过滤仓中水的作用是。
 (4)、分子筛式制氧机是一种利用分子筛的吸附特性,从空气中分离制取高纯度氧气的设备。在一定条件下分别将N2、O2通过某种分子筛,测定其对N2、O2的吸附量,结果如图所示(纵坐标数值越大,代表吸附量越大)。请结合图中数据分析,25℃时吸附压越大越有利于分离N2和O2的原因是________。
(4)、分子筛式制氧机是一种利用分子筛的吸附特性,从空气中分离制取高纯度氧气的设备。在一定条件下分别将N2、O2通过某种分子筛,测定其对N2、O2的吸附量,结果如图所示(纵坐标数值越大,代表吸附量越大)。请结合图中数据分析,25℃时吸附压越大越有利于分离N2和O2的原因是________。
-
20、海水是宝贵的自然资源,从海水中提取食盐的主要过程如图1。
 (1)、在蒸发池内,海水经过风吹日晒,除去了大量(选填“溶质”或“溶剂”),最终得到的母液是氯化钠的(选填“饱和溶液”或“不饱和溶液”),上述过程利用的是(选填“降温结晶”或“蒸发结晶”)的方法。(2)、粗盐中除了氯化钠外,还含有少量泥沙等杂质。下表是氯化钠的溶解度,设计实验提纯30.0g粗盐。
(1)、在蒸发池内,海水经过风吹日晒,除去了大量(选填“溶质”或“溶剂”),最终得到的母液是氯化钠的(选填“饱和溶液”或“不饱和溶液”),上述过程利用的是(选填“降温结晶”或“蒸发结晶”)的方法。(2)、粗盐中除了氯化钠外,还含有少量泥沙等杂质。下表是氯化钠的溶解度,设计实验提纯30.0g粗盐。温度(℃)
0
10
20
40
溶解度(g/100g水)
氯化钠
35.7
35.8
36.0
36.4
①称量30.0g粗盐,用(选填“10mL”、“50mL”或”100mL”)量筒量取一定量蒸馏水,将两者依次转移至(选填“50mL”、“100mL”或“250mL”)烧杯,充分搅拌溶解:
②搭建过滤装置,用烧杯(如图2)承接滤液,漏斗下端应位于该烧杯(选填或“a”、“b”或“c”)处附近,过滤引流时,玻璃棒紧靠漏斗(如图3)内三层滤纸的(“x”、“y”或“z”)处附近:

③搭建蒸发装置,将滤液转移至蒸发皿,蒸发滤液,当时停止加热;
④将所得固体转移至试剂瓶,请在图4中书写该试剂瓶的标签。
