相关试卷
- 广东省清远市2016-2017学年九年级化学一模考试试卷
- 广西钦州港经济开发区2015-2016学年九年级上学期化学期末考试试卷
- 广西北海市合浦县教育局教研室2013-2014学年九年级上学期化学期末考试试卷
- 广西北海市合浦县2012-2013学年九年级上学期化学期末考试试卷
- 广东省肇庆市鼎湖中学2017-2018学年九年级上学期化学期中考试试卷
- 2016年广西钦州市中考化学试题
- 2015年广西钦州市中考化学试卷
- 广西桂林市灌阳县2015-2016学年九年级上学期化学期中考试试卷
- 广西桂林市灌阳县2015-2016学年九年级上学期化学期中考试试卷
- 广西钦州地区2016-2017学年九年级化学中考模拟考试试卷
-
1、规范的实验操作是实验成功和安全的重要保证。下列实验操作正确的是A、
 倾倒液体
B、
倾倒液体
B、 取用固体
C、
取用固体
C、 点燃酒精灯
D、
点燃酒精灯
D、 液体加热
液体加热
-
2、武汉美食享誉全国。以下制作过程中发生化学变化的是A、糯米酿酒 B、包鸡冠饺 C、刀切豆皮 D、拌热干面
-
3、构成物质的微粒有分子、原子、离子等。下列物质由离子构成的是A、
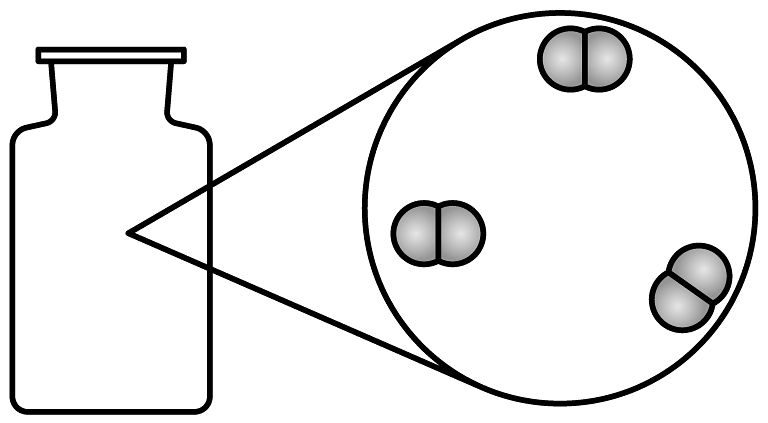 氮气
B、
氮气
B、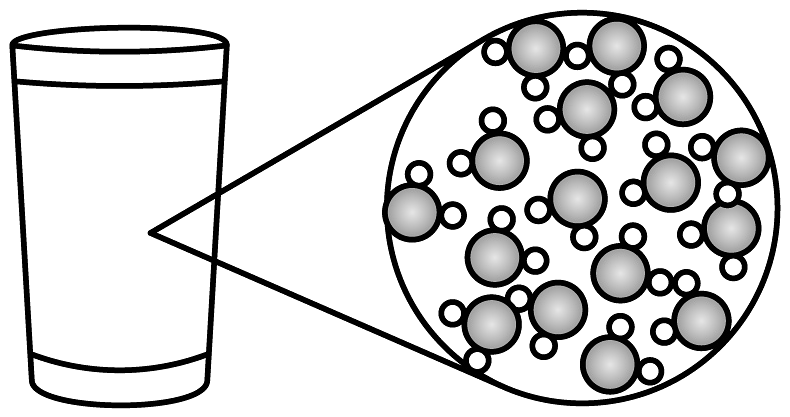 水
C、
水
C、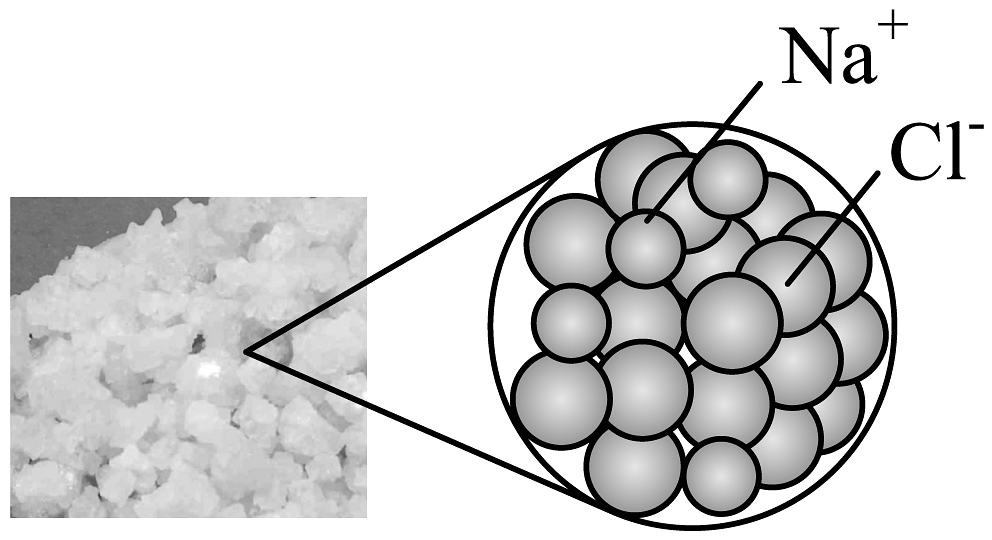 氯化钠
D、
氯化钠
D、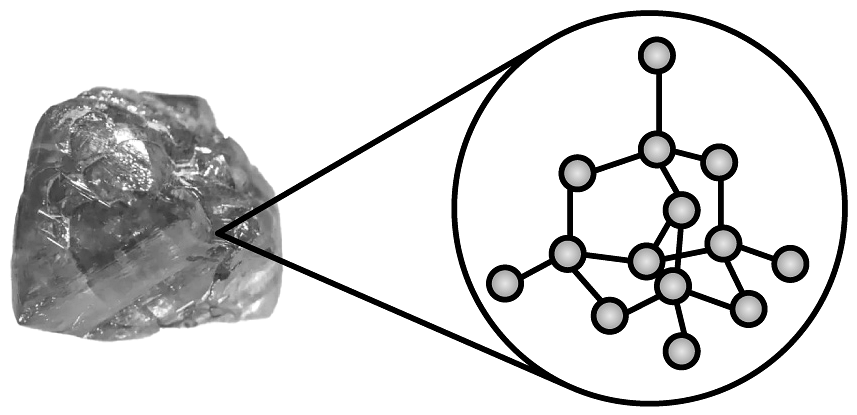 金刚石
金刚石
-
4、
自热食品中的发热包浸泡在水中即可发热。下图为某食品发热包的标签,化学兴趣小组为解密发热包展开项目式学习活动。
【品名】食品发热包 【主要成分】氧化钙、铝粉、碳酸钠 【净含量】
【使用方法】撕开塑料袋后加常温水发热 【贮存条件】存放于阴凉干燥处
【注意事项】使用时有气体产生,要远离明火,严禁在密闭场所中使用
资料1:;
资料2:发热包发热温度能保持在以上分钟;
任务一,认识发热包的主要成分
(1)氧化钙:氧化钙与水反应放出热量,写出该反应的化学方程式:。
(2)碳酸钠:在碳酸钠溶液中加入无色酚酞,可以观察到的现象是。

任务二:探究发热包可以持续发热的原理
小组同学分别取不同样品,各加水,用数字化实验获得如下曲线图(图1):
【分析得出结论】
(3)发热包可以持续发热的原理是。
任务三:自制发热包
兴趣小组将碳酸钠粉末、氯化钙粉末(稍过量)、铝粉混合均匀配成50克的自制发热包,倒入无纺布袋中后封口。小组同学将自制发热包放入烧杯,加常温水,并用温度传感器和传感器进行测量,结果如图2所示,观察有大量气泡产生。
(4)内,先降低后升高的原因是。
(5)根据检测结果,该自制发热包不能达到专用发热包的效果。小组同学提出可能是物质的质量比不恰当导致的。请通过计算说明铝粉、生石灰、碳酸钠的质量比理论上应是。
【拓展延伸】
(6)使用发热包时,撕开外包装塑料袋,检查装有发热粉的无纺布袋无破损后,放入凉水中。使用后妥善处理发热包。试推测无纺布应具备的性质(答一条即可)。
任务三:发热包使用过程中的注意事项及使用后的处理方法。
(7)使用过程中不能加入开水,请结合燃烧的条件分析可能的原因:。
(8)使用后的废液含有氢氧化钠、碳酸钠等物质,不能直接扔掉。请写出合适的处理法。
-
5、
金属材料承载人类文明进程。及其合金是人类使用最早的金属材料。
资料:①孔雀石的主要成分为[],受热易分解得到三种氧化物。
②镍是一种银白色金属,可与酸反应,生成绿色的溶液。
Ⅰ:古代金属成就

(1)《梦溪笔谈》记载了古代劳动人民冶炼青铜器的工艺(如图1)。整个工艺过程中至少发生个反应,其中得到铜的化学反应方程式为。
(2)古籍记载镍白铜(主要成分为)是中国古代发明和研制出的铜合金。为探究的金属活动性,某同学设计了实验(如图2)。试管①中的现象为 , 反应的化学方程式。若要确定镍、铜、锌的活动顺序,请写出能达到实验目的的试剂X和Y。
Ⅱ:探秘铜的锈蚀
(3)青铜器在含有的环境中容易生成铜锈【】,其产生过程如图3所示。过程②中与水反应的化学方程式为 , X的化学式为;过程③中,部分在酸性溶液中,吸收一种常见气体 , 形成疏松多孔的铜锈 , 加快铜的锈蚀。
(4)通过对青铜器锈蚀的探究可知,铜制品锈蚀的原理是。
-
6、山西运城“五步产盐法”属于国家级非物质文化遗产。盐湖(卤水)中溶质的主要成分为碳酸钠,其次是氯化钠和硫酸镁。下图是“五步产盐法”的流程图(图1)及相关物质的溶解度曲线(图2)。
资料1:箩的形成——当卤水达到一定浓度时,低温析芒硝(硫酸钠)于池底,形成硝板,(有大量的筛孔,可以作为“箩”)。以上时,卤水中的和少量残余形成块状白钠镁矾,过箩就是将卤水通过“硝板”,可以起到除杂和提纯效果。
资井2:储卤——将多次过“箩”的液体,提送到储卤畦储存,作为产盐主原料储备。
 (1)、写出一种卤水中的溶质:。(2)、盐池充分利用四季温度变化,冬季产硝(硫酸钠),夏季产盐()。请结合图2分析,冬季只析出硫酸钠(固体A)的根本原因是。此时溶液B中硫酸钠的状态对应图2中的(填“a”、“b”或“c”)点。
(1)、写出一种卤水中的溶质:。(2)、盐池充分利用四季温度变化,冬季产硝(硫酸钠),夏季产盐()。请结合图2分析,冬季只析出硫酸钠(固体A)的根本原因是。此时溶液B中硫酸钠的状态对应图2中的(填“a”、“b”或“c”)点。 (3)、第Ⅱ步的“过箩除杂,相当于化学实验操作。(4)、第Ⅰ步“集卤蒸发”和第Ⅳ步“结晶”都需要蒸发水,但作用不同,请分析其作用:。(5)、结合“五步产盐法”的过程,你认为五步产盐法的优点有哪些?(填一种即可)。
(3)、第Ⅱ步的“过箩除杂,相当于化学实验操作。(4)、第Ⅰ步“集卤蒸发”和第Ⅳ步“结晶”都需要蒸发水,但作用不同,请分析其作用:。(5)、结合“五步产盐法”的过程,你认为五步产盐法的优点有哪些?(填一种即可)。 -
7、实验是学习化学的重要途径,某同学欲制备并收集一定体积的气体供实验室使用。请回答下列问题:
 (1)、实验室用高锰酸钾制取氧气,应选择的发生装置为(填字母),其反应的化学方程式为 , 基本反应类型为。(2)、实验室用大理石和稀盐酸制取二氧化碳,收集装置可用(填字母),其反应的化学方程为。(3)、图4实验,紫色纸花变红,(能或不能)证明与水反应生成碳酸;两支蜡烛由下到上先后熄灭,体现的化学性质是。(4)、设计并制作家用便携式简易供氧器(如图5),验证导出气体是氧气的方法是。用过氧化氢溶液和过碳酸钠固体两种制氧剂于反应器中制取氧气,相同条件下分别测定产生氧气后气压随时间变化的情况、利用传心器采集数据入图6所示。结合图像及药品状态分析,家用供氧器选择过碳酸钠作制氧剂而不选择过氧化氢溶液的理由是。
(1)、实验室用高锰酸钾制取氧气,应选择的发生装置为(填字母),其反应的化学方程式为 , 基本反应类型为。(2)、实验室用大理石和稀盐酸制取二氧化碳,收集装置可用(填字母),其反应的化学方程为。(3)、图4实验,紫色纸花变红,(能或不能)证明与水反应生成碳酸;两支蜡烛由下到上先后熄灭,体现的化学性质是。(4)、设计并制作家用便携式简易供氧器(如图5),验证导出气体是氧气的方法是。用过氧化氢溶液和过碳酸钠固体两种制氧剂于反应器中制取氧气,相同条件下分别测定产生氧气后气压随时间变化的情况、利用传心器采集数据入图6所示。结合图像及药品状态分析,家用供氧器选择过碳酸钠作制氧剂而不选择过氧化氢溶液的理由是。 -
8、雷雨天气后,空气中部分氧气会转变为臭氧()。是一种有鱼腥气味的气体,能吸收来自太阳的紫外线,保护地面生物不受伤害,同时还可降解水中的有机污染物,净化水体。(1)、臭氧与氧气性质不同的原因是。(2)、人工制取的装置和反应的微观示意图如图1和图2所示。在转变为的过程中,未发生改变的是。
 (3)、请写出转变为的化学反应方程式。若要制得 , 理论上需消耗的质量为。(4)、降解水中污染物时采用一次性投加的方式。实验发现,温度升高,相同时间内有机物降解率降低。可能的原因是。
(3)、请写出转变为的化学反应方程式。若要制得 , 理论上需消耗的质量为。(4)、降解水中污染物时采用一次性投加的方式。实验发现,温度升高,相同时间内有机物降解率降低。可能的原因是。 -
9、“林城叠翠秀黔中,甲秀清波映古风,青云烟火味无穷”,欢迎来到爽爽的贵阳。(1)、林城叠翠——黔中氧吧焕生机。树木生长需要养分,若叶色发黄,可以施用肥(填化肥种类);腐烂的枯叶也可以为树木提供一定的养料,枯叶腐烂属变化(填“物理”或“化学”)。(2)、甲秀南明——白石筑桥连两岸。甲秀楼前,以白色大理石()建成的浮玉桥连接南明河两岸,中碳元素的化合价为 , 南明河水净化过程中可以采取的方法是(填一种即可)。(3)、青云飘香——夜市烟火引客来。走进市集,迎面而来的是食物香气。能闻到食物香气,微观原因是。贵阳特色美食酸粉在食用时要添加铁强化酱油,可以为人体补充元素,预防贫血。
-
10、是发酵粉的主要成分,加热后充分分解所得剩余固体为 , 常用于制作糕点、馒头的发泡剂。某同学为探究发酵粉样品中的质量分数,他取样品 , 用下图实验步骤进行探究(假设样品中除之外的杂质成分加热不发生变化,也不与盐酸反应,直接进入固体B中)。下列判断正确的是
 A、加热后的生成物有和两种 B、加热后固体减少的质量等于产生的质量 C、固体A中含有的质量为 D、发酵粉样品中的质量分数为
A、加热后的生成物有和两种 B、加热后固体减少的质量等于产生的质量 C、固体A中含有的质量为 D、发酵粉样品中的质量分数为 -
11、下列实验设计不能达到实验目的的是
选项
实验目的
实验设计
A
鉴别稀盐酸和溶液
取样,分别滴入紫色石蕊溶液
B
配制溶质质量分数为的氯化钠溶液
向盛有氯化钠固体的烧杯中,加入水,搅拌
C
除去固体中的少量
向样品中加入适量稀盐酸,蒸发结晶
D
证明氢氧化钠溶液与稀盐酸能反应
取适量氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液振荡,再滴入稀盐酸至溶液变为无色
A、A B、B C、C D、D -
12、下列对化学核心素养的认识正确的是A、化学观念:物质都是由微观粒子构成的,所以物质都是由分子或原子构成的 B、科学思维:离子是带电的微粒,则所有带电的微粒都是离子 C、科学探究与实践:酸能使石蕊溶液变红,将通入石蕊溶液,石蕊溶液变红,则是酸 D、科学态度与责任:化石燃料是有限的,我们应大力开发新能源燃料
-
13、下列物质的性质和用途对应关系正确的是A、铜呈紫红色,可用作导线 B、浓硫酸具有强腐蚀性,常用作干燥剂 C、活性炭具有吸附性,常用作冰箱除味剂 D、氢氧化钠具有碱性,用于治疗胃酸过多
-
14、2025年,我国自主研发的“生物基聚乳酸”( , 化学式为)被广泛用于替代传统塑料。以下关于的说法正确的是A、属于天然有机高分子材料 B、由碳、氢、氧三种元素组成 C、由3个碳原子、4个氢原子和2个氧原子构成 D、中氢元素的质量分数最大
-
15、2024年12月,国务院印发《“无废城市”建设深化行动方案》,要求到2025年实现生活垃圾回收利用率超。以下做法中不符合该方案环保理念的是A、焚烧塑料垃圾 B、积极开展植树造林活动 C、使用可降解餐具 D、开发使用新能源
-
16、某化学兴趣小组的同学为测定某工厂废水中盐酸的含量,进行了如下实验:取146g废水于烧杯中,加入80g溶质质量分数为13.25%的碳酸钠溶液,恰好完全反应(废水中的其他成分不与碳酸钠反应)。(1)、若要配制80g溶质质量分数为的碳酸钠溶液,需要碳酸钠固体的质量。(2)、该废水中盐酸的溶质质量分数。(3)、完全反应后,所得溶液的溶质质量分数(结果保留至)。
-
17、人体缺锌式可在医生指导下通过服用葡萄糖酸锌( , 相对分子质量为455)口服液来补锌。(1)、组成葡萄糖酸锌的元素中
①属于非金属元素的有种;
②属于微量元素的是。
(2)、中碳、氢、氯、锌元素的原子个数比为。(3)、某葡萄糖酸锌口服液每支 , 每毫升含葡萄糖酸锌 , 则每支口服液中锌的含量是(用含V、x的代数式表示)。 -
18、小明发现家用清洁剂(主要含有氢氯化钠,其他成分不与盐酸反应)使用后常忘盖瓶盖,一段时间后清洁效果变差,猜测该清洁剂有部分变质为碳酸钠。为了探究该清洁剂的成分,他取一定量的该清洁剂样品,用传感器测定逐滴加入稀盐酸过程中(均常温下)的变化,测定结果如下图所示。
 (1)、变质原因及其验证方案
(1)、变质原因及其验证方案①用化学方程式表示氢氧化钠变质为碳酸钠的反应:。
②为了验证该猜想,可向少量样品加入(填一种试剂名称),若观察到有白色沉淀产生,则证明猜想成立。
(2)、a点处向待测样品中加入一种指示剂(填名称),溶液呈色。(3)、a至b阶段一定发生反应的化学反应方程式为。(4)、当时,溶液呈性,其中溶质为(填名称)。(5)、当进行到d点时,需向溶液中需加入一种廉价的常见物质进行处理,使其达到排放标准。写出该反应的化学方程式:。 -
19、某同学利用下列实验探究常见酸与碱的性质与用途。(1)、按图1所示实验,一段时间后,可观察到烧杯乙中红色溶液逐渐变浅。试剂X的名称为。由这一现象可得到的结论有(填字母)。

a.盐酸具有挥发性 b.能运动到空气中
c.烧杯乙溶液中钠离子数目变少了 d.分子能运动到烧杯乙中
(2)、为从微观粒子变化的角度理解图1中烧杯乙中发生的化学反应,在图2中画出乙中假设至恰好反应完全时的示意图。 (3)、该同学在观察到图1烧杯乙中溶液变浅红色时,猜测其中氢氧化钠是过量的,为进一步验证猜想,他取此时少量的样品于试管中,滴加试剂Y,有蓝色沉淀Z生成。
(3)、该同学在观察到图1烧杯乙中溶液变浅红色时,猜测其中氢氧化钠是过量的,为进一步验证猜想,他取此时少量的样品于试管中,滴加试剂Y,有蓝色沉淀Z生成。①推测试剂Y中的溶质所属物质类别是(填“酸”“碱”或“盐”);它可能是或或(填化学式);
②写出滴加试剂Y生成蓝色沉淀Z的化学方程式:;该反应类型为。
(4)、用的氢氧化钠溶液洗涤某石油样品中残余的硫酸,共消耗氢氧化钠溶液质量为 , 洗涤后的溶液呈中性。该石油样品中含的质量分数为。 -
20、我国某盐湖(湖水中主要含有)常采用“夏天晒盐,冬天捞碱”的传统工艺。结合下图所示溶解度曲线及所学知识,回答下列问题:
 (1)、夏天晒得的“盐”是指(填化学式),其分离方法是(填“蒸馏”“蒸发结晶”或“降温结晶”)。(2)、冬天捞“碱”时,湖水中溶质的溶解度较小的是(填化学式);所得的“碱”是指(填俗称),它所属物质类别是(填字母)。
(1)、夏天晒得的“盐”是指(填化学式),其分离方法是(填“蒸馏”“蒸发结晶”或“降温结晶”)。(2)、冬天捞“碱”时,湖水中溶质的溶解度较小的是(填化学式);所得的“碱”是指(填俗称),它所属物质类别是(填字母)。A.酸 B.碱 C.盐 D.化合物 E.纯净物
(3)、此工艺实现“盐”和“碱”的分离原理中,不涉及的性质是______(填字母)。A、溶解度受温度变化的影响不同 B、溶液酸碱性 C、溶解性(4)、假设在时实施“冬天捞碱”,对此时的湖水进行分析:
①湖水中一定饱和的溶质是(填名称)。
②一次性取湖水样品A于试管中,选择(现有可选择试剂有稀硫酸、稀硝酸、澄清石灰水、硝酸银溶液)适合的试剂,检验湖水中的主要酸根离子的种类。
i、滴入试剂2后,可观察到的现象为沉淀部分溶解、。
ii、写出试剂1的名称:、沉淀2的化学式:。
iii、结论:湖水样品A中含有的主要酸根离子有。