相关试卷
-
1、“类推”这种思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中错误的是( )
①钠与水反应生成NaOH和H2 , 所有金属与水反应都生成碱和H2 ②铁露置在空气中一段时间后就会生锈,性质更活泼的铝不能稳定存在于空气中 ③Al(OH)3、Cu(OH)2受热易分解,Fe(OH)3受热也易分解 ④不能用电解熔融的AlCl3来制取金属铝,也不能用电解熔融的MgCl2来制取金属镁
A、①④ B、②④ C、①②④ D、①②③④ -
2、、、 , 都是氯的常见氧化物,制备方法如下:
①
②
③
下列说法错误的是
A、反应①每生成0.5mol , 转移电子数约为 B、反应②中氧化剂与还原剂的物质的量之比为1∶1 C、是酸性氧化物,与水反应的离子方程式为 D、、均可用作消毒剂,自身会被还原为 , 则消毒能力是等质量的1.25倍 -
3、《自然》发表的关于乳酸的研究认为,乳酸是经血液循环转换能量的基本成员。常温下,乳酸(用表示)的 , 碳酸的。下列说法正确的是A、乳酸酸性比碳酸弱 B、乳酸溶液的 C、乳酸溶液中: D、稀释乳酸溶液,乳酸电离程度减小
-
4、“价—类二维图”是学习元素及其化合物知识的高效模型,有关氯的“价—类二维图”说法错误的是
 A、e的某种常见化合物可以用于实验室制备O2 B、将b通入盛有鲜花的试剂瓶,鲜花褪色,说明b具有漂白性 C、类比d的分子式,g的分子式为HClO4 , 是氯元素的最高价态化合物 D、84消毒液的有效成分是f的钠盐,作用原理是与空气中的水和二氧化碳反应生成d
A、e的某种常见化合物可以用于实验室制备O2 B、将b通入盛有鲜花的试剂瓶,鲜花褪色,说明b具有漂白性 C、类比d的分子式,g的分子式为HClO4 , 是氯元素的最高价态化合物 D、84消毒液的有效成分是f的钠盐,作用原理是与空气中的水和二氧化碳反应生成d -
5、NaCl是一种化工原料,可以制备一系列物质,如图所示。下列说法正确的是
 A、氢气和氯气混合光照时会产生苍白色火焰 B、石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 C、常温下干燥的Cl2能用钢瓶贮运,所以Cl2不能与铁反应 D、图示中涉及的反应都是氧化还原反应
A、氢气和氯气混合光照时会产生苍白色火焰 B、石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 C、常温下干燥的Cl2能用钢瓶贮运,所以Cl2不能与铁反应 D、图示中涉及的反应都是氧化还原反应 -
6、过氧化钙是一种安全无毒的物质,带有数量不等的结晶水,通常还含有部分。(1)、称取过氧化钙样品,灼热时发生如下反应:。得到的质量为 , 该样品中的物质的量为。(2)、另取同一样品 , 溶于适量的稀盐酸中,然后加入足量的溶液,将溶液中全部转化为沉淀,得到干燥的。
①样品中的质量为。
②样品中的x值为。
-
7、实验室中模拟工业上制取少量无水氯化铁的装置及操作如下。
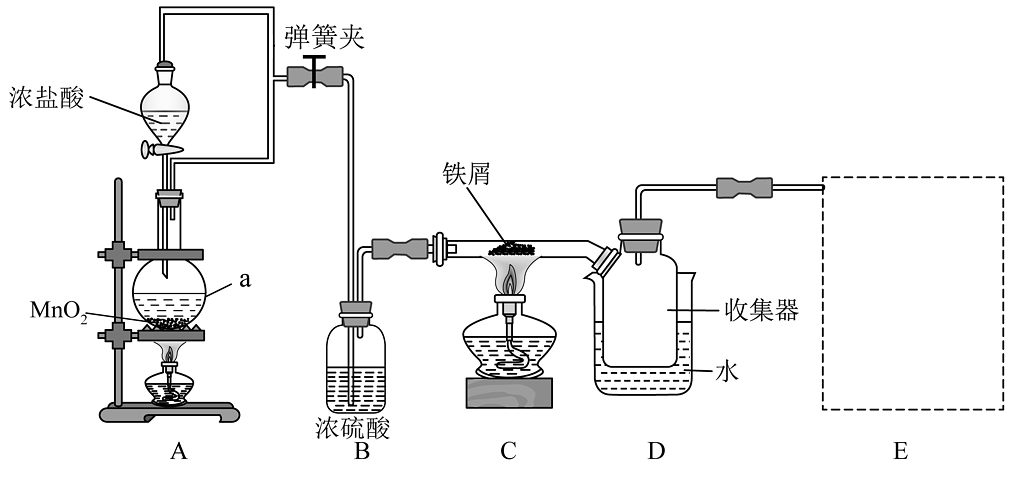
已知:无水遇水剧烈反应,加热易升华。请回答下列问题:
(1)、仪器a的名称是 , 装置A中反应的离子方程式为。(2)、装置C中硬质玻璃管内的实验现象为。(3)、下列有关说法正确的是_______。A、组装好仪器后,关闭弹簧夹,向分液漏斗中加水,打开漏斗的活塞,根据水是否持续流下来判断装置A的气密性 B、两处酒精灯加热的顺序为:先加热A处,再加热C处。 C、装置D中的水可用冷水或冰水,目的是更好地冷凝收集 D、E处虚线框内的装置可选用 或
或 (4)、实验结束后,在装置C的硬质玻璃管右侧内壁会有部分氯化铁残留,为提高氯化铁的收集率,应如何操作?。(5)、反应后的产物中可能会存在杂质,为减少该杂质的生成,对装置进行改进的方法是。
(4)、实验结束后,在装置C的硬质玻璃管右侧内壁会有部分氯化铁残留,为提高氯化铁的收集率,应如何操作?。(5)、反应后的产物中可能会存在杂质,为减少该杂质的生成,对装置进行改进的方法是。 -
8、现有未知成分的混合溶液,其中除了含有的外,还可能含有下列离子中的一种或几种:。现进行如下实验操作(每次实验所加试剂均过量):
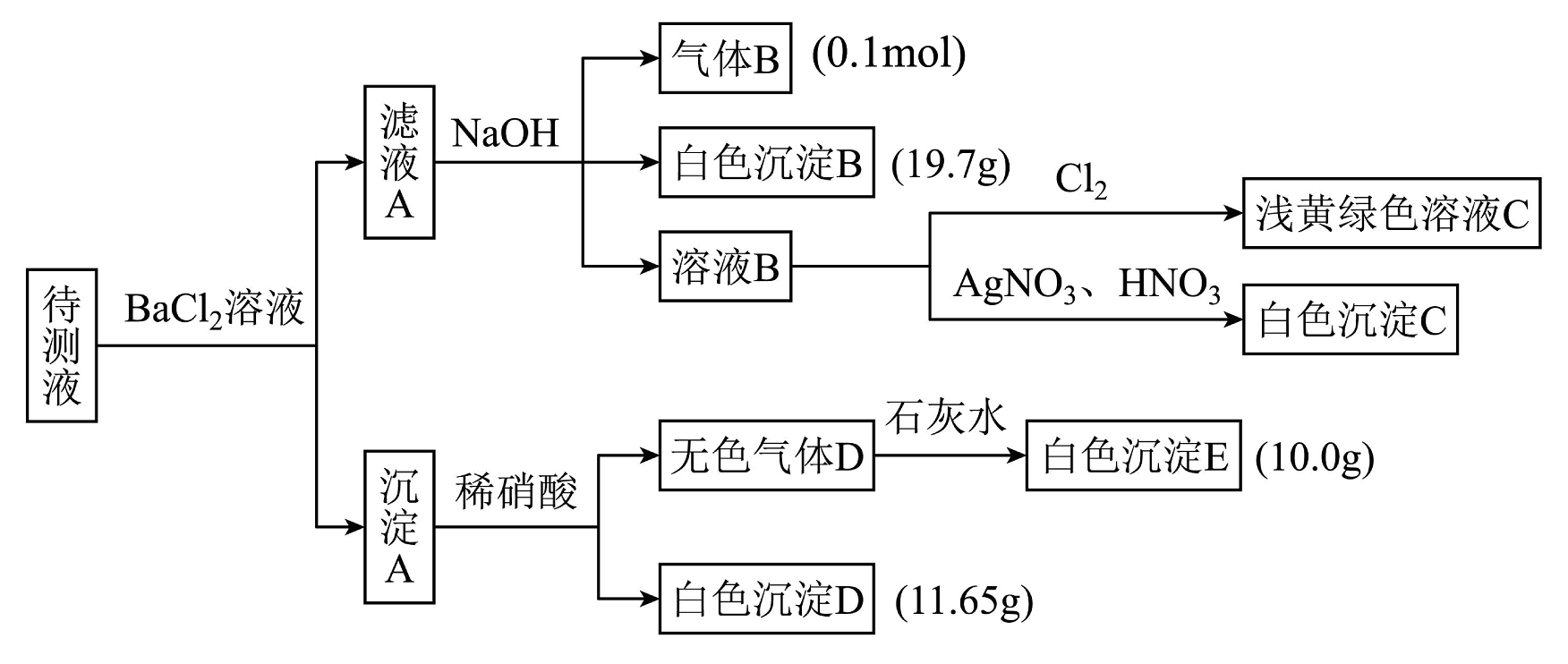
已知:在常温下是深红棕色液体,微溶于水,其水溶液为黄色。
(1)、由气体B可确定待测液中含有的离子是。(2)、由沉淀D和沉淀E可以判断待测液中一定含有离子,据此可以排除的离子是。(3)、由白色沉淀B可确定待测液中含有的离子是 , 写出产生沉淀B的离子方程式。(4)、设计实验方案确定原待测液中是否含。(5)、综合分析,此待测液中的物质的量(用字母a表示)取值范围为。 -
9、高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:。(1)、该反应的氧化剂是 , 氧化产物是。(2)、用单线桥标出该反应中电子转移的方向和数目。(3)、若反应转移的电子数为 , 则生成的物质的量为。(4)、已知高铁酸钠具有强氧化性,试分析其用于饮用水处理时的净水原理。(5)、制备高铁酸钠时,原料可用氯气与氢氧化钠反应制得(该反应为放热反应),若没有采取降温措施,会生成杂质。现将通入溶液中,反应得到的混合液,经测定与的的物质的量之比为 , 则与溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为。
-
10、按要求回答下列问题:(1)、的俗称。(2)、离子的摩尔质量。(3)、写出的电离方程式。(4)、漂白粉水溶液中通少量 , 反应的离子方程式。(5)、属于电解质的是(填序号,下同)属于非电解质的是。
①晶体;②盐酸;③液态醋酸;④;⑤干冰;⑥乙醇;⑦氯水;⑧熔化的
-
11、下列选项描述与对应图像相符的是
 A、图①为新制氯水在阳光直射时,溶液中浓度随着时间变化的曲线 B、图②为向与的混合溶液中滴加盐酸产生的图像 C、图③为向溶液中滴加溶液的导电性变化图像 D、已知还原性: , 图④为混合溶液,各离子物质的量随氯气通入的变化图像,b代表的是
A、图①为新制氯水在阳光直射时,溶液中浓度随着时间变化的曲线 B、图②为向与的混合溶液中滴加盐酸产生的图像 C、图③为向溶液中滴加溶液的导电性变化图像 D、已知还原性: , 图④为混合溶液,各离子物质的量随氯气通入的变化图像,b代表的是 -
12、下列实验操作、现象和结论均正确的是
操作
现象
结论
A
先滴加溶液再滴加溶液
生成白色沉淀
原溶液中有
B
将钠燃烧后的固体投入水中
有气体产生
固体产物中只有过氧化钠
C
用洁净铁丝蘸取溶液进行焰色反应
火焰呈黄色
原溶液中一定有 , 也可能有
D
滴加溶液,将湿润红色石蕊试纸置于试管口
试纸不变蓝
原溶液中无
A、A B、B C、C D、D -
13、代表阿伏加德罗常数的值。下列说法正确的是A、红热的铁丝与氯气充分反应,转移的电子数目为 B、将氯气溶于足量的水中,则该氯水中的和四种微粒的总数为 C、常温常压下,和的混合气体中含有个原子 D、质量分数为的乙醇水溶液中含有的氧原子数为
-
14、宇航装置中常用超氧化钾作吸收剂和供氧剂,反应方程式(未配平)为: , NA为阿伏加德罗常数的值。下列说法不正确的是A、晶体中离子的数目为 B、可用代替宇航装置中的 C、氧化剂与还原剂的物质的量之比为 D、该反应生成时转移个电子
-
15、下列化学或离子方程式书写正确的是A、钠与水反应离了方程式: B、碳酸钙和醋酸溶液反应离子方程式: C、氯气和水反应的离子方程式: D、向澄清石灰水中通入过量:
-
16、侯氏制碱法生产纯碱的主要流程如图所示,请结合流程图判断下列说法不正确的是
 A、该流程中未涉及氧化还原反应 B、该流程中可循环使用,副产品可作肥料 C、该流程中向饱和食盐水中先通至饱和,再通足量 D、沉淀池中发生反应的化学方程式为:
A、该流程中未涉及氧化还原反应 B、该流程中可循环使用,副产品可作肥料 C、该流程中向饱和食盐水中先通至饱和,再通足量 D、沉淀池中发生反应的化学方程式为: -
17、氯水中存在多种分子和离子,它们在不同的反应中表现出不同的性质。下列结论正确的是A、氯水中加入镁粉,片刻后气泡冒出,说明有存在 B、滴到淀粉—试纸上,先变蓝后褪色。其中褪色可能是由引起的 C、加入溶液,氯水的浅黄绿色消失,说明有存在 D、先加入盐酸酸化,再加入溶液,生成白色沉淀,说明有存在
-
18、为除去括号内的杂质,所选用的试剂或方法正确的是A、:升华法 B、:灼烧 C、固体(固体):加热 D、:通过饱和溶液的洗气瓶
-
19、在无色强碱性溶液中,下列各组离子能大量共存的是A、 B、 C、 D、
-
20、下列说法不正确的是A、实验室可以将未用完的钠放回原试剂瓶 B、进行焰色试验时如无铂丝,可用铁丝代替 C、蒸发结晶使用的蒸发皿一般可用明火直接加热 D、过滤时,用玻璃棒搅拌漏斗中的液体以加快过滤速度