相关试卷
-
1、实验室用6.5g锌和200mL稀硫酸反应制取氢气。若恰好完全反应时计算:(1)、写出H2SO4在水溶液中的电离方程式:。(2)、所用锌的物质的量:mol。(3)、在标准状况下产生氢气的体积:L。(4)、该硫酸溶液中H+物质的量浓度:mol/L。
-
2、分类法是一种简单易行的科学方法。现对Ca(ClO)2进行多角度分析并预测其性质。(1)、从组成特点分析,Ca(ClO)2属于(填“氧化物”、“酸”或“盐”)。(2)、Ca(ClO)2的水溶液可导电,Ca(ClO)2的电离方程式是。(3)、从Ca(ClO)2中Cl元素价态分析, Cl元素化合价为价。(4)、已知盐酸的酸性强于次氯酸,Ca(ClO)2可以和盐酸发生复分解反应,该反应的化学方程式为:。
-
3、在KCl、MgCl2、Mg(NO3)2形成的溶液中,c(K+)0.1mol/L,c(Mg2+)=0.15mol/L,c(Cl-)=0.2mol/L,则c(NO3-)为( )A、0.15 mol/L B、0.20 mol/L C、0.25 mol/L D、0.40 mol/L
-
4、焰火让国庆70周年联欢会更加辉煌壮观,这些五彩缤纷的焰火与元素的焰色反应有关。下列说法不正确的是A、观察K2SO4的焰色应透过蓝色的钴玻璃 B、Na与NaCl在灼烧时火焰颜色相同 C、可以用焰色反应来区别NaCl和KCl D、焰色反应一定发生化学变化
-
5、胶体区别于其他分散系最本质的特征是( )A、丁达尔现象 B、是混合物 C、较稳定 D、分散质粒子直径介于1 nm ~100nm
-
6、下列物质属于非电解质的是A、蔗糖溶液 B、CO2 C、Cu D、KOH
-
7、“g·mol-1”是一个物理量的单位,这个物理量是( )A、物质的量 B、摩尔质量 C、气体摩尔体积 D、物质的量浓度
-
8、空气中的自由电子附着在分子或原子上形成的空气负离子(也叫阴离子)被称为“空气维生素”。就是一种空气负离子,其摩尔质量为A、32g•mol﹣1 B、33g•mol﹣1 C、32g D、33g
-
9、下列物质与水反应生成强酸的是A、Na2O B、SO3 C、CO2 D、SiO2
-
10、萃取碘水中的碘,可采用的萃取剂是A、酒精 B、四氯化碳 C、醋酸 D、氢氧化钠溶液
-
11、生产、生活中离不开各类化学物质。下列物质中属于盐类的是A、生石灰 B、硫酸 C、胆矾 D、酒精
-
12、碳酸钾在火焰上灼烧时,透过蓝色钴玻璃观察火焰的颜色为A、黄色 B、紫色 C、绿色 D、红色
-
13、反应2NO+2CON2+2CO2可应用于汽车尾气的净化。下列判断正确的是A、该反应是置换反应 B、该反应是复分解反应 C、碳元素化合价降低 D、该反应是氧化还原反应
-
14、下列物质属于电解质的是A、铜 B、氯化钠溶液 C、熔融态硫酸钾 D、蔗糖
-
15、L/mol是哪个物理量的单位A、摩尔质量 B、体积 C、气体摩尔体积 D、密度
-
16、近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的(如图所示)。苯(
 )属于
)属于 A、氧化物 B、硫化物 C、无机物 D、有机物
A、氧化物 B、硫化物 C、无机物 D、有机物 -
17、化学与生活密切相关。下列生活中常见物质的俗名与化学式相对应的是A、苏打--NaHCO3 B、醋酸--C2H5OH C、明矾—KAl(SO4)2 D、生石灰—CaO
-
18、自然界含量最多的金属元素是A、氧 B、镁 C、铝 D、钠
-
19、我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、P、Al、Ni、Fe 等元素。回答下列问题:(1)、下列不同状态的硼中,失去一个电子需要吸收能量最多的是 (填标号)。
A.

B.

C.
 (2)、镍能形成多种配合物,其中Ni(CO)4是无色挥发性液体,K2[Ni(CN)4]是红黄色单斜晶体。K2[Ni(CN)4]的熔点高于Ni(CO)4的原因是。(3)、Al2O3的熔点(2054℃)很高,工业冶炼铝时要加入冰晶石(化学式为Na3AlF6)来降低生产成本,如下图所示为冰晶石的晶胞。用“
(2)、镍能形成多种配合物,其中Ni(CO)4是无色挥发性液体,K2[Ni(CN)4]是红黄色单斜晶体。K2[Ni(CN)4]的熔点高于Ni(CO)4的原因是。(3)、Al2O3的熔点(2054℃)很高,工业冶炼铝时要加入冰晶石(化学式为Na3AlF6)来降低生产成本,如下图所示为冰晶石的晶胞。用“ ”和“
”和“  ”代表Na+”或“AlF ”。图中“
”代表Na+”或“AlF ”。图中“  ”位于大立方体顶点和面心,“
”位于大立方体顶点和面心,“  ”位于大立方体的12条棱的中点和8个小立方体的体心。则大立方体的体心处△代表的微粒是(填“Na+”或“AlF”);与Na+距离相等且最近的Na+有个。
”位于大立方体的12条棱的中点和8个小立方体的体心。则大立方体的体心处△代表的微粒是(填“Na+”或“AlF”);与Na+距离相等且最近的Na+有个。
-
20、
根据物质的结构特点,回答以下问题。
I.磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。回答下列问题:
(1)在周期表中,与Li的化学性质最相似的邻族元素是 , 该元素基态原子核外M层电子的自旋状态(填“相同”或“相反”)。
(2)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在,双聚分子中存在四元环结构。画出双聚FeCl3分子的结构式。
(3)苯胺(
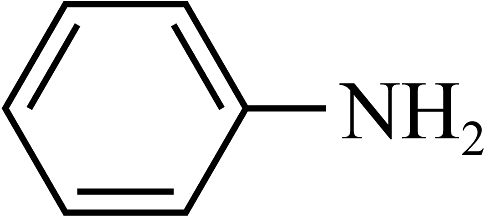 )的晶体类型是。苯胺与甲苯(
)的晶体类型是。苯胺与甲苯(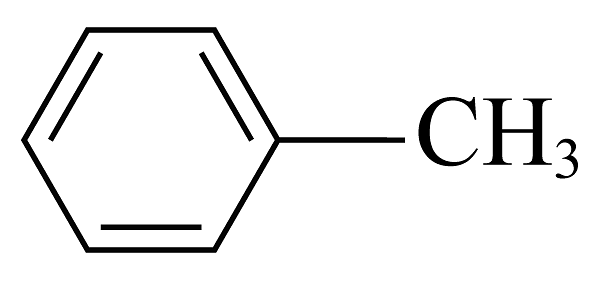 )的相对分子质量相近,但苯胺的沸点(184.4℃)高于甲苯的沸点(110.6℃),主要原因是。相同条件下,苯胺(
)的相对分子质量相近,但苯胺的沸点(184.4℃)高于甲苯的沸点(110.6℃),主要原因是。相同条件下,苯胺( )在水中的溶解能力(填“大于”、“小于”或“等于”)甲苯(
)在水中的溶解能力(填“大于”、“小于”或“等于”)甲苯( )的在水中的溶解能力。
)的在水中的溶解能力。II.有机物的结构与性质息息相关,官能团决定了有机物的主要化学性质。
(4)具有α-H的醛或酮,在酸或碱的催化作用下,与另一分子醛或酮发生缩合,生成β-羟基醛或β-羟基酮。以乙醛为例,其过程可表示如下:

请从元素电负性的角度解释第一步加成反应发生的原理。
(5)已知醛基(—CHO)能够和银氨溶液发生银镜反应,如乙醛(CH3CHO)发生的银镜反应:CH3CHO+2[Ag(NH3)2]OH2Ag↓+CH3COONH4+3NH3↑+H2O。请根据甲醛(HCHO)的结构,推测并写出甲醛和银氨溶液发生的化学反应方程式:。