相关试卷
-
1、反应物转化为产物时,能量变化与反应历程的关系如图所示,下列说法正确的是
 A、该反应是吸热反应 B、由图可知比稳定 C、是催化剂,可降低反应所需的活化能 D、使用催化剂后,反应历程中的决速步为
A、该反应是吸热反应 B、由图可知比稳定 C、是催化剂,可降低反应所需的活化能 D、使用催化剂后,反应历程中的决速步为 -
2、从炼锌厂的废渣(含、、、、等)中回收钴和锌的一种工艺流程如图:

下列说法错误的是
A、“加热酸浸”过程中生成的滤渣1主要成分为 B、“氧化”过程中发生反应: C、可通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥的操作得到晶体 D、在有机溶剂中的溶解度比小 -
3、直接燃料电池是一种新型化学电源,工作原理如图所示。电池放电时,下列说法正确的是
 A、电极Ⅰ的电势高于电极Ⅱ B、电极Ⅱ的反应为 C、工作一段时间后,电极Ⅰ附近的溶液减小 D、当外电路转移电子时,电极Ⅰ附近理论上收集到
A、电极Ⅰ的电势高于电极Ⅱ B、电极Ⅱ的反应为 C、工作一段时间后,电极Ⅰ附近的溶液减小 D、当外电路转移电子时,电极Ⅰ附近理论上收集到 -
4、经催化加氢可制得甲醇。下列说法正确的是A、分子和分子中均存在两个键 B、分子和分子均为直线型的非极性分子 C、分子中的原子和原子均为杂化 D、和分子间均存在氢键,因此比较稳定
-
5、向的恒容密闭容器中通入和各 , 发生反应:。在不同温度下测得随时间变化的曲线如图所示。下列说法正确的是
 A、该反应在任意温度下均可自发进行 B、温度下,的平衡转化率是30% C、、两点平衡常数: D、温度下,0到内,用表示的平均反应速率为0.1mol·L-1·min-1
A、该反应在任意温度下均可自发进行 B、温度下,的平衡转化率是30% C、、两点平衡常数: D、温度下,0到内,用表示的平均反应速率为0.1mol·L-1·min-1 -
6、短周期元素、、、的原子序数依次增大,的最高正化合价和最低负化合价的代数和为0,和的最外层电子数相同,的焰色试验呈黄色,四种元素最外层电子数之和为17。下列说法不正确的是A、易溶于的简单氢化物中 B、最高价氧化物对应水化物的酸性: C、与形成的化合物可能含有共价键 D、原子半径:
-
7、对于下列实验操作和现象,其结论正确的是
选项
操作
现象
结论
A
向盛有水的锥形瓶中小心滴加8~10滴
剧烈反应,液面上有白雾形成,并产生有刺激性气味的气体
水解生成氯化氢
和硫酸
B
将样品溶于稀硫酸后,滴加溶液
溶液变红
溶液中含但不确定样品在实验之前已变质
C
向盛有的溶液中先后滴加2滴的溶液和溶液
先生成白色沉淀,后变为黄色沉淀
D
将红热的木炭放置于盛有浓硝酸的试管中
试管内生成红棕色气体
木炭与浓硝酸反应生成
A、A B、B C、C D、D -
8、以和为原料制备清洁燃料二甲醚涉及的主要反应如下:
Ⅰ.
Ⅱ.
下列说法正确的是
A、反应Ⅰ的 B、增大反应体系压强,可提高二甲醚产率 C、越大,的平衡转化率越高 D、200℃平衡体系中比100℃平衡体系中大 -
9、能正确表示下列反应的离子方程式的是A、四氧化三铁溶于氢碘酸中: B、将过量的通入溶液中: C、向酸性高锰酸钾溶液中通入: D、将少量澄清石灰水滴加到碳酸氢钠溶液中:
-
10、脱落酸也称离层酸,是指能引起芽休眠、叶子脱落和抑制细胞生长等生理作用的植物激素,其结构简式如图所示,下列关于脱落酸的说法错误的是
 A、该化合物不溶于水 B、该化合物分子式为 C、能发生取代反应、加成反应、氧化反应 D、脱落酸最多可以与发生反应
A、该化合物不溶于水 B、该化合物分子式为 C、能发生取代反应、加成反应、氧化反应 D、脱落酸最多可以与发生反应 -
11、用于金属精制、农药、医药、催化剂再生等。室温下,关于溶液中,下列说法正确的是A、在水中的电离方程式为: B、溶液中存在: C、与的溶液等体积混合,混合液呈碱性 D、加水稀释会促进的电离,使溶液减小
-
12、设为阿伏加德罗常数的值,下列说法正确的是A、标准状况下氨气溶于水后所得溶液中 B、标准状况下的质量为 C、与稀硝酸反应,铁完全溶解转移电子数目一定是 D、含有电子的数目为
-
13、化学知识广泛应用于生产、生活中。下列叙述不正确的是A、用饱和氯化铵溶液可以清洗钢铁表面的锈迹 B、明矾和均可用作净水剂,且净水原理相同 C、在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 D、高分子材料聚乙烯广泛应用于食品包装材料
-
14、索拉非尼在临床上是一种新型的,多靶向性的治疗肿瘤的口服药,是多种激酶的抑制剂,它可抑制肿瘤细胞增殖和抗血管生成作用。它的合成路线如下:

已知:①R-NCO+R'-NH2→

②R-NO2R-NH2
③DMF、THF、BuOH、CH2Cl2都是反应中的溶剂
④碳氟键在酸碱性环境中不易水解
请回答:
(1)、化合物E的官能团名称是。(2)、化合物C的结构简式是。(3)、下列说法正确的是___________。A、F→索拉非尼的反应为取代反应 B、化合物D与苯甲醇互为同系物 C、索拉非尼的分子式是C21H16ClF3N4O3 D、A物质既能溶于酸也能溶于碱(4)、写出索拉非尼在氢氧化钠溶液中充分水解的化学方程式。(5)、设计以D为原料合成E的路线(用流程图表示,无机试剂任选)。(6)、写出3种同时符合下列条件的化合物C的同分异构体的结构简式①含有
 环
环②1H-NMR谱和IR谱检测表明:分子中共有3种不同化学环境的氢原子
③该物质和新制Cu(OH)2悬浊液加热条件下反应有砖红色沉淀生成。
-
15、氢化亚铜为红棕色固体,不稳定,60℃时分解为金属铜和氢气,难溶于水。某研究小组实验室条件下制备CuH,流程如下:

已知:①H3PO3在空气中易氧化成H3PO4 , Cu3(PO4)2溶于强酸。
②CuH + HCl = CuCl + H2↑
步骤Ⅳ实验装置图如下:
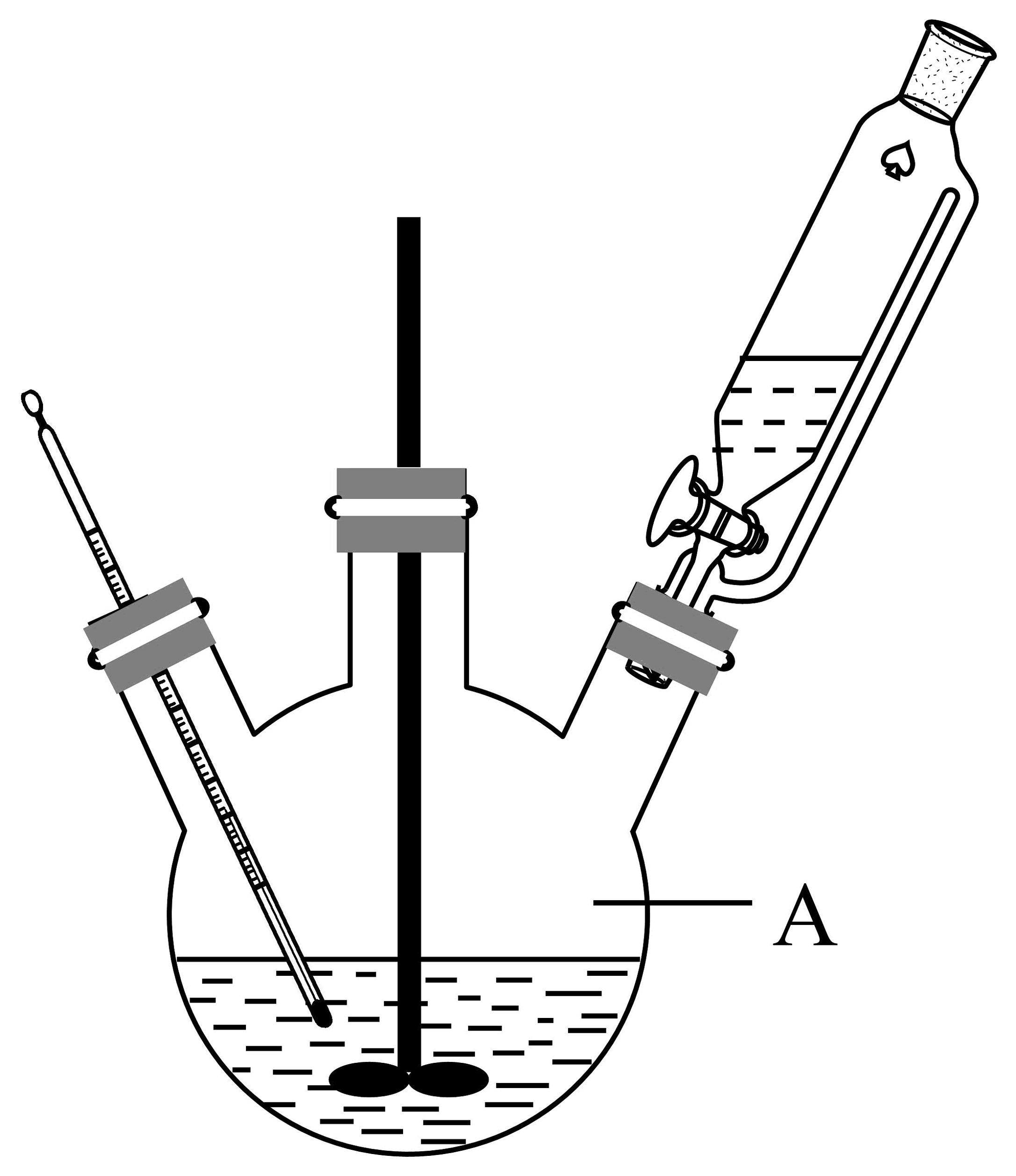 (1)、反应温度控制在40℃-50℃的原因(2)、写出仪器A的名称(3)、写出流程中步骤Ⅳ的离子方程式(4)、下列说法正确的是___________A、步骤Ⅰ中,加入80℃水是为了加快CuSO4· 5H2O的溶解速率 B、步骤Ⅳ中,反应可用水浴加热 C、步骤Ⅴ中多步操作为:过滤、洗涤、烘干 D、实验得到的棕色悬浊液底部可能会有紫红色固体(5)、产品纯度分析:称取氢化亚铜粗品10g,加入足量稀盐酸,充分反应(假设杂质与盐酸不反应),收集生成的氢气。
(1)、反应温度控制在40℃-50℃的原因(2)、写出仪器A的名称(3)、写出流程中步骤Ⅳ的离子方程式(4)、下列说法正确的是___________A、步骤Ⅰ中,加入80℃水是为了加快CuSO4· 5H2O的溶解速率 B、步骤Ⅳ中,反应可用水浴加热 C、步骤Ⅴ中多步操作为:过滤、洗涤、烘干 D、实验得到的棕色悬浊液底部可能会有紫红色固体(5)、产品纯度分析:称取氢化亚铜粗品10g,加入足量稀盐酸,充分反应(假设杂质与盐酸不反应),收集生成的氢气。①甲、乙、丙三位同学分别以下列装置测定生成氢气的体积(其他操作正确,最终液面如下图),测得气体体积偏大是(填甲、乙或丙)

②若按规范操作收集生成的氢气为VmL(已经换算成标准状况下的体积),则产品纯度为。
-
16、
丙烯是重要的化工原料,目前生产丙烯主要有丙烷脱氢、丙烷与二氧化碳耦合等技术。
方法一:丙烷在催化剂作用下直接脱氢法制丙烯
已知:主反应 Ⅰ:C3H8(g) C3H6(g)+H2(g)ΔH1>0
副反应 Ⅱ:C3H8(g)C2H4(g)+CH4(g)
(1)反应Ⅰ自发进行的条件________。(2)一定温度下,向1L恒容密闭容器中通入0.6mol C3H8 , 压强为0.75MPa,反应后测得各组分的平衡压强(即组分的物质的量分数×总压)为:p(C3H8)=0.5MPa、p(CH4)=0.075MPa,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数Kc的数值为________。(3)下列说法正确的是___________A. 通过充入惰性气体增大压强,不改变反应Ⅰ的反应速率 B. 恒温恒压条件下,ΔH1保持不变,说明反应Ⅰ达到平衡状态 C. 若只发生反应Ⅰ,恒压条件下,向原料气中掺入水蒸气,可增大反应的平衡常数,提高丙烯的产率 D. 已知高温条件下,C-C键比C-H键更易断裂,则制备丙烯应选择较低温度下的高效催化剂 方法二:丙烷与二氧化碳耦合法制丙烯
(4)以In/Zn作为催化剂,丙烷与二氧化碳可通过耦合法制丙烯,主要发生如下反应:Ⅰ:C3H8(g)C3H6(g)+H2(g)
Ⅱ:C3H8(g)C2H4(g)+CH4(g)
Ⅲ:CO2(g)+9H2(g) C3H6(g)+6H2O(g)
Ⅳ:CO2(g)+H2(g)CO(g)+H2O(g)
在580℃时,将C3H8和CO2按体积比1:1充入一恒压密闭容器中进行反应,实验测得体系中C3H8(g)、CO2(g)的转化率和C3H6(g)的选择性随催化剂组成变化如图甲,体系中C3H8(g)、CO2(g)的平衡转化率和C3H6(g)的平衡产率随压强变化如图乙。
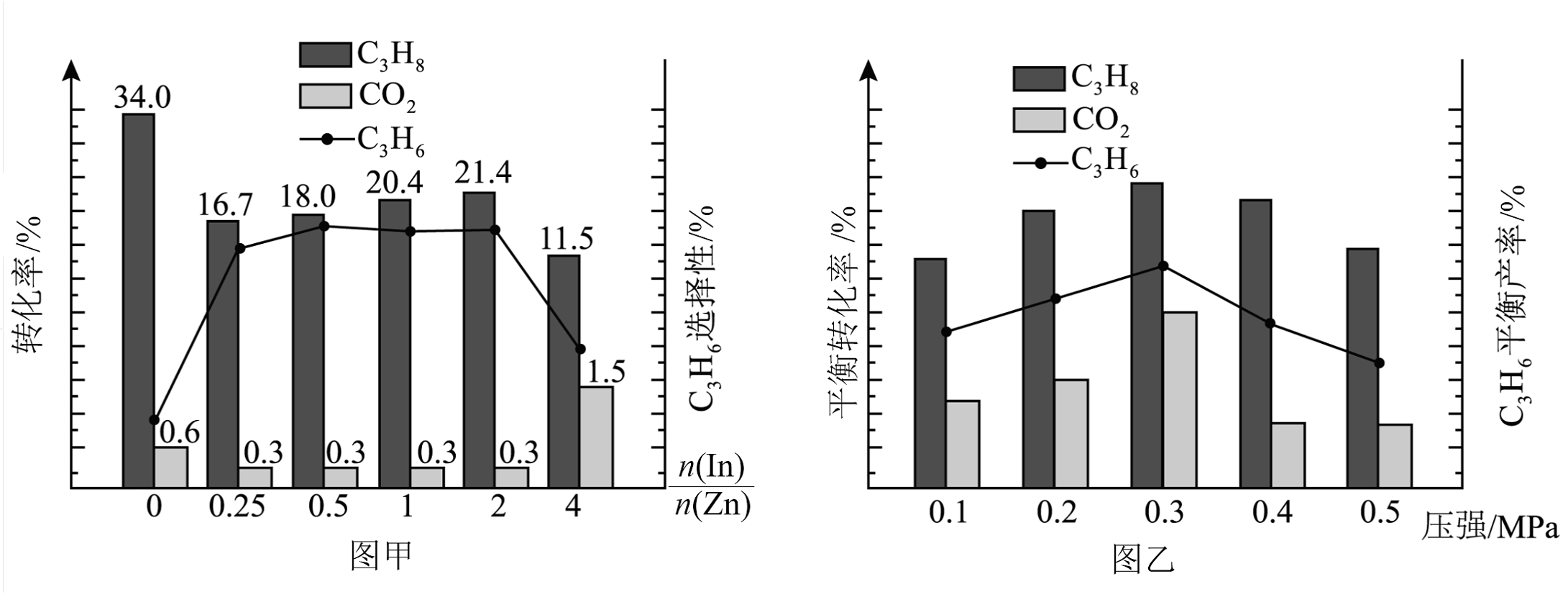
已知:C3H6(g)的选择性越高,副产物的含量越低。
耦合法制丙烯适宜选择的生产条件为________,随压强增大C3H6(g)的平衡产率先增大后减小的原因为________。
-
17、结晶水合物X由4种元素组成,某学习小组按如下流程进行实验:

已知:黑色固体B用100mL2.0 mol/L H2SO4溶液溶解后,多余的酸用0.30 mol NaOH恰好中和。
(1)、组成X的元素有H、O和(填元素符号),A的两种成分为(填写化学式)。(2)、写出X隔绝空气加热分解的化学方程式。(3)、写出金属粉末C生成深蓝色D溶液的离子方程式。(4)、黑色固体B加入稀硫酸溶解后,再加入足量氢氧化钠溶液,生成的蓝色沉淀可能是氢氧化物、碱式硫酸盐或两者的混合物(都难溶于水,易溶于强酸),请设计一个实验方案证明蓝色沉淀只有氢氧化物没有碱式硫酸盐:。 -
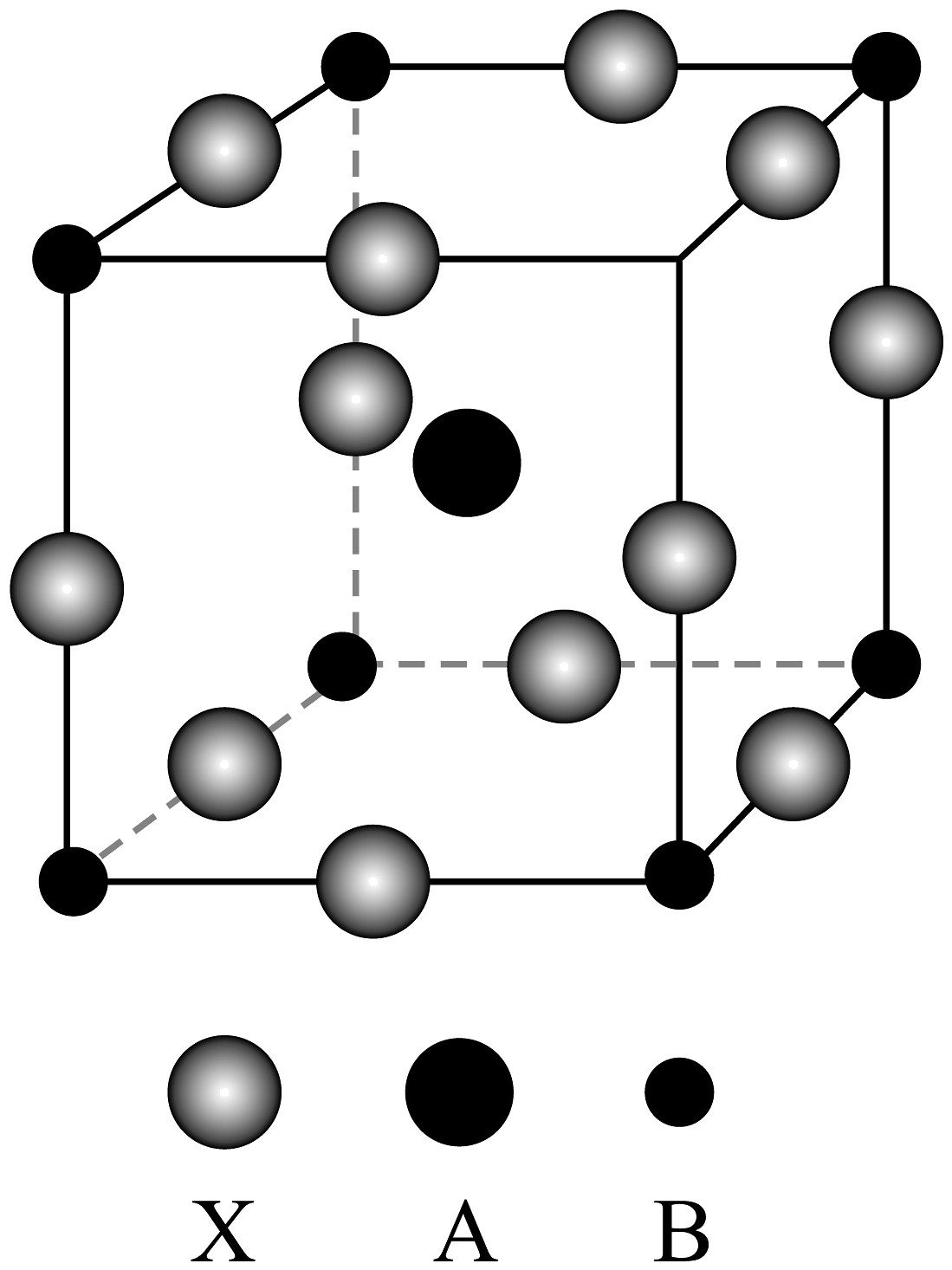
18、钙钛矿材料具有可设计性,其吸光能力远高于晶硅材料。钙钛矿常由H、N、O、Ca、Ti、卤素等元素形成。请回答下列问题:(1)、基态Ti原子的价电子排布图为。与Ti位于同一周期且含有相同未成对电子数的主族元素为。(2)、下列说法正确的是___________(填字母)A、CH3NH其中C原子与N原子的杂化类型不同 B、N、O元素的第二电离能大小顺序为O>N C、CaTiO3的组成元素的电负性大小顺序是O>Ti>Ca D、SiCl4的相对分子质量大于SiO2 , 所以SiCl4的沸点大于SiO2(3)、C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。从原子半径和共价键成键的角度分析,C、O原子间易形成C=O键,而Si、O原子间不易形成Si=O键的原因。(4)、钙钛矿并不是专指一种含钙和钛的某种化合物,而是一类具有相似结构的晶体材料的总称,其中A是较大的阳离子,B是较小的阳离子,X是阴离子。下图的晶胞表示立方钙钛矿,其通式可表示为(用A、B、X表示)。一种金属卤化物光电材料的组成为Pb2+、I﹣和有机碱离子CH3NH(结构与立方钙钛矿相同)。若晶胞参数为a nm,则晶体密度为g·cm-3(列出计算式)。
-
19、下列方案设计、现象和结论都正确的是
选项
实验方案
现象
结论
A
有机物A加入NaOH乙醇溶液中,充分加热;冷却后,取混合液加足量硝酸酸化的硝酸银溶液
未产生白色沉淀
有机物A不可能是氯代烃
B
常温下,用pH计测得0.1mol/L弱酸盐NaA、NaB、NaC溶液pH值分别为a、b、c
若c>b>a
水解程度A->B->C-
C
向放有少量脱脂棉的试管中加入几滴较浓的硫酸,充分搅拌后,加入新制Cu(OH)2悬浊液,加热
未观察到砖红色沉淀生成
说明纤维素没有发生水解
D
将封装有NO2和N2O4混合气体的圆底烧瓶浸泡在热水中
红棕色加深
NO2转化为N2O4是放热反应
A、A B、B C、C D、D -
20、已知25℃,Ksp (CaC2O4)=4.0×10-8 , H2C2O4的电离常数Ka1=5.6×10-2 , Ka2=1.5×10-4;Ksp(CaCO3)=3.4×10-9 , H2CO3的电离常数Ka1=4.5×10-7 , Ka2=4.7×10-11。下列有关说法正确的是A、25℃时,同浓度的NaHC2O4溶液的pH比NaHCO3大 B、用0.5mol/L的草酸钠溶液浸泡CaCO3 , 可实现CaCO3完全转化为CaC2O4 C、某温度下,向含CaC2O4固体的饱和CaC2O4溶液中加入少量草酸钠固体,则CaC2O4溶解性将减小 D、过量CaCO3溶于水达到溶解平衡,其上层清液中含碳微粒主要是CO