相关试卷
-
1、如图为有机物结构式,有关说法正确的是( )
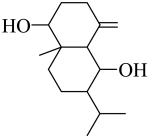 A、分子式为 B、手性碳有3个 C、
A、分子式为 B、手性碳有3个 C、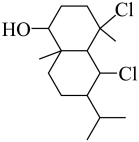 为加成产物
D、
为加成产物
D、 为缩聚产物
为缩聚产物
-
2、根据元素周期律,同时满足条件(ⅰ)和条件(ⅱ)的元素是( )
(ⅰ)电负性是同主族元素中最大:
(ⅱ)第一电离能比同周期相邻主族元素大的。
A、Al B、Si C、B D、Be -
3、下列实验操作及装置正确的是( )
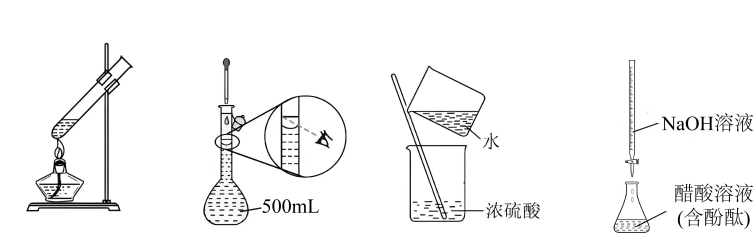 A、加热 B、定容 C、稀释 D、滴定
A、加热 B、定容 C、稀释 D、滴定 -
4、下列有关离子反应错误的是( )A、亚硫酸氢钠与石灰水反应: B、与水反应: C、与水反应: D、与NaBr溶液反应:
-
5、下列实验对应物质性质、现象都正确是( )
选项
性质
现象
A
焰色反应
Na、K火焰都是紫色
B
漂白性
、都可以使物质永久漂白
C
蛋白质变性
醋酸铅和甲醛都能让蛋白质变性
D
腐蚀印刷电路
用氯化铁和浓硫酸在常温下都可以刻画电路板
A、A B、B C、C D、D -
6、抗日战争时期,我国军民同仇敌忾,利用简易装置制作了许多武器,下列制造过程中涉及氧化还原反应的是( )A、用研磨法代替粉碎机碾碎硝化棉 B、在陶缸中使用硫磺制作硫酸 C、用蒸馏法将白酒制取工业酒精 D、用水解法将植物油与熟石灰制备甘油
-
7、化合物G是一种药物合成中间体,其合成路线如图。

已知:
 。
。回答以下问题:
(1)、D中的官能团有碳氯键、。(2)、B的结构简式为;反应④的反应类型为反应。(3)、E→F的化学方程式为。(4)、满足下列条件的D的同分异构体有种(不考虑立体异构)。①苯环上含有三个不同取代基;②能与溶液反应放出气体;③含氨基但与苯环不直接相连。
(5)、由苯甲醇制备 的合成路线如图,其中M、N的结构简式依次为、。
的合成路线如图,其中M、N的结构简式依次为、。
-
8、CO具有毒性,浓度较高时会使人出现不同程度中毒症状,危害人体的脑、心、肝、肾、肺及其他组织,但CO也是一种重要的化工原料,可用于甲醇和光气的生产以及有机合成等。(1)、已知:断开1mol化学键所需能量如表所示。
化学键
所需能量/(kJ·mol-1)
1076
436
413
463
则反应 kJ·mol-1;该反应在(填“高温”“低温”或“任意温度”)下能自发进行。
(2)、在体积为VL的恒容密闭容器中,充入1mol和5mol , 一定温度下仅发生反应 , 10min时反应达到平衡。测得和的物质的量随时间的变化曲线如图所示。
①3min时,(填“>”“<”或“=”)。
②0~10min内,的平均反应速率(用含V的式子表示)mol·L-1·mun-1;10min时,的体积分数为%(保留2位小数)。
③起始时容器内总压强为 , 该温度下该反应的平衡常数(用含的式子表示,无须化简,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)、在催化剂M的作用下,与水蒸气反应可以制取。
从图1中可得出的信息是(任写一条);根据图2,试分析当反应器中存在Pd膜时CO具有更高转化率的原因:(答一条即可)。
-
9、以某种锰尘(主要成分为 , 杂质为、MgO、CaO和FeO)为原料制备高纯的工艺流程如图。

已知:①25℃时,、。
②溶液中金属离子开始沉淀和沉淀完全时溶液的pH如表。
金属离子
开始沉淀时溶液的pH
8.1
6.3
1.5
3.4
沉淀完全时溶液的pH
10.1
8.3
2.8
4.7
回答下列问题:
(1)、Mn元素位于元素周期表的(填“s”“p”“d”或“ds”)区。(2)、“酸浸”过程中反应生成的气体①为(填化学式,下同);滤渣①的主要成分是。(3)、保持其他条件不变,在不同温度下“酸浸”时锰元素的浸出率随时间的变化如图。则“酸浸”的最佳温度是℃,最佳时间是mɪn。 (4)、“除杂②”后所得滤液中,。(5)、“沉淀”过程发生反应的化学方程式为。“沉淀”步骤反应完全后,分离出的操作为 , 该操作需要使用的玻璃仪器有烧杯、漏斗和。(6)、取5.00g碳酸锰样品,加入适量硫酸,加热,待固体完全溶解后,用1.000mol·L-1的溶液滴定,至滴定终点时,消耗溶液的体积为23.50mL。已知:最终反应产物为 , 设杂质均不参与反应。则样品中的质量分数为%(保留2位小数)。
(4)、“除杂②”后所得滤液中,。(5)、“沉淀”过程发生反应的化学方程式为。“沉淀”步骤反应完全后,分离出的操作为 , 该操作需要使用的玻璃仪器有烧杯、漏斗和。(6)、取5.00g碳酸锰样品,加入适量硫酸,加热,待固体完全溶解后,用1.000mol·L-1的溶液滴定,至滴定终点时,消耗溶液的体积为23.50mL。已知:最终反应产物为 , 设杂质均不参与反应。则样品中的质量分数为%(保留2位小数)。 -
10、某实验小组设计实验制备(摩尔质量为376g·mol-1),是具有光泽的红色晶体,受热易分解,是一种氧气吸收剂。实验步骤如下:
步骤1:将100mL纯水煮沸10min后,隔绝空气冷却。
步骤2:在仪器2(吸滤瓶)中放1.5g(摩尔质量为294g·mol-1)粉末、7.6g锌丝,仪器1(锥形瓶)中放冷的溶液(13.5g固体,加12mL无氧纯水),仪器3中加入自来水。

步骤3:在仪器5中放35mL8mol·L-1盐酸,打开弹簧夹4,夹紧通向锥形瓶的弹簧夹,向吸滤瓶内缓慢滴加盐酸,当2吸滤瓶内溶液变成纯蓝色时,表示反应结束(始终没有生成)。经一系列操作,将吸滤瓶中的溶液转移至锥形瓶中,当转移完全后,迅速塞紧锥形瓶,用冰水冷却,有红色晶体析出。
步骤4:洗涤。摇动锥形瓶,将溶液与晶体一起过滤,依次用冷的无氧水、无水乙醇、无水乙醚洗涤晶体。操作时,下一次洗涤剂须在前一次溶液或洗涤液流尽前加入。
步骤5:干燥。抽干,在纸上晾干,将晶体转移到有塞的干燥瓶中,最终得到1.8g。
回答下列问题:
(1)、仪器5的名称是 , 仪器3中自来水的作用是(任答一条)。(2)、步骤1将纯水煮沸的目的是。(3)、写出吸滤瓶中生成的离子方程式:。(4)、步骤3中,“一系列操作”是(填“关闭”或“打开”,下同)弹簧夹4,吸滤瓶通向锥形瓶的弹簧夹。转移完全后,“用冰水冷却”的目的是。(5)、的产率为(计算结果保留4位有效数字)。(6)、可用于除去氮气中的微量氧气,吸收后的产物为、、和 , 则该反应中n(还原剂)(氧化剂)=。 -
11、T℃下,三种碳酸盐(M表示、或)的沉淀溶解平衡曲线如图所示。已知: , , a点对应的横纵坐标数值相等。下列说法正确的是
 A、 B、在任何条件下,三种物质之间都不可能相互转化 C、a点对应的溶液为不饱和溶液,且 D、当向1L0.001mol·L-1溶液中滴加1mL0.001mol·L-1的溶液时有沉淀析出
A、 B、在任何条件下,三种物质之间都不可能相互转化 C、a点对应的溶液为不饱和溶液,且 D、当向1L0.001mol·L-1溶液中滴加1mL0.001mol·L-1的溶液时有沉淀析出 -
12、我国研究人员研究了在催化剂X的作用下加氢形成乙醇的反应机理,反应过程中物质相对能量与反应进程关系如图(加“*”物质为吸附态)。下列说法正确的是
 A、的脱附过程为放热过程 B、的过程中存在非极性键的断裂和形成 C、为决速步骤 D、若用代替反应,则产物为
A、的脱附过程为放热过程 B、的过程中存在非极性键的断裂和形成 C、为决速步骤 D、若用代替反应,则产物为 -
13、杜仲甙又名桃叶珊瑚甙,是具有清湿热、利小便、镇痛、降压、保肝护肝、抗肿瘤等作用的生物活性物质,能促进干细胞再生,明显抑制乙型肝炎病毒DNA的复制,结构简式如图。下列说法正确的是
 A、分子式为 B、该物质为苯的同系物 C、该物质能使酸性高锰酸钾溶液褪色 D、1mol该物质最多能消耗6molNaOH
A、分子式为 B、该物质为苯的同系物 C、该物质能使酸性高锰酸钾溶液褪色 D、1mol该物质最多能消耗6molNaOH -
14、下列实验装置(部分夹持装置略)或操作正确且能达到实验目的的是
选项
A
B
C
D
实验装置或操作




实验目的
制取氯气
牺牲阳极法保护铁电极
向容量瓶中转移溶液
观察丁达尔效应
A、A B、B C、C D、D -
15、设为阿伏加德罗常数的值,部分含氮物质的转化如图所示。下列叙述正确的是
 A、8.0g含有的数目大于 B、标准状况下,4.48L含有的σ键数目为 C、反应(i)中1mol能提供的孤电子对数目为 D、反应(ii)中1mol完全反应转移的电子数为
A、8.0g含有的数目大于 B、标准状况下,4.48L含有的σ键数目为 C、反应(i)中1mol能提供的孤电子对数目为 D、反应(ii)中1mol完全反应转移的电子数为 -
16、NiO是一种极有前景的功能材料,已被广泛应用于冶金、化工及电子工业等领域。其晶胞结构(与NaCl相同)如图所示。按面对角线对晶胞进行垂直切割,得到的截面图是
 A、
A、 B、
B、 C、
C、 D、
D、
-
17、下列各组离子在水溶液中能大量共存的是A、、、、 B、、、、 C、、、、 D、、、、
-
18、下列关于碳、氮、硫及其化合物的叙述正确的是A、键角: B、酸性: C、和中硫原子均采取杂化 D、熔、沸点:

-
19、下列化学用语表述正确的是A、的VSEPR模型:
 B、的电子式:
B、的电子式: C、HCl分子中共价键类型:p-pσ键
D、2-乙基-1-丁醇的结构简式:
C、HCl分子中共价键类型:p-pσ键
D、2-乙基-1-丁醇的结构简式:
-
20、氮化镓是新型半导体材料。工业制备氮化镓的常用方法是GaCl3+NH3=GaN+3HCl。下列叙述正确的是A、基态Ga原子电子排布式:[Ar]4s24p1 B、NH3的VSEPR模型:
 C、HCl中的共价键是s-pσ键
D、HCl溶于水形成的水合氯离子:
C、HCl中的共价键是s-pσ键
D、HCl溶于水形成的水合氯离子: