相关试卷
-
1、以粮食为原料制取乙醇并利用其制备乙酸乙酯(C)和高分子材料(G)的流程如下:

已知:
ⅰ.D的产量可以用来衡量一个国家石油化工水平。
ⅱ.饱和水溶液pH为5.6。
(1)、某兴趣小组尝试利用该原理酿制米酒。①《齐民要术》中记载“浸曲三日,如鱼眼汤沸,酘米。其米绝令精细”。此中“曲”为酒曲,含有酶,在反应中起作用。“精细”即将米研磨为粉状,目的是。
②为了更好地了解米的发酵过程,小组同学每隔24小时测定米酒的酒精度和pH,连续10天,收集相关数据绘制了实验数据图。

针对米酒的pH变化趋势,甲同学分析原因是酿酒过程中产生了。乙同学认为不合理,其依据一是;依据二是乙醇中含官能团(填名称),在一定条件下会被氧化成B且酸性比碳酸强。
(2)、“酒越陈越香”是因为生成酯类物质。①反应Ⅰ的化学方程式是 , 其中n(氧化剂):n(还原剂)=。
②反应Ⅲ的发生装置如图所示,有关说法正确的是。

a.试剂X为饱和溶液。
b.实验时,先加浓硫酸,再加无水乙醇和冰醋酸。
c.一段时间后,观察到X溶液的液面上有一层无色有特殊香味的油状液体。
d.实验结束时,采用蒸发的方法将乙酸乙酯从混合物中分离出来。
(3)、①D也可由戊烷裂化裂解制得。写出一氯代物只有一种的戊烷同分异构体的结构简式。②F→G为加聚反应,化学方程式是。
(4)、在反应Ⅰ→Ⅵ中,属于加成反应的是。(5)、研究资料表明,酿酒的过程中会产生乳酸( ),请依据反应Ⅲ推测其生成的六元环酯()的结构简式。
),请依据反应Ⅲ推测其生成的六元环酯()的结构简式。 -
2、X、Y、Z、M、Q、R皆为周期表中前20号元素,其原子半径与主要化合价的关系如图所示。
 (1)、已知X位于第一周期,则X2Y电子式为。(2)、比较Y和Z的简单氢化物,更稳定的是(填化学式)。(3)、已知Q位于第三周期,则R在元素周期表中的位置是。(4)、下列推断正确的是(填序号)。
(1)、已知X位于第一周期,则X2Y电子式为。(2)、比较Y和Z的简单氢化物,更稳定的是(填化学式)。(3)、已知Q位于第三周期,则R在元素周期表中的位置是。(4)、下列推断正确的是(填序号)。a.简单离子半径:
b.由X、Y、Z三种元素组成的化合物可能是盐或碱
c.Z与M的最高价氧化物对应水化物均为强酸
(5)、比较I-和M的阴离子,还原性更强的是(填离子符号),从原子结构的角度解释原因。 -
3、一种简单的原电池装置如图所示。据图回答下列问题。
 (1)、锌是该电池的(填“正”或“负”)极,发生的电极反应为。(2)、装置中稀硫酸的作用是。
(1)、锌是该电池的(填“正”或“负”)极,发生的电极反应为。(2)、装置中稀硫酸的作用是。a.电极材料 b.电极反应物 c.电子导体 d.离子导体
(3)、该原电池外电路中电流方向为(填“Zn→Cu”或者“Cu→Zn”)。从化学的角度分析,原电池产生电流的原因是:。(4)、若将稀硫酸换成硫酸铜,电池总反应方程式为。(5)、下列反应通过原电池装置,可实现化学能直接转化为电能的是。a. b. c.
-
4、某实验小组用0.1 mol/L Na2S2O3溶液和0.1 mol/L H2SO4溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
已知:Na2S2O3 + H2SO4 = Na2SO4 + SO2 + S ↓+ H2O
实验序号
温度/℃
Na2S2O3溶液体积/mL
H2SO4溶液体积/mL
H2O体积/mL
出现沉淀所需的时间/s
Ⅰ
20
5
5
10
t1
Ⅱ
20
5
10
a
t2
Ⅲ
60
5
5
10
t3
实验结果:t1>t2>t3。下列说法不正确的是
A、研究H2SO4浓度对该反应速率的影响,a = 5 B、对比实验Ⅰ、Ⅱ可知,c (H2SO4) 越大,反应速率越快 C、对比实验Ⅱ、Ⅲ可知,升高温度能加快该反应速率 D、进行实验Ⅰ、Ⅱ时,依次向试管中加入Na2S2O3溶液、H2SO4溶液、H2O -
5、下列实验方案(夹持装置已略)能达实验目的的是


A.分离酒精和水
B.比较Mg、Al金属性的强弱


C.探究浓度对化学反应速率的影响
D.除去SO2中的少量CO2
A、A B、B C、C D、D -
6、10mL0.40mol/LH2O2溶液在催化剂作用下发生分解。不同时刻测定生成O2的体积(已折算为标准状况)如下表。
t/min
0
2
4
6
8
10
V(O2)/mL
0.0
4.6
11.2
22.4
26.5
29.9
忽略溶液的体积变化,下列叙述不正确的是
A、0~4min的平均反应速率: B、0~6min随反应进行速率变快可能是由于反应放热使温度升高 C、反应至4min时,c(H2O2)=0.3mol/L D、反应至4min时,H2O2分解了50% -
7、一定温度下,反应H2(g)+I2(g)⇌2HI(g)在密闭容器中进行,下列措施不改变化学反应速率的是A、压缩容器,增大压强 B、恒容,充入H2 C、恒压,充入氩气 D、恒容,充入He
-
8、1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列事实
①苯不能使溴的CCl4溶液褪色 ②苯能与H2发生加成反应 ③溴苯没有同分异构体 ④邻二溴苯只有一种⑤苯不能使酸性高锰酸钾溶液褪色
A、①②⑤ B、②④⑤ C、①④⑤ D、①③⑤ -
9、氢化铵(NH4H)与氯化铵结构相似,又已知NH4H与水反应有氢气产生,下列叙述中不正确A、NH4H是离子化合物 B、NH4H固体投入少量水中,稍稍加热后有两种气体产生 C、NH4H中的H-离子半径比锂离子半径大 D、NH4H溶入水后,形成的溶液显酸性
-
10、可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中少量乙烯的操作方法是A、将混合气体通过盛有硫酸的洗气瓶 B、将混合气体通过盛有足量溴水的洗气瓶 C、将混合气体通过盛有酸性高锰酸钾溶液的洗气瓶 D、将混合气体通过盛有澄清石灰水的洗气瓶
-
11、糖类、油脂、蛋白质是重要的营养物质。下列说法正确的是A、油脂属于高分子化合物 B、硫酸铜溶液可使蛋白质变性 C、纤维素和淀粉互为同分异构体 D、糖、油脂、蛋白质均可水解
-
12、我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下:
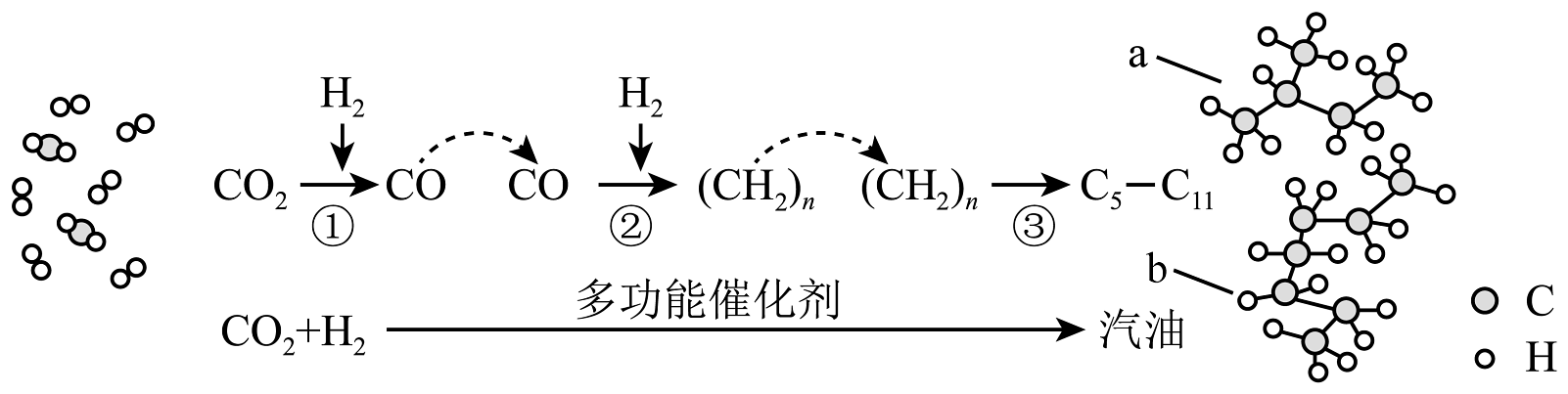
下列说法不正确的是
A、反应①的产物中含有水 B、反应②中有碳碳键和碳氢键的形成 C、汽油主要是C5~C11的烃类混合物 D、通过石油的裂化也可以获得汽油,石油的裂化属于物理变化 -
13、下列反应既属于氧化还原反应 , 又属于吸热反应的是A、镁条与稀盐酸的反应 B、碳酸氢钠粉末与柠檬酸的反应 C、甲烷在氧气中的燃烧反应 D、灼热的二氧化碳与碳粉的反应
-
14、硫酸羟胺在工业和分析领域有广泛应用。已知硫酸羟胺具有还原性,易溶于水,羟胺为白色晶体,沸点为 , 易溶于水、甲醇,受热易分解。实验室制备硫酸羟胺的流程及装置如图(加热及夹持装置略)。

回答下列问题:
(1)、仪器A的名称为 , 实验装置连接顺序为a→(填标号),步骤Ⅰ中发生反应的化学方程式为。(2)、从结构上分析,等浓度的和的混合溶液中离子浓度大小比较为(填“>”“=”或“<”)。(3)、分离和时可按下列步骤进行操作:a.向混合溶液中加入氨水,生成
b.再加入甲醇,析出晶体B
c.过滤,将滤液进行减压蒸馏
d.加入硫酸得到产品
步骤b中析出晶体B的化学式为 , 步骤c中选择进行减压蒸馏的目的是。
(4)、晶体中存在的化学键类型有(填标号)。a.离子键 b.共价键 c.配位键 d.氢键 e.范德华力
(5)、利用硫酸羟胺可制备环己酮肟,制备过程如下图所示。已知环己酮( , 可溶于水,易溶于有机溶剂)和羟胺反应生成环己酮肟(
, 可溶于水,易溶于有机溶剂)和羟胺反应生成环己酮肟( )的反应称为肟化反应。环己酮肟能溶于水,难溶于浓溶液,时在酸性条件下水解生成羟胺盐和环己酮。
)的反应称为肟化反应。环己酮肟能溶于水,难溶于浓溶液,时在酸性条件下水解生成羟胺盐和环己酮。
该流程中,通过过滤可将Y与环己酮肟分离,则肟化反应中通入气体X的化学式为。
-
15、有机化合物的提取与合成极大地促进了化学科学的发展;药物化学是重要的有机化学分支之一,合成某药物中间体G的流程如图所示:

已知:乙酸酐为2分子乙酸脱水得到,结构简式为
 。(1)、化合物分子A的名称为。(2)、化合物C中除羟基外的含氧官能团的名称为:;化合物C的某同分异构体含有苯环,在核磁共振氢谱图上只有4组峰,且能够发生银镜反应,其结构简式为。(任意写一种)(3)、对化合物D,分析预测其可能的化学性质,完成下表。
。(1)、化合物分子A的名称为。(2)、化合物C中除羟基外的含氧官能团的名称为:;化合物C的某同分异构体含有苯环,在核磁共振氢谱图上只有4组峰,且能够发生银镜反应,其结构简式为。(任意写一种)(3)、对化合物D,分析预测其可能的化学性质,完成下表。序号
反应试剂、条件
反应形成的新结构
反应类型
①
H2 , 钯催化
②
-COOCH3
(4)、以下关于物质E说法正确的是_______。A、分子中不存在手性碳原子 B、可以发生缩聚反应形成聚酯 C、可以和FeCl3发生显色反应 D、1 molE与足量NaHCO3反应产生1 molCO2(5)、以对甲基苯酚为有机原料,合成 。基于你设计的合成路线,回答下列问题:
。基于你设计的合成路线,回答下列问题:①第一步反应的化学方程式为。
②第一步含苯环产物与足量的NaOH在加热条件下反应的化学方程式为。
③目标产物被酸性KMnO4氧化后的产物的结构简式为。
-
16、煤气中主要的含硫杂质有H2S以及CS2、COS等有机硫煤气中的湿法脱硫的原理是利用Na2CO3溶液吸收H2S生成NaHS,再进一步被空气氧化成Na2S2O3.请回答下列问题:(1)、脱除煤气中COS的方法有Br2的KOH溶液氧化法、H2还原法以及水解法等。
①COS的分子结构与CO2相似,COS的电子式为。
②Br2的KOH溶液将COS氧化为硫酸盐和碳酸盐的离子方程式为。
③已知断裂1 mol化学键所需的能量如下:
化学键
H-H
C=O
C=S
H-S
CO
E/kJ·mol-1
436
745
577
339
1072
H2还原COS发生的反应为H2(g)+COS(g)=H2S(g)+CO(g),该反应的ΔH=kJ·mol-1。
④用活性α-Al2O3催化COS水解的反应为 , 相同投料比、相同流量且在催化剂表面停留相同时间时,在相同的时间内测得不同温度下COS的转化率(未达平衡)如图1所示;某温度下,COS的平衡转化率与的关系如图2所示。

由图1可知,催化剂活性最大时的温度约为;由图2可知,P点时平衡常数K=(保留2位有效数字)。
(2)、回收处理燃煤烟气中SO2的方法之一是用氨水先将SO2转化为NH4HSO3 , 再通入空气将其氧化成(NH4)2SO4.能提高燃煤烟气中SO2去除率的措施有(填字母)。a.增大氨水浓度 b.增大燃煤烟气的流速 c.升高温度 d.增大压强
(3)、某的甲酸可与其他有机酸混合作清洗剂,研究混合酸中的微粒数量关系有意义。25℃时,相同浓度甲酸、丙酸(C2H5COOH)及某羧酸R1COOH的水溶液中,酸分子的分布分数随pH变化曲线如下图所示。
①往HCOOH和C2H5COOH的混合溶液中加入NaOH至pH=7,(填“>”“=”或“<”)。
②将等物质的量浓度等体积的HCOOH和R1COONa混合充分,发生的反应为: , 求平衡时HCOOH的转化率。
-
17、铟被广泛应用于电子、太阳能等领域。以某炼锌废渣(主要含ZnO、In2O3 , 还含少量SnO2、PbO、SiO2等物质)为原料,制备粗铟的工艺流程如下:

已知:①In(铟)与Al是同主族元素,Sn(锡)是第ⅣA族元素;
②H2A2为萃取剂,萃取In3+原理为:In3+(水相)+3H2A2(有机相)InA3·3HA(有机相)+3H+(水相)
(1)、In元素位于第五周期,基态In原子的价电子排布式为。(2)、“酸浸”中滤渣的主要成分是。(3)、“反萃取”中,溶液M是_____。A、硫酸 B、盐酸 C、硝酸 D、氢氧化钠溶液(4)、“沉铟”中,转化为。①的立体构型为;
②写出该步转化的离子方程式。
(5)、“酸溶”后,铟主要以NaInCl4形式存在溶液中;加入锌粉制得粗铟,同时还生成一种还原性的气体,该气体和生成In的物质的量之比为1:2,写出“还原”步骤中发生反应的化学方程式。(6)、一种铜铟硒晶体(化学式为CuInSe2)的晶胞结构如图,晶胞中In和Se未标明,用A或B代替。
①推断In是(填“A”或“B”)。
②晶体中一个Cu周围与它最近且等距离的B粒子的个数为。
-
18、我国科研人员提出了由和转化为高附加值产品的催化反应历程。该历程示意图如下图,下列说法不正确的是
 A、为正四面体构型 B、①→②的过程要释放能量 C、反应过程中只存在极性键的断裂和形成 D、生成的总反应原子利用率为100%
A、为正四面体构型 B、①→②的过程要释放能量 C、反应过程中只存在极性键的断裂和形成 D、生成的总反应原子利用率为100% -
19、某温度下,在密闭容器中充入一定量的 , 发生下列反应:、 , 测得各气体浓度与反应时间的关系如图所示。下列反应进程示意图符合题意的是
 A、
A、 B、
B、 C、
C、 D、
D、
-
20、下列陈述I与陈述Ⅱ均正确,且具有因果关系的是
选项
陈述I
陈述Ⅱ
A
氨气易液化
氨分子间形成氢键
B
存在稳定的H2、HCl,不存在H3、H2Cl
共价键具有方向性
C
工业用电解熔融AlCl3制取Al
金属铝的还原性很强,需电解法制备
D
溶解度:O2<O3
相对分子质量越大,分子间作用力越大
A、A B、B C、C D、D