相关试卷
-
1、锂-氟化碳()电池具有优异的性能。该电池的总反应为 , 电池工作时,下列说法正确的是A、锂电极为正极 B、电子由Li电极经导线流向电极 C、负极反应为 D、将电能转化为化学能
-
2、白木香醛(如图)是沉香精油的主要成分之一。下列关于该化合物的说法不正确的是
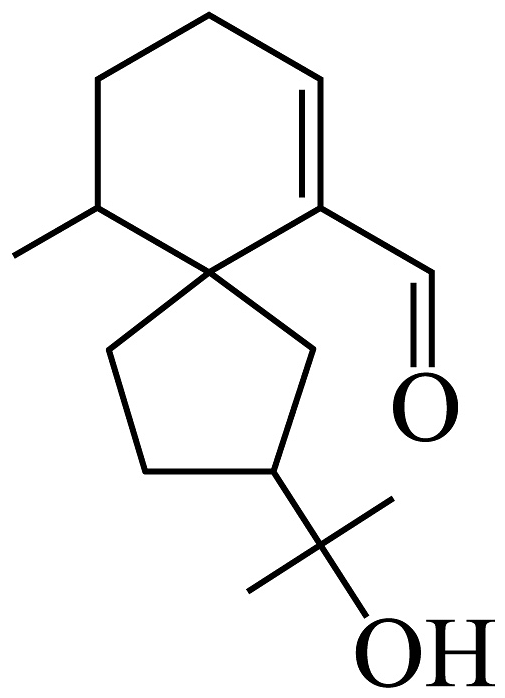 A、能发生银镜反应 B、能使溴的四氯化碳溶液褪色 C、其结构中两个碳环一定共平面 D、1mol该化合物与足量Na反应可产生0.5mol
A、能发生银镜反应 B、能使溴的四氯化碳溶液褪色 C、其结构中两个碳环一定共平面 D、1mol该化合物与足量Na反应可产生0.5mol -
3、为达到相应实验目的,下图所示实验装置不合理的是
 A、图甲:分离正己烷(沸点69℃)和正庚烷(沸点98℃) B、图乙:提纯粗苯甲酸时,趁热过滤去除不溶物 C、图丙:完成乙酸乙酯制备后,分离有机相和水相 D、图丁:用盐酸标准液滴定未知浓度的NaOH溶液
A、图甲:分离正己烷(沸点69℃)和正庚烷(沸点98℃) B、图乙:提纯粗苯甲酸时,趁热过滤去除不溶物 C、图丙:完成乙酸乙酯制备后,分离有机相和水相 D、图丁:用盐酸标准液滴定未知浓度的NaOH溶液 -
4、下列化学方程式或离子方程式书写正确的是A、溶液与NaOH溶液反应: B、高温下Fe与反应: C、与冷的石灰乳反应: D、铜丝与热的浓硫酸反应:
-
5、劳动创造价值。下列劳动项目与所述化学知识没有关联的是
选项
劳动项目
化学知识
A
化学实验员:用化学沉淀法去除粗盐溶液中的
B
水厂净水工:使用去除水中的细小悬浮物
是电解质
C
材料分析员:通过X射线衍射实验区分石英玻璃和水晶
石英玻璃是非晶体,水晶是晶体
D
肥皂生产工:利用油脂和烧碱制肥皂
油脂在碱性条件下水解
A、A B、B C、C D、D -
6、实验室中利用如图所示装置进行的相关实验,其中,能够达到预期目的的是


A.制备
B.除杂


C.验证与的反应
D.验证能否与水反应
A、A B、B C、C D、D -
7、服装材料的演变反映了人类文明的进步。下列说法不正确的是A、兽皮制表:用骨针缝制时主要发生物理变化 B、蚕丝纺衣:蚕丝中的蛋白质受热后易发生变性 C、棉花织衣:棉花中的纤维素属于多糖 D、纤维成衣:合成聚氯乙烯纤维的反应属于缩聚反应
-
8、“北斗巡天”“脑机融通”等彰显了我国科技发展的巨大成就。下列说法正确的是A、北斗技术助力生产:卫星外壳中合金的硬度比其成分金属的大 B、人工智能服务生活:人工智能芯片的主要成分为 C、脑机接口融入医疗:植入式电极中的石墨烯属于烯烃 D、多箭齐发探索宇宙:火箭发动机使用的煤油属于可再生能源
-
9、古代的计量器具是劳动人民智慧的结晶。下列计量器具中,主要材质为金属的是


A.称量质量的铜秤砣
B.测量容积的陶量


C.测量长度的木尺
D.计算数目的竹算筹
A、A B、B C、C D、D -
10、
氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。
方法Ⅰ.氨热分解法制氢气
相关化学键的键能数据
化学键
N≡N
H-H
N-H
键能E(kJ·mol-1)
946
436
391
在一定温度下,利用催化剂将NH3分解为N2和H2。回答下列问题:
(1)反应2NH3(g)⇌N2(g)+ 3H2(g) ∆H=kJ·mol-1。
(2)已知该反应的∆S=0.1989kJ·mol-1 ·K-1 , 则该反应在(填“较高温度”、“较低温度”、“任意温度”)下反应能自发进行;
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1molNH3通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。

①若保持容器体积不变,t1 时反应达到平衡,用N2的分压变化表示0~t1 时间内的反应速率v(N2)=kPa·min-1(用含t1的代数式表示)。
②t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2 分压变化趋势的曲线是(用图中a、b、c、d表示),重新达到平衡后该反应的平衡常数为。
方法Ⅱ.氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。

(4)电解过程中OH- 的移动方向为(填“从左往右”或“从右往左”)。
(5)阴极的电极反应式为。
-
11、As2O3在诱导癌细胞凋亡、治疗急性早幼粒细胞性白血病等方面表现出显著疗效。对某睢黄矿处理后得到一种含砷矿流(主要成分为As2S3和 FeS), 由该矿渣生产As2O3 的工艺流程如下:

已知:①As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
②砷存在两种常见的含氧酸根离子,AsO和AsO , 前者易被氧化
回答下列问题:
(1)、As 位于第四周期,且与N同主族,基态As 的原子结构示意图为(2)、下列有关硫黄的性质和用途的说法错误的是(填字母)。a.不溶于水,易溶于乙醇 b.可用于制造农药、火柴、火药
c.易溶于二硫化碳 d.硫黄在足量氧气中燃烧生成三氧化硫
(3)、“浸取”产生的AsO和AsS中As的杂化方式一致,均为杂化,浸渣的成分为。(4)、“脱硫”时,Na3AsO3和Na3AsS3均会被NaClO氧化,其中AsS与ClO-反应的离子方程式为。(5)、“酸化”后,砷以H3AsO4的形式存在,则“还原”时H3AsO4参与反应的化学方程式为。(6)、③某含氮催化剂的六方晶胞如图,晶胞参数为a=b≠c,α=β=90°,γ=120°。其化学式为;若A点原子的分数坐标为(1,0,0),则B点Li原子的分数坐标为;1个N原子周围距离相等且最近的Li原子数目为。
-
12、镓(Ga)是一种战略性元素,科学家制备了一种日盲紫外响应增强的全光谱异质结自供能光电探测器,其在零偏压下表现出200至850 nm的响应范围,并具备优异的稳定性和成像能力。回答下列问题:(1)、基态Ga原子的价电子排布图为 , 该基态原子最高能级的电子云轮廓图形状为。(2)、已知的熔点为1000℃,而GaCl3的熔点只有77.9℃,在270℃时,氯化镓以二聚体(Ga2Cl6)存在。
①和中Ga原子的杂化方式分别为、。
②的熔点比高的原因是。
③分子中存在。
A. 极性键 B. 配位键 C. 非极性键 D. 离子键 E. 氢键
(3)、[Ga(NH3)4Cl2]+中Ga3+的配位数为 , 1个该配位离子中含有σ键数目为(4)、某Ga、As组成的化合物晶胞结构如图所示,该晶体的密度为ρ g⋅cm-3 , 阿伏加德罗常数的值为。
①该化合物的化学式为。
②该晶胞中As原子间的最近距离为nm(用含ρ、的代数式表示)。
-
13、
I.以下是10种常见的有机物,请根据要求回答下列问题。

(1)以上属于芳香烃的是(填序号)。
(2)某烃与氢气1:1加成后得到①,该烃的结构简式可能有种。
(3)②分子中最多有个碳原子在同一直线上。
(4)③的核磁共振氢谱中有组峰。
(5)④属于(填“醇类”或“酚类”),写出④中官能团的电子式。
(6)⑥中的官能团的名称为。
(7)以上物质中属于同系物的是;属于同分异构体的是。
(8)⑨的一氯代物有种,其中一种一氯代物的核磁共振氢谱显示有4组峰,且峰面积比为3:4:4:2,写出该一氯代物的结构简式。
Ⅱ.
(9)准确称取4.4g某有机物样品X(只含C、H、O三种元素),将有机物X经充分燃烧后的产物依次通过浓硫酸和碱石灰,二者质量分别增加3.6g和8.8g。又知有机物X的质谱图和红外光谱图分别如图所示,核磁共振氢谱只有3组峰,则该有机物X的结构简式可能为(任写一种)。

(10)已知共轭二烯与含有双键的化合物相互作用,能生成六元环状化合物,例如
 , 在一定条件下,异戊二烯
, 在一定条件下,异戊二烯 和丙烯腈(CH2=CHCN)能发生类似上述的反应,生成两种化合物(互为同分异构体),写出任意一种产物的结构简式。
和丙烯腈(CH2=CHCN)能发生类似上述的反应,生成两种化合物(互为同分异构体),写出任意一种产物的结构简式。 -
14、氮化硼是重要的无机非金属材料,在工业生产中有着重要的作用。常见的三种氮化硼晶体结构如下图所示:

下列叙述错误的是
A、h-BN晶体中存在大π键 B、c-BN晶体中N位于由B构成的四面体空隙中 C、w-BN晶体中B的配位数为6 D、晶体硬度大小关系为c-BN>h-BN -
15、向CuSO4溶液中逐滴加入氨水至过量,得到深蓝色的溶液,将溶液分为两份,分别进行下列实验操作:
序号
实验操作
实验现象或结论
①
再加入95%乙醇
析出深蓝色晶体
②
向深蓝色溶液中插入打磨至光亮的铁丝
一段时间后,铁丝表面析出有金属光泽的红色固体
下列说法不正确的是
A、和中N的杂化方式不同 B、实验①析出深蓝色晶体为[Cu(NH3)4]SO4·H2O C、实验②说明[Cu(H2O)4]2+与NH3的反应是可逆反应 D、上述实验可得配离子的稳定性顺序为:[Cu(NH3)4]2+˃[Cu(H2O)4]2+ -
16、铁有δ、γ、α三种同素异形体,其晶胞结构如图所示,下列判断正确的是
 A、δ、γ、α铁晶体中存在金属阳离子和阴离子 B、γ-Fe晶胞中所含有的铁原子数为14 C、δ、α两种晶胞中铁原子周围等距离且最近的铁原子个数之比为4∶3 D、若α-Fe晶胞棱长为acm,γ-Fe晶胞棱长为bcm,则两种晶体的密度比为b3∶a3
A、δ、γ、α铁晶体中存在金属阳离子和阴离子 B、γ-Fe晶胞中所含有的铁原子数为14 C、δ、α两种晶胞中铁原子周围等距离且最近的铁原子个数之比为4∶3 D、若α-Fe晶胞棱长为acm,γ-Fe晶胞棱长为bcm,则两种晶体的密度比为b3∶a3 -
17、设NA为阿伏加德罗常数的值,下列说法正确的是A、1.8g D2O含有中子数为NA B、2.24L乙烯中含σ键的数目为0.5 NA C、1mol 配合物[Co(NH3)5Cl]Cl2完全电离的Cl-数目为3NA D、20g SiC晶体中Si―C键的数目为2NA
-
18、咪唑类盐可作离子液体,在电池、有机合成和催化剂方面具有广泛的用途。下图是一类咪唑类盐的结构简式,其中X、Y、Z均是短周期主族元素,X、Z同主族,基态Y原子和基态Z原子核外电子均有5种空间运动状态,基态X原子的最高能级的不同轨道中均有电子且自旋方向相同。下列说法正确的是
 A、简单氢化物的沸点: B、电负性: C、原子半径: D、最高价氧化物对应水化物的酸性:
A、简单氢化物的沸点: B、电负性: C、原子半径: D、最高价氧化物对应水化物的酸性: -
19、下列说法正确的是A、超分子“杯酚”具有分子识别的特性,利用此特性可分离和 B、利用红外光谱可以测定分子的相对分子质量 C、苹果酸
 含有1个手性碳原子
D、基态S原子核外电子的运动状态有9种
含有1个手性碳原子
D、基态S原子核外电子的运动状态有9种
-
20、下列除杂试剂和方法的选择均正确的是
选项
物质(杂质)
除杂试剂
方法
A
苯(溴)
水
过滤
B
甲烷(乙烯)
酸性高锰酸钾溶液
洗气
C
CO2(HCl)
碳酸钠
洗气
D
苯甲酸(泥沙,NaCl)
蒸馏水
重结晶
A、A B、B C、C D、D