相关试卷
-
1、
回答下列问题:
Ⅰ.(红棕色)和(无色)之间发生反应:。将一定量气体充入体积为的恒容密闭容器中,控制反应温度为。
(1)下列可以说明该反应达到平衡的是_______(填标号)。
A. B. C. 容器内气体的颜色不再变化 D. 混合气体的压强不再变化 (2)在温度为的条件下,向该恒容密闭容器中充入 , 随时间的变化曲线如图所示。

①a~b四个点中,的点有________。
②反应进行到时,的转化率是________。
③下列措施能使该反应速率加快的是________(填标号)。
A.增大的浓度 B.增大容器体积 C.恒容条件下充入He
Ⅱ.反应速率的调控对于化工生产有重大的意义。
(3)小王同学为了探究锌片与盐酸反应过程中的速率变化,他在稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值):
时间(min)
1
2
3
4
5
氢气体积(mL)(标准状况)
50
191
414
526
570
①为加快该反应的反应速率,可采取的措施是:________。
②求2~4分钟时间段以盐酸的浓度变化来表示的该反应速率________。(设溶液体积不变)
③小蒋同学认为在盐酸溶液中滴入少量的溶液可以加快反应的速率,请从电化学的角度给于分析:构成的原电池中负极反应式为________;溶液中移向________极(填“正”或“负”)。
(4)已知与硫酸的反应为 , 某研究小组为研究外界条件对化学反应速率的影响,设计实验如下,请回答下列问题:
实验
序号
反应
温度
加入
溶液的体积
加入0.1mol/L
溶液的体积
加入水
的体积
出现浑
浊的时间
℃
mL
mL
mL
S
一
20
2
2
0
二
40
2
0
三
20
1
2
①________。________。
②、、由大到小的顺序是________。
-
2、是生产多晶硅的副产物。利用对废弃的锂电池正极材料进行氯化处理以回收、等金属,工艺路线如下:

回答下列问题:
(1)、中元素的化合价为 , 在元素周期表中的位置是。(2)、已知烧渣是LiCl、CoCl2和SiO2的混合物,生成该混合物的化学方程式是。(3)、“500℃焙烧”后剩余的应先除去,否则水浸会因与水剧烈反应生成硅酸和另一种酸而产生大量烟雾,写出与水反应的化学方程式。(4)、已知滤饼2主要为 , 沉钴反应的离子方程式为。(5)、鉴别洗净的“滤饼3”和固体中金属元素常用方法的名称是。(6)、“850℃煅烧”时发生的反应中氧化剂与还原剂的物质的量之比为。 -
3、
某研究性学习小组对二氧化硫的制备、性质以及含量测定进行探究。

Ⅰ.制备二氧化硫:用70%的浓硫酸与固体反应制备气体
(1)制备气体最合适的发生装置是(填写字母),反应的化学方程式为。
Ⅱ.某实验小组利用如图装置模拟古法制硫酸并进行性质探究。

已知:①“绿矾”高温受热可完全分解得红棕色固体和气体混合物;
②熔点-75.5℃,沸点-10℃;熔点16.8℃,沸点44.8℃。
(一)制取硫酸:实验开始前打开活塞、 , 关闭活塞 , 通入一段时间后,关闭活塞、 , 打开活塞 , 用酒精喷灯高温加热绿矾。
(2)①C装置中覆盖食用油的目的是。
②B装置的作用是和分离出(填化学式)。
(二)探究的性质:在装置C中先后加入同浓度同体积不同的钡盐溶液,控制食用油油层厚度一致、通入流速一致。四次实验分别得到如表图:
①已煮沸的
②未煮沸的


③已煮沸的
④未煮沸的


(3)图中,用化学用语解释曲线①缓慢下降的原因;对比四组实验分析,②中发生反应(写离子方程式)。对比②④实验分析,④中还发生反应(写离子方程式)使溶液酸性增强。
(4)上述四次实验中有白色沉淀生成的是(填编号)。
Ⅲ.二氧化硫的处理:某化工厂用如图所示工艺流程除去燃煤产生的。

(5)写出在催化剂条件下总反应的化学方程式。
(6)过程Ⅱ发生反应的离子方程式为。
-
4、水煤气变换反应为: , 我国学者结合实独与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用标注。下列说法正确的是
 A、水煤气变换反应的 B、步骤③的化学方程式为: C、步骤⑤只有非极性键H-H键形成 D、该历程中需要吸收的最大能量
A、水煤气变换反应的 B、步骤③的化学方程式为: C、步骤⑤只有非极性键H-H键形成 D、该历程中需要吸收的最大能量 -
5、实验室模拟氨催化氧化法制硝酸的装置如图所示(无水CaCl2可用于吸收氨气),下列说法错误的是
 A、装置①、②、⑤依次盛装碱石灰、无水CaCl2、NaOH溶液 B、装置③中气体呈红棕色 C、装置④中溶液可使紫色石蕊溶液变红,说明有HNO3生成 D、通空气的主要作用是鼓出氨气,空气可用N2代替
A、装置①、②、⑤依次盛装碱石灰、无水CaCl2、NaOH溶液 B、装置③中气体呈红棕色 C、装置④中溶液可使紫色石蕊溶液变红,说明有HNO3生成 D、通空气的主要作用是鼓出氨气,空气可用N2代替 -
6、下列离子方程式书写正确的是A、通入水中制氯水: B、少量通入溶液: C、稀硝酸与氯化亚铁混合: D、溶液与少量溶液混合:
-
7、设为阿伏加德罗常数的值。下列说法正确的是A、与完全反应时转移的电子数为 B、常温下,铁与足量的浓硝酸反应,转移的电子数为 C、固体中含离子数目为 D、标准状况下,中含有的共价键数目为
-
8、在相同条件下研究催化剂Ⅰ、Ⅱ对反应的影响,各物质浓度随反应时间的部分变化曲线如图,则
 A、无催化剂时,反应不能进行 B、与催化剂Ⅰ相比,Ⅱ的催化效果更好 C、a曲线表示使用催化剂Ⅱ时X的浓度随的变化 D、使用催化剂Ⅰ时,内,
A、无催化剂时,反应不能进行 B、与催化剂Ⅰ相比,Ⅱ的催化效果更好 C、a曲线表示使用催化剂Ⅱ时X的浓度随的变化 D、使用催化剂Ⅰ时,内, -
9、部分含硫物质的分类与相应化合价关系如图所示,下列推断不合理的是
 A、a与b反应可产生淡黄色固体 B、c既可被氧化,也可被还原 C、加热时d的浓溶液与铜反应可生成b D、酸雨的形成涉及b→e→d→c的转化
A、a与b反应可产生淡黄色固体 B、c既可被氧化,也可被还原 C、加热时d的浓溶液与铜反应可生成b D、酸雨的形成涉及b→e→d→c的转化 -
10、实验室用加热和固体混合物的方法制取少量氨气。实验室制取时,下列装置能达到相应实验目的的是


A.生成
B.干燥


C.收集
D.吸收尾气
A、A B、B C、C D、D -
11、以化合物Ⅰ为原料,利用代谢工程和合成生物学技术可实现苯乙烯的绿色合成,进而制各种高级芳醇,合成路线如图(微生物酶、部分反应条件略)。
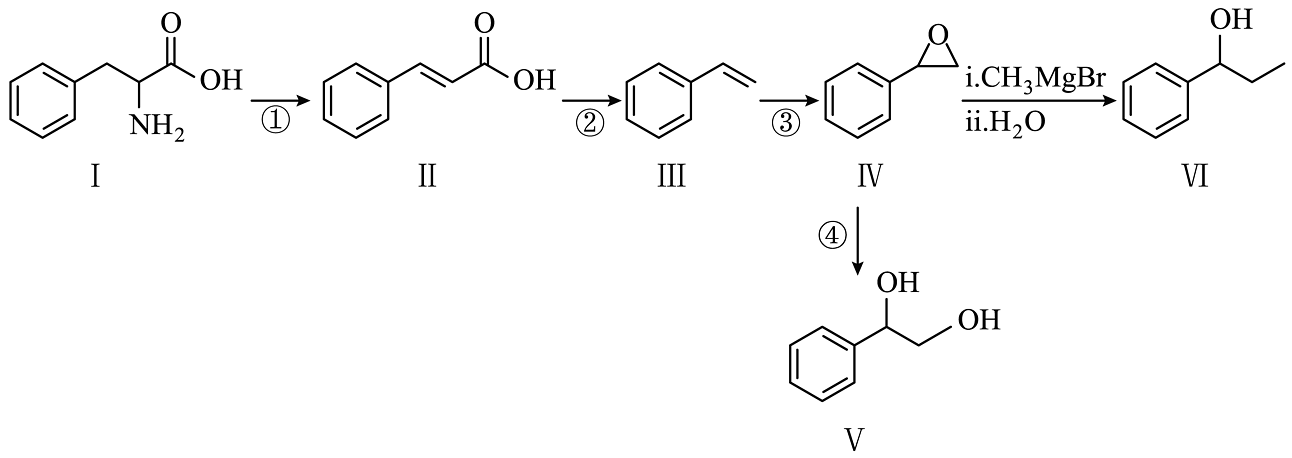
已知:
(1)、化合物Ⅰ的分子式为;其中,含氮官能团的名称为。(2)、对化合物Ⅱ,分析预测其可能的化学性质,完成下表。序号
反应试剂、条件
反应形成的新结构
反应类型
a

b
酯化反应
(3)、反应②的化学方程式可表示为: , 化合物Z为。(4)、化合物Ⅳ的某同分异构体含有苯环,在核磁共振氢谱图上只有4组峰,且峰面积之比为1:2:2:3,其结构简式为(写一种)。(5)、关于上述合成路线中的相关物质及转化,下列说法正确的有___________(填标号)。A、化合物Ⅰ与 混合,最多可生成2种二肽
B、反应①中,有键和键的断裂
C、反应③中,存在C原子杂化方式的改变,且有手性碳原子形成
D、若反应④是原子利用率100%的反应,则另一反应物为直线形分子
(6)、参考上述合成路线,以苯、为原料,合成
混合,最多可生成2种二肽
B、反应①中,有键和键的断裂
C、反应③中,存在C原子杂化方式的改变,且有手性碳原子形成
D、若反应④是原子利用率100%的反应,则另一反应物为直线形分子
(6)、参考上述合成路线,以苯、为原料,合成 。
。①由合成
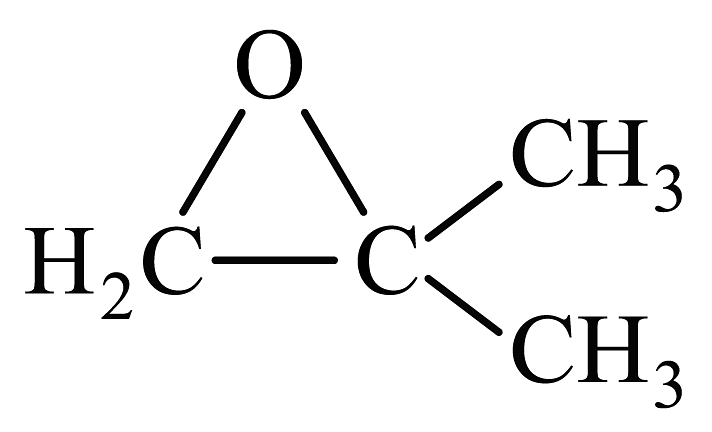 , 第一步反应的化学方程式为(注明反应条件)。
, 第一步反应的化学方程式为(注明反应条件)。②从苯出发,第一步反应的化学方程式为(注明反应条件)。
-
12、铂族金属是国家战略性金属,被誉为“现代工业维他命”。从某矿渣[含钯(Pd)、铂(Pt)、FeS、NiS及等]中提取Pd、Pt、Ni的工艺如下。
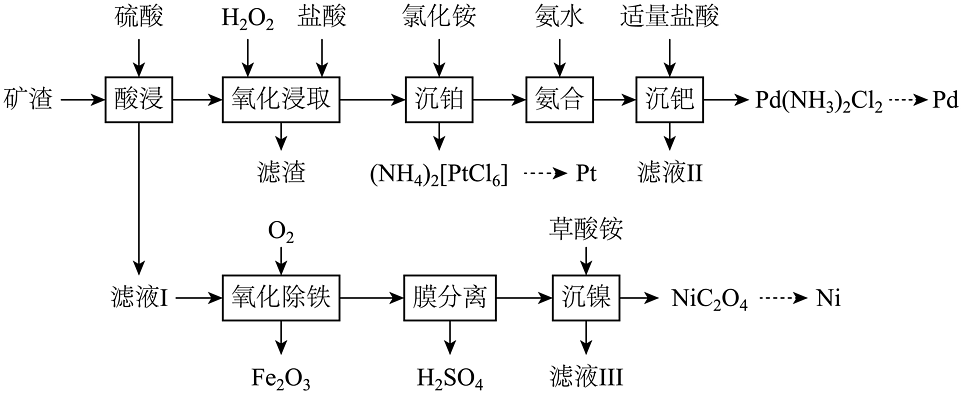
已知:Pd、Pt经“氧化浸取”转化为、;“氨合”后,Pd(Ⅱ)主要以的形式存在;常温下,的 , 。
(1)、Pt、Pd与Fe为同族元素,位于元素周期表的区。(2)、“氧化浸取”时,Pd发生反应的化学方程式为。(3)、“滤液Ⅱ”中的溶质可在工序中循环利用。(4)、“氧化除铁”时,温度为180℃,该过程主要发生两步反应:(ⅰ)
(ⅱ)(填离子方程式)。
(5)、常温下,“沉镍”时,需调节溶液pH=2,此时。(6)、含钯催化剂可与其他催化剂协同催化乙烯氧化为乙醛的反应,该催化氧化反应经历如图所示5步(①→⑤),其中发挥催化作用的阳离子有和。 (7)、含Pd、Cs、I的化合物可用于太阳能电池材料。一定条件下,其中一种晶体可由立方结构(结构单元如图ⅰ所示)转化为四方结构(晶胞结构如图ⅱ所示),两种结构的棱边夹角均为90°,且转化过程中原子个数比保持不变。
(7)、含Pd、Cs、I的化合物可用于太阳能电池材料。一定条件下,其中一种晶体可由立方结构(结构单元如图ⅰ所示)转化为四方结构(晶胞结构如图ⅱ所示),两种结构的棱边夹角均为90°,且转化过程中原子个数比保持不变。
①立方结构中Pd、Cs、I的原子个数比为;
②立方结构单元与四方晶胞结构的密度之比为。
-
13、
溶解过程常伴随热量变化。
Ⅰ.配制500mL 0.5mol/L盐酸。
(1)需12mol/L浓盐酸的体积为________mL(精确至小数点后一位)。
(2)该过程不需用到的仪器有________(填标号)。
A.
 B.
B. C.
C. D.
D. E.
E.
(3)下列操作会导致所配制溶液的浓度偏高的是___________(填标号)。
A. 转移溶液时部分溶液洒出 B. 转移溶液时未洗涤烧杯内壁 C. 定容时俯视刻度线 D. 加水超过刻度线,将多余液体吸出 Ⅱ.测定的溶解焓:
已知:在不同温度下的溶解度如下表:
温度/℃
10
20
30
40
溶解度/g
0.18
0.17
0.15
0.14
(4)利用量热法测定
初步实验 甲同学取一定质量固体完全溶解于一定体积的水中,利用量热计测算溶解前后体系的温度差,代入公式 , 再计算得出。
发现问题 ①甲同学实验结果误差较大,乙同学结合在水中的溶解性,分析其原因是________。
优化实验 ②乙同学根据相关原理间接测算:先测算固体与过量稀盐酸反应的焓变;再测算反应________(填离子方程式,需注明物质的聚集状态)的焓变。最后,计算得出为。
(5)为避免实验过程热量损失引起实验误差,该小组同学尝试其他实验方案。
查阅资料 不同温度下,物质的溶度积常数与满足(R、C为常数,)
实验思考 ①根据饱和溶液中和的关系,推出________[用仅含的式子表示,忽略水的电离]。测定不同温度下饱和溶液的pH,再结合相应温度下水的离子积常数 , 即可求算出不同温度下。
设计实验 方案1 将20℃的饱和溶液逐步升温至40℃,每隔5℃测量并记录溶液pH;
方案2 将40℃的饱和溶液逐步降温至20℃,每隔5℃测量并记录溶液pH。
②应选择________(填“方案1”或“方案2”)进行实验;选择该方案的依据是________。
数据处理 绘制随的变化曲线如图。
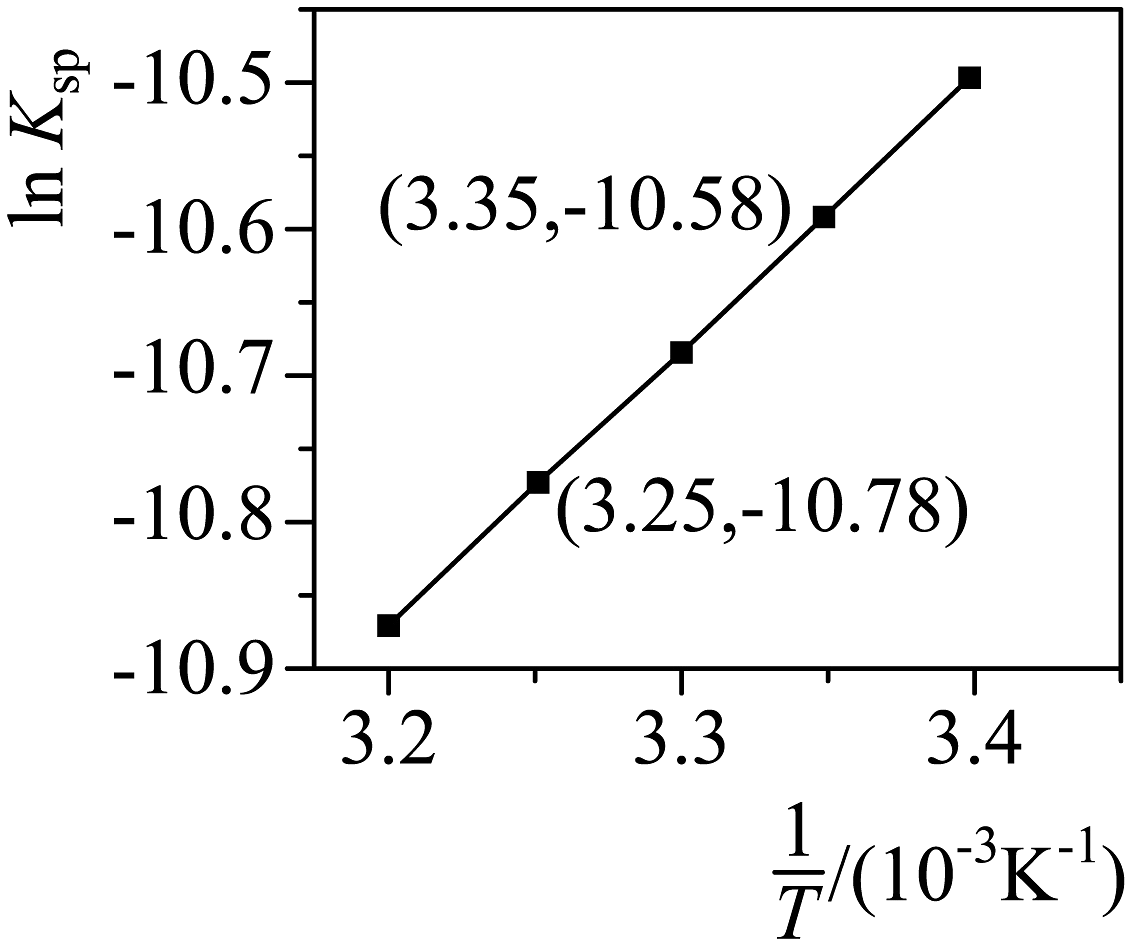
③根据公式,利用直线的斜率值,计算________(保留三位有效数字)。
-
14、化学镀镍废水经分离处理后得到含磷废液(主要含)和含镍废液(主要含),分别通入如图所示电解装置的两极室回收磷、镍。已知:是一元中强酸;25℃时,的、、。电解过程中,下列说法不正确的是
 A、阳极的主要反应为 B、Ⅰ室溶液的pH逐渐增大,Ⅱ室溶液的pH逐渐减小 C、理论上,每生成1mol Ni,同时处理0.5mol D、理论上,电路中每转移1mol , Ⅲ室溶液质量减少65g
A、阳极的主要反应为 B、Ⅰ室溶液的pH逐渐增大,Ⅱ室溶液的pH逐渐减小 C、理论上,每生成1mol Ni,同时处理0.5mol D、理论上,电路中每转移1mol , Ⅲ室溶液质量减少65g -
15、四种燃煤烟气脱硫方法的原理如图,下列说法不正确的是
 A、方法1中,吸收前后的溶液中硫元素的化合价未发生改变 B、若烟气中还含有 , 采用方法2可实现同时脱硫脱硝 C、方法3中能循环利用的物质是NaOH D、方法4中与CO反应,氧化剂与还原剂的物质的量之比为2:1
A、方法1中,吸收前后的溶液中硫元素的化合价未发生改变 B、若烟气中还含有 , 采用方法2可实现同时脱硫脱硝 C、方法3中能循环利用的物质是NaOH D、方法4中与CO反应,氧化剂与还原剂的物质的量之比为2:1 -
16、水煤气变换反应是获取的重要方式之一,在不同催化剂作用下,其反应历程如图所示(*表示吸附态)。下列说法正确的是
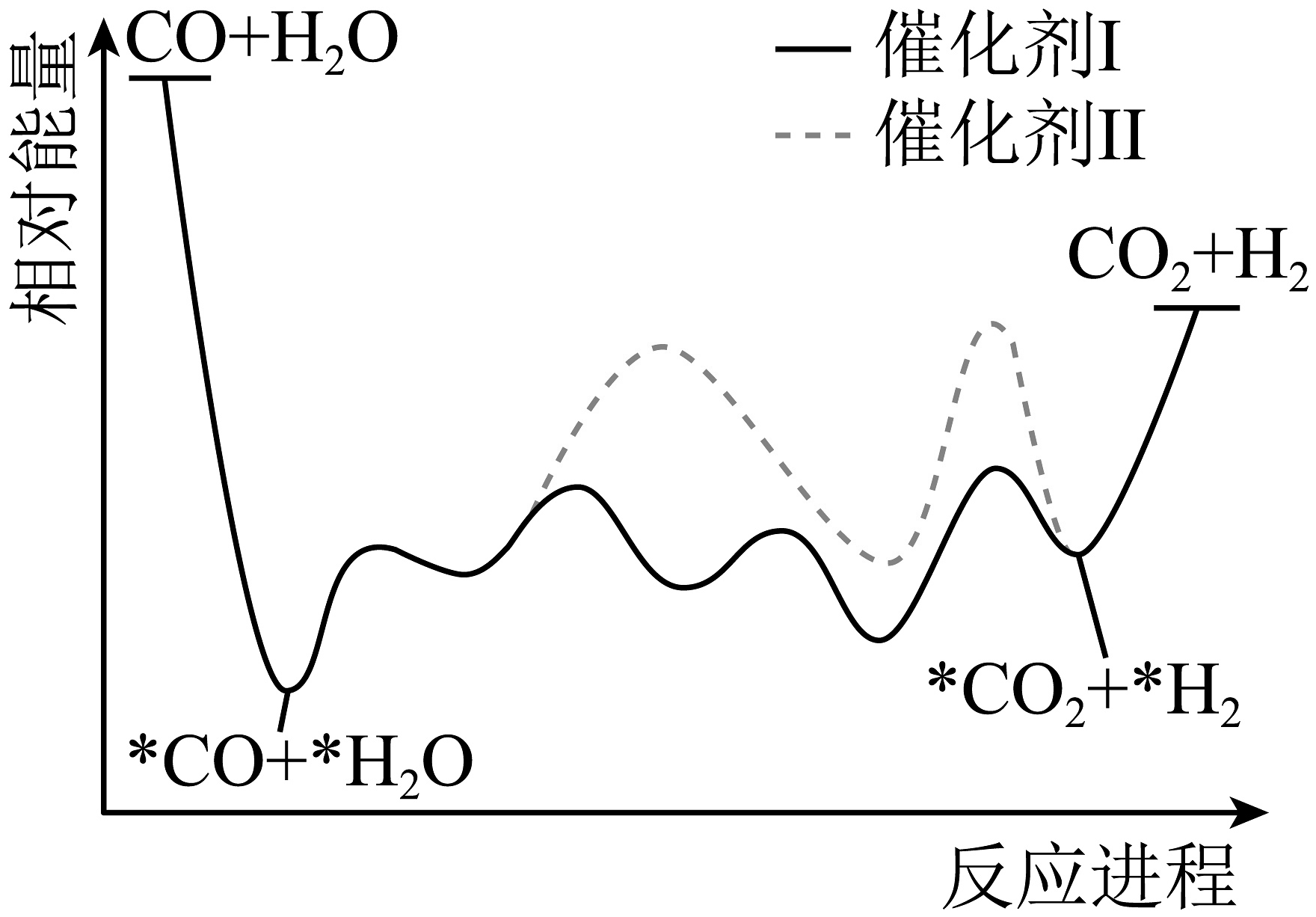 A、使用Ⅰ、Ⅱ,反应历程均分4步进行 B、反应达平衡时,增大压强,增大 C、使用Ⅰ时,反应体系更快达到平衡 D、Ⅰ、Ⅱ均能降低反应的焓变
A、使用Ⅰ、Ⅱ,反应历程均分4步进行 B、反应达平衡时,增大压强,增大 C、使用Ⅰ时,反应体系更快达到平衡 D、Ⅰ、Ⅱ均能降低反应的焓变 -
17、化合物可作催化剂,所含的5种主族元素在每个短周期均有分布,W与Z同族,X、W、Y同周期且原子序数依次递增。X与W的基态原子未成对电子数相同,W的基态原子p能级电子数与s能级电子数相等。下列说法正确的是A、第一电离能:W>Y B、最高价氧化物的水化物的酸性:X>Z C、简单氢化物的沸点:Z>W D、和的VSEPR模型均为四面体形
-
18、实验室利用如图所示装置模拟氨的催化氧化实验。用酒精灯预热催化剂至红热后,移开酒精灯并向试管中注入浓氨水;一段时间后,烧瓶中有红棕色气体产生,再向烧瓶中注入浓氨水,烧瓶中有白烟产生。下列说法正确的是
 A、每消耗0.1mol 生成0.1mol B、催化剂持续红热,说明氨的催化氧化反应为吸热反应 C、烧瓶中有红棕色气体产生,说明被直接氧化为 D、烧瓶中所产生的白烟的主要成分为
A、每消耗0.1mol 生成0.1mol B、催化剂持续红热,说明氨的催化氧化反应为吸热反应 C、烧瓶中有红棕色气体产生,说明被直接氧化为 D、烧瓶中所产生的白烟的主要成分为 -
19、下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
选项
陈述Ⅰ
陈述Ⅱ
A
当镀层破损时,马口铁(镀锡钢板)比白铁皮(镀锌钢板)更难被腐蚀
用牺牲阳极法防止金属腐蚀
B
冠醚可用于识别碱金属离子
不同空穴大小的冠醚可与不同的碱金属离子形成超分子
C
酸性:
烷基是推电子基团,烷基越长推电子效应越小
D
向溴乙烷水解后的上层溶液中,滴入几滴溶液,有淡黄色沉淀生成
溴乙烷中存在溴离子
A、A B、B C、C D、D -
20、设为阿伏加德罗常数的值。下列说法正确的是A、22.4L乙炔中含有σ键的数目为3 B、1L 1.5 溶液中的数目为1.5 C、46g 和的混合气体含有的原子数目为3 D、溶液与溶液反应生成1mol S,转移电子数目为2