相关试卷
-
1、新质生产力涵盖创新材料、新能源、生物医药等产业链。下列说法错误的是( )A、具有储氢潜力的新型材料碳纳米管属于单质 B、创新药氢溴酸氘瑞米德韦片中所含氘与氕互为同位素 C、可精确控制硬化过程的可编程水泥属于无机非金属材料 D、具有独特光学、电学性能的纳米半导体CdTe量子点属于胶体
-
2、研究氮的氧化物(如:NO、、)和氮的氢化物都有广泛的用途,如:和可作为运载火箭的推进剂。(1)、已知: 。现将2mol 放入1L恒容密闭容器中,平衡体系中的体积分数()随温度的变化如图所示。
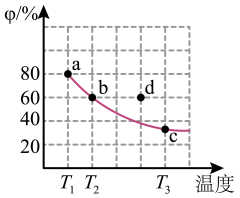
①d点v(正)v(逆)(填“>”“=”“<”)。
②a、b、c三点中平衡常数、、由小到大是。
③在时,的平衡转化率为;若平衡时的总压为100kPa,则该反应平衡常数(保留到小数点后1位)。
(2)、NO氧化为的反应为: , 该反应分如下两步进行:Ⅰ. (较快)
Ⅱ. (较慢)
在恒容的密闭容器中充入一定量的NO和 , 保持其它条件不变,控制反应温度分别为和 , c(NO)随t(时间)的变化如图所示。

在反应时间相同时,条件下转化的NO量(填“大于”“等于”“小于”)条件下转化的NO量,其本质原因是(结合反应Ⅰ和Ⅱ的反应热进行分析)。
(3)、肼除了可作火箭的推进剂外,还可用于新型环保电池中,电池工作原理如图所示。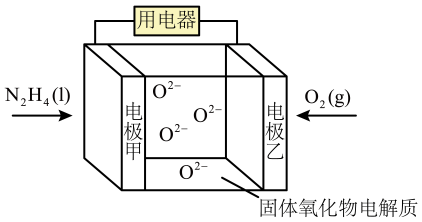
①向移动(填“电极甲”或“电极乙”)。
②该电池的负极反应式为。
-
3、二氯异氰尿酸钠(结构为
 )是一种非常高效的强氧化性消毒剂。常温下是白色固体,难溶于冷水;合成二氯异氰尿酸钠的反应为 。某同学在实验室用如下装置制取二氯异氰尿酸钠(部分夹持装置已略)。
)是一种非常高效的强氧化性消毒剂。常温下是白色固体,难溶于冷水;合成二氯异氰尿酸钠的反应为 。某同学在实验室用如下装置制取二氯异氰尿酸钠(部分夹持装置已略)。
请回答下列问题:
(1)、Cl的价电子轨道表达式为。(2)、仪器a的名称是;仪器D中的试剂是。(3)、A中烧瓶内发生反应的化学方程式为。(4)、装置B的作用是;如果没有B装置,NaOH溶液会产生的不良结果是。(5)、待装置C时(填实验现象),再滴加溶液,反应过程中需要不断通入Cl2的目的是。(6)、实验室测定二氯异氰尿酸钠样品中有效氯的原理如下:准确称取m g样品,配成100mL溶液,取20.00mL所配溶液于碘量瓶中,加入稀和过量KI溶液,充分反应后,加入淀粉溶液,用c mol/LNa2S2O3标准溶液滴定,滴到终点时,消耗Na2S2O3标准溶液的体积为V mL,则样品有效氯含量为%( )
-
4、催化剂催化水煤气变换反应:CO(g)+H2O(g)CO2(g)+H2(g) △H<0,过程示意图如图所示,下列说法错误的是( )
 A、过程I、过程II中都有水参与反应 B、该反应反应物总能量高于生成物总能量 C、使用催化剂不能改变水煤气变换反应的△H D、催化过程中既有极性键的断裂和形成,也有非极性键的断裂和形成
A、过程I、过程II中都有水参与反应 B、该反应反应物总能量高于生成物总能量 C、使用催化剂不能改变水煤气变换反应的△H D、催化过程中既有极性键的断裂和形成,也有非极性键的断裂和形成 -
5、用下列装置进行相应实验,能达到实验目的的是( )
A
B
C
D
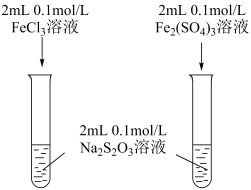
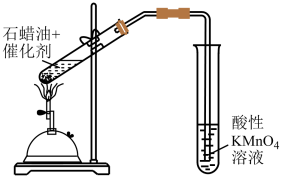


探究Cl-对Fe3+与S2O反应速率的影响
验证石蜡油发生了裂化(或裂解)反应
融化Na2CO3固体
干燥一氯甲烷
A、A B、B C、C D、D -
6、设为阿伏加德罗常数的值,下列说法正确的是( )A、标准状况下,2.24L中含有的极性共价键数目为 B、5.6 g铁与足量硫粉反应,转移的电子数为 C、含0.1mol的水溶液中含有的原子数目为 D、的溶液中含铬微粒的数目为
-
7、某同学利用下图所示装置探究金属的腐蚀与防护条件。

下列说法不合理的是( )
A、①区Cu电极上产生气泡,Fe电极附近滴加K3Fe(CN)6溶液后出现蓝色,Fe被腐蚀 B、②区Cu电极附近滴加酚酞后变成红色,Fe电极附近滴加K3[Fe(CN)6]溶液出现蓝色,Fe被腐蚀 C、③区Zn电极的电极反应式为Zn-2e-=Zn2+ , Fe电极附近滴加K3[Fe(CN)6]溶液未出现蓝色,Fe被保护 D、④区Zn电极的电极反应式为2H2O+2e-=H2↑+2OH- , Fe电极附近滴加K3[Fe(CN)6]溶液出现蓝色,Fe被腐蚀 -
8、化学与我们的生活息息相关,下列有关说法正确的是( )A、太阳能电池的主要材料是SiO2 B、明矾可用于自来水的杀菌消毒 C、大气中PM2.5比表面积大,吸附能力强,能吸附许多有毒有害物质 D、75%的医用酒精常用于消毒,用95%的酒精消毒效果更好
-
9、有机化合物H为某药物中间体,一种合成化合物H的路线如图。

已知:Ⅰ.(R为烃基或H原子,X为卤素原子,下同)
Ⅱ.

Ⅲ.

回答下列问题:
(1)、A的名称为 , H中含氧官能团的名称为醚键、。(2)、C的结构简式为。(3)、E→F的化学方程式为。(4)、B有多种同分异构体,其中能发生银镜反应和水解反应的芳香族化合物的同分异构体有种(不考虑立体异构),核磁共振氢谱有4组峰的同分异构体的结构简式为。(任写一个)(5)、 的合成路线如图(部分反应条件已略去),其中M和N的结构简式分别为和。
的合成路线如图(部分反应条件已略去),其中M和N的结构简式分别为和。
-
10、KMnO4是生活中常用的消毒剂。已知在酸性介质中墨绿色的易发生歧化反应,生成和MnO2 , 回答下列问题:(1)、实验(一)制备KMnO4。
“熔融”时分批加入MnO2粉末的目的是 , “熔融”时不需选用的仪器是(填标号)。
A.铁坩埚 B.玻璃棒 C.泥三角 D.坩埚钳
(2)、“抽滤”时选择乙装置,相对甲,乙的主要优点是(任写一条)。 (3)、“歧化”时锰元素进入产品的百分率约为%(保留三位有效数字),用盐酸代替CO2的后果是。(4)、工业上,常用“电解”代替“歧化”,提高锰元素利用率,电解的总反应方程式为。(5)、实验(二)测定产品纯度。
(3)、“歧化”时锰元素进入产品的百分率约为%(保留三位有效数字),用盐酸代替CO2的后果是。(4)、工业上,常用“电解”代替“歧化”,提高锰元素利用率,电解的总反应方程式为。(5)、实验(二)测定产品纯度。取wgKMnO4溶于水配成250mL溶液,取25.00mL于锥形瓶中,加入适量稀硫酸酸化,用Na2C2O4标准溶液滴定至终点,消耗标准溶液VmL。
下列叙述正确的是____(填标号)。
A、滴定终点时溶液由无色变为紫红色 B、滴定时眼睛始终注视锥形瓶中溶液颜色变化 C、若锥形瓶未干燥,测得结果会偏高 D、本实验需要托盘天平、量筒、容量瓶、滴定管等(6)、该产品的纯度为。 -
11、黄金除具备货币商品属性外,由于其优良特性,还可用作珠宝装饰、金触媒、超导体等。以含砷金精矿(成分为Au、FeAsS)为原料提炼黄金的工艺流程如图,请回答下列问题:
 (1)、焙烧时,FeAsS转化为两种有毒物质和一种红棕色固体,写出此反应的化学方程式:。(2)、焙烧温度对硫、砷的脱除率的影响如图所示,则最适宜的焙烧温度为℃,原因为。
(1)、焙烧时,FeAsS转化为两种有毒物质和一种红棕色固体,写出此反应的化学方程式:。(2)、焙烧温度对硫、砷的脱除率的影响如图所示,则最适宜的焙烧温度为℃,原因为。 (3)、磨砂的目的是。(4)、氰化过程中,通入O2将Au转化为Na[Au(CN)2](易溶于水),写出该反应的离子方程式:。(5)、滤渣的主要成分为、。(6)、at含Auw%的含砷金精矿通过上述流程(假设Au的损失率为5%)可制得tAu。
(3)、磨砂的目的是。(4)、氰化过程中,通入O2将Au转化为Na[Au(CN)2](易溶于水),写出该反应的离子方程式:。(5)、滤渣的主要成分为、。(6)、at含Auw%的含砷金精矿通过上述流程(假设Au的损失率为5%)可制得tAu。 -
12、常温下,用HCl(g)调节SrF2浊液的pH,测得在通入HCl(g)的过程中,体系中-lgc(X)(X代表Sr2+或F-)与的关系如图所示。下列说法错误的是( )

已知:SrF2为微溶于水,溶于盐酸,不溶于氢氟酸、乙醇和丙酮的固体。
A、 B、L2表示的变化情况 C、随着HCl的加入,SrF2溶解度逐渐增大 D、m、n点对应的溶液中均存在 -
13、异丁烯(
 )是重要的化工原料,可由异丁醇(
)是重要的化工原料,可由异丁醇( )脱水制得。异丁醇催化脱水时发生如下反应:
)脱水制得。异丁醇催化脱水时发生如下反应:反应1(主反应):

 (异丁烯,g)
(异丁烯,g)反应2(副反应):2


保持压强为100MPa不变,向一定体积的密闭容器中充入V(异丁醇)的混合气体(不参与反应),平衡时所得异丁醇的转化率、异丁烯的产率与温度的关系如图所示。下列说法错误的是( )
 A、反应1为消去反应,反应2为加成反应 B、保持其他条件不变,升高温度,反应1和反应2平衡均向正反应方向移动 C、100MPa、200℃时,V(异丁醇)起始比值越小,平衡时异丁烯的产率越高 D、100MPa、200℃时,若起始时将V(异丁醇)改为V(异丁醇) , 平衡时异丁烯的产率降低
A、反应1为消去反应,反应2为加成反应 B、保持其他条件不变,升高温度,反应1和反应2平衡均向正反应方向移动 C、100MPa、200℃时,V(异丁醇)起始比值越小,平衡时异丁烯的产率越高 D、100MPa、200℃时,若起始时将V(异丁醇)改为V(异丁醇) , 平衡时异丁烯的产率降低 -
14、常温下,在MoS2催化下可实现CH4向CH3OH的直接转化。原理如图。下列说法正确的是( )
 A、反应过程中,Mo的化合价未发生变化 B、生成甲醇的总反应为 C、MoS2降低了总反应的焓变 D、反应过程中有非极性键的断裂和形成
A、反应过程中,Mo的化合价未发生变化 B、生成甲醇的总反应为 C、MoS2降低了总反应的焓变 D、反应过程中有非极性键的断裂和形成 -
15、某小组为探究NaHSO3和NaHCO3溶液的相关性质,进行如下实验:常温下,用pH计测得NaHCO3溶液的pH为9.7,向该溶液中缓慢通入SO2 , 使溶质恰好变为NaHSO3(忽略体积变化,CO2全部逸出),测得NaHSO3溶液的pH为5.28。一段时间后,取少量NaHSO3溶液,滴加BaCl2溶液,产生白色沉淀,加入过量的盐酸,白色沉淀不溶解。下列叙述正确的是( )A、产生的白色沉淀为BaSO3 B、常温下, C、NaHSO3溶液中: D、久置于空气中的NaHSO3溶液的pH可能增大
-
16、下列实验设计及原理都错误的是( )
选项
实验设计
原理
A
利用NaOH溶液鉴别Al与Mg
Al会与NaOH溶液反应,而Mg不与其反应
B
分别加热Na2CO3与NaHCO3固体,并将可能产生的气体通入澄清石灰水,鉴别Na2CO3与NaHCO3
碳酸钠受热易分解,生成的CO2使澄清石灰水变浑浊
C
利用苯鉴别碘单质与高锰酸钾
二者在苯中的溶解度不同
D
利用紫色石蕊试液鉴别二氧化碳与二氧化硫
SO2具有漂白性
A、A B、B C、C D、D -
17、氧化铈(CeO2)常用作玻璃工业添加剂,在其立方晶胞中掺杂Y2O3 , Y3+占据原来Ce4+的位置,可以得到更稳定的结构,这种稳定的结构使得氧化铈具有许多独特的性质和应用,CeO2晶胞中Ce4+与最近O2-的核间距为apm。下列说法正确的是( )


已知:。
A、已知M点原子的分数坐标为(0,0,0),则N点原子的分数坐标为(1,0,1) B、CeO2晶胞中与Ce4+最近的Ce4+的个数为6 C、CeO2晶体的密度为 D、若掺杂Y2O3后得到n(CeO2):n(Y2O3)=0.6:0.2的晶体,则此晶体中O2-的空缺率为10% -
18、氢键在电池中的应用广泛,可精细调控电极和电解质的性质,提高可充电电池的性能。某可充电电池装置如图所示(其他阴离子不参与反应,已略去)。下列叙述错误的是( )
 A、放电时,电极X为负极 B、放电时,阳离子向电极Y迁移 C、充电时,电极Y与电源正极连接 D、充电时,电极X的电极反应式为
A、放电时,电极X为负极 B、放电时,阳离子向电极Y迁移 C、充电时,电极Y与电源正极连接 D、充电时,电极X的电极反应式为 -
19、代表阿伏加德罗常数的值。下列说法正确的是( )A、11.2LCO2含π键数目为 B、电解熔融CuCl2 , 阴极增重6.4g,外电路中通过电子的数目为 C、NaCl和NH4Cl的混合物中含1molCl- , 则混合物中质子数为 D、1.7gNH3完全溶于1LH2O所得的溶液中,NH3·H2O微粒的数目为
-
20、研究表明:在高压下可发生聚合,甚至改变成键方式。在高压下MgCO3中碳酸根离子形成环状三聚体(如图所示),下列说法正确的是( )
 A、该种环状三聚体是一种有机阴离子 B、该种环状三聚体中,O的杂化方式有2种 C、高压下,相较于单个碳酸根离子,该种环状三聚体更稳定 D、该种环状三聚体与Mg2+形成的化合物中,化学键种类有极性共价键、离子键及配位键
A、该种环状三聚体是一种有机阴离子 B、该种环状三聚体中,O的杂化方式有2种 C、高压下,相较于单个碳酸根离子,该种环状三聚体更稳定 D、该种环状三聚体与Mg2+形成的化合物中,化学键种类有极性共价键、离子键及配位键