相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、寿山石的主要成分为 , X、Y、Z、W为四种原子序数递增的短周期不同族元素,X是周期表中半径最小的原子,基态Y原子有2个未成对电子,W的L层电子数是M层的2倍。下列说法正确的是A、原子半径Z<W B、简单氢化物的稳定性Y<W C、电负性Z>X D、Z最高价氧化物的水化物呈两性
-
2、“价-类-途”体现了元素化合物的内在联系和应用价值。氮及其化合物的三维关系图如图所示,下列说法不正确的是
 A、铵盐通过氧化还原反应直接得到X或W B、工业制硝酸的基础是X到Y C、雷雨天空气中存在的物质转化: D、汽车尾气处理中可能涉及反应:
A、铵盐通过氧化还原反应直接得到X或W B、工业制硝酸的基础是X到Y C、雷雨天空气中存在的物质转化: D、汽车尾气处理中可能涉及反应: -
3、中科院福建物构所制备了一种新型的铋基有机复合框架(),电池用其做电极能大大提高放电效率,电池结构如图所示,下列说法错误的是

已知:双极膜能在直流电场的作用下,将膜复合层间的解离成和并移向两极。
A、锌片为负极 B、放电时,电极上发生的反应: C、该电池工作时,锌片上每消耗锌,双极膜内将解离 D、铋基有机复合框架在电池中主要起吸附、催化转化为的作用 -
4、下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
选项
陈述Ⅰ
陈述Ⅱ
A
氯化铜在碱性溶液中生成沉淀
能与氨水反应生成络合离子
B
金属钠与水反应生成氢气
金属钠表面变暗
C
铜丝在氯气中燃烧生成氯化铜烟雾
铜丝质量增加
D
氯化铵受热易分解
可用加热法除去氯化钠中的氯化铵
A、A B、B C、C D、D -
5、和两种气体的制备和性质一体化探究实验装置(已省略夹持装置)如图所示。下列说法正确的是
 A、制备氯气可以采用浓盐酸与反应 B、A-2/B-2两处的品红溶液变色的原理相同,都是利用其氧化性 C、A-3/B-3两处的实验现象是一样的,都是蓝色石蕊试纸变红 D、试剂瓶C中的溶液若是氯化钡溶液,则会出现白色沉淀
A、制备氯气可以采用浓盐酸与反应 B、A-2/B-2两处的品红溶液变色的原理相同,都是利用其氧化性 C、A-3/B-3两处的实验现象是一样的,都是蓝色石蕊试纸变红 D、试剂瓶C中的溶液若是氯化钡溶液,则会出现白色沉淀 -
6、铋酸钠()是分析化学中的重要试剂。某同学设计实验制取铋酸钠,装置如图所示(加热和夹持仪器已略去),部分物质性质如表。
物质
性质
不溶于冷水,浅黄色
难溶于水,白色

下列说法错误的是
A、装置B用于除去中 B、装置C中反应的离子方程式为: C、拆除装置前必须进行的操作是关闭 , 打开 D、装置D用于除去多余的氯气 -
7、利用下列实验药品,不能达到实验目的的是
实验目的
实验药品
A
检验加碘盐中的
加碘盐、碘化钾溶液、淀粉溶液、白醋
B
判断淀粉是否水解
淀粉溶液、20%硫酸溶液、银氨溶液
C
比较镁和铝的金属性强弱
MgCl2溶液、AlCl3溶液、NaOH溶液
D
探究浓度对化学平衡移动的影响
K2CrO4溶液、HNO3溶液、NaOH溶液
A、A B、B C、C D、D -
8、亚氯酸钠()用于各种纤维和某些食品的漂白,其制备流程如下:
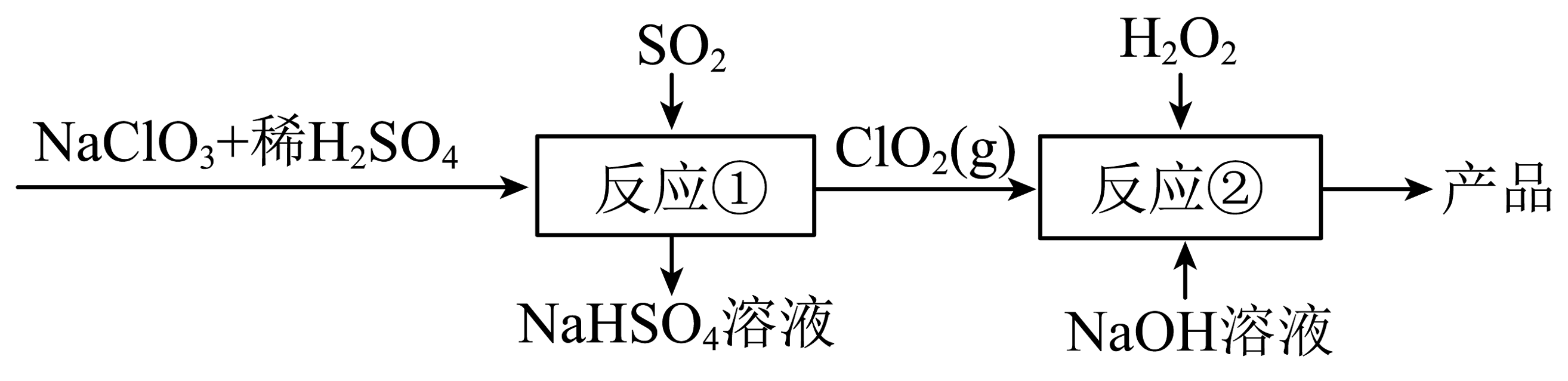
已知:下列有关离子反应错误的是
A、溶液呈碱性的原因: B、用足量氨水吸收含的尾气: C、反应①中主要发生的反应: D、反应②中主要发生的反应: -
9、利用绿矾()制备电极材料的前驱体的流程如下:
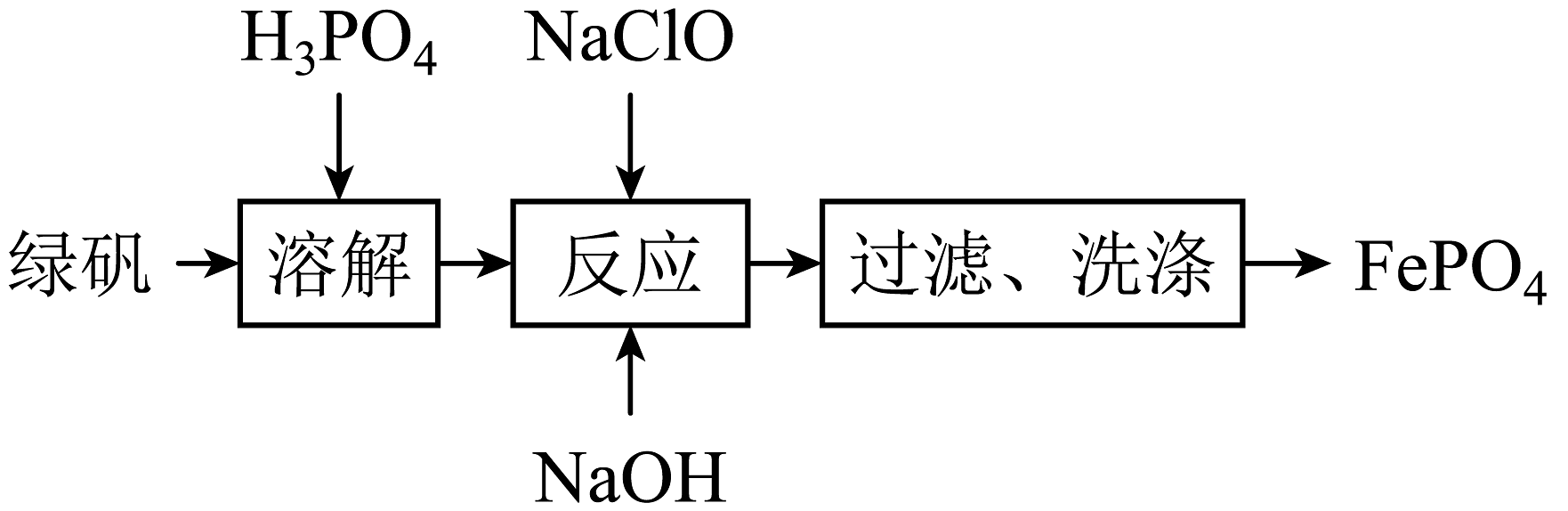
下列说法正确的是
A、溶解过程中可抑制的水解 B、可以用KSCN溶液判断反应是否完全 C、过滤需要的玻璃仪器有烧杯、玻璃棒、分液漏斗 D、反应中氧化剂与还原剂的物质的量之比为 -
10、下列选项中的物质能按图示路径一步转化,且甲和丙反应不能直接生成乙的是

选项
甲
乙
丙
A
B
C
C
D
A、A B、B C、C D、D -
11、设为阿伏加德罗常数的值。下列说法正确的是A、25℃,时,4g氦气所含分子数为 B、4.48L由乙烯、丙烯组成的混合气体中含有的氢原子数为 C、100mL的盐酸与醋酸溶液中氢离子数目均为 D、1mol与足量水蒸气反应转移电子数为
-
12、下列实验装置对应的操作正确的是
 A、加热NaOH溶液 B、制备乙酸乙酯 C、从碘水中萃取并分液提取碘 D、制备溴苯并证明发生取代反应
A、加热NaOH溶液 B、制备乙酸乙酯 C、从碘水中萃取并分液提取碘 D、制备溴苯并证明发生取代反应 -
13、下列化学用语表示正确的是A、基态铁原子价电子的轨道表示式:
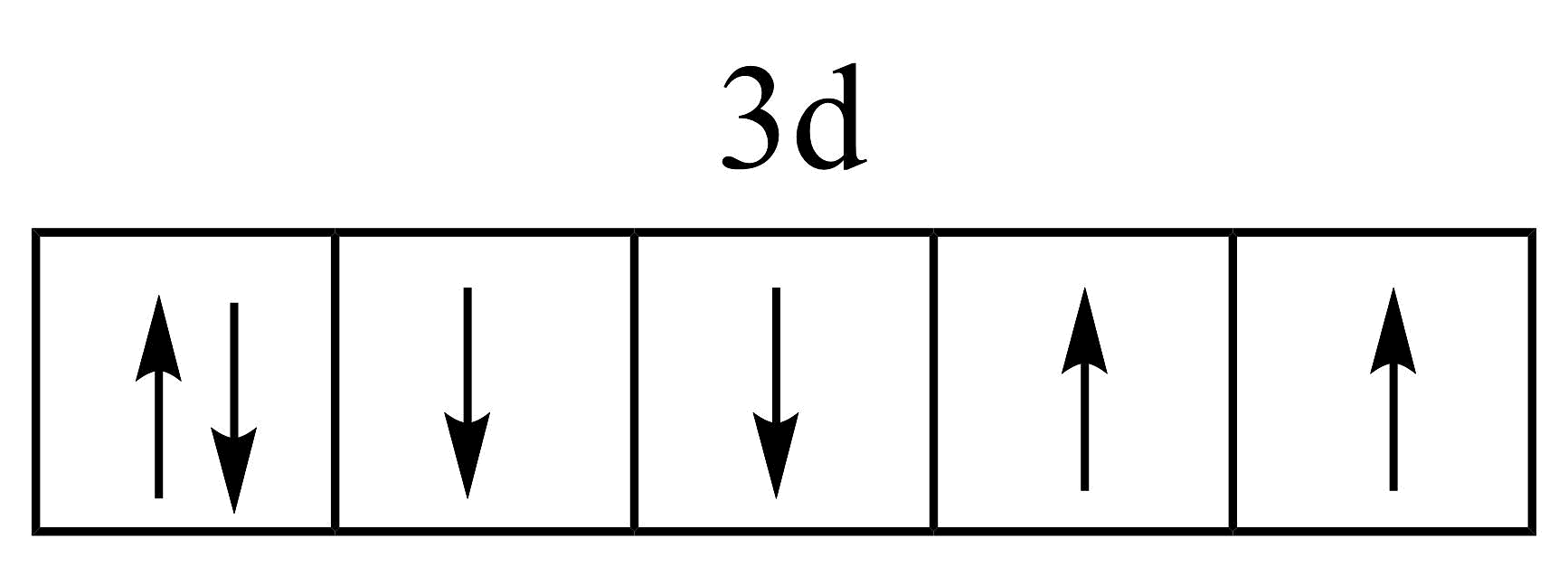 B、电子式表示NaH的形成过程:
B、电子式表示NaH的形成过程: C、的键电子云轮廓图:
C、的键电子云轮廓图: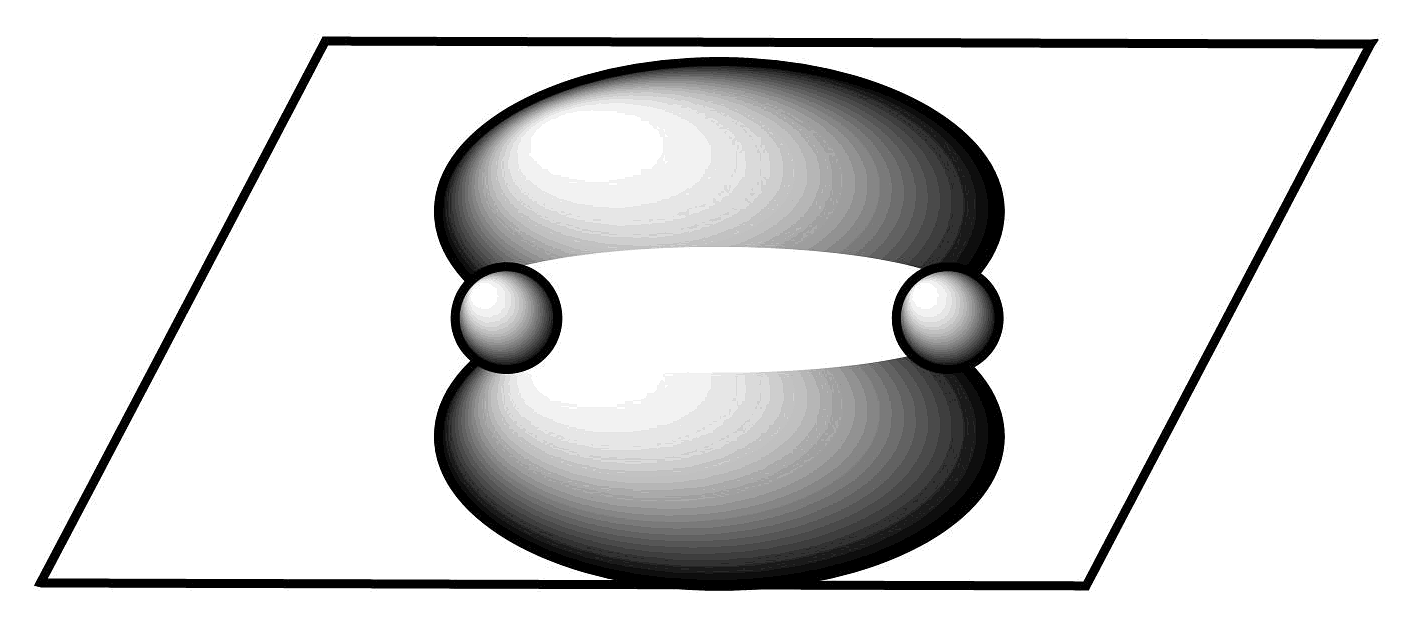 D、次氯酸的结构式:
D、次氯酸的结构式:
-
14、“扑热息痛”是重要的解热镇痛药,其结构如下。下列有关该物质的说法正确的是
 A、分子式为 B、含有2种官能团 C、所有原子可能处于同一平面 D、能与溴水发生加成反应
A、分子式为 B、含有2种官能团 C、所有原子可能处于同一平面 D、能与溴水发生加成反应 -
15、福建舰拥有世界上最先进的雷达系统,其雷达射频微波器件所用的碳化硅材料能实现电信号的可控改变。下列关于碳化硅的说法错误的是A、C原子的杂化类型为 B、属于高分子化合物 C、熔点高、硬度大 D、属于半导体材料
-
16、利用下图装置进行铁上电镀铜的实验探究。
装置示意图
序号
电解质溶液
实验现象

①
0.1mol/LCuSO4
+少量H2SO4
阴极表面有无色气体,一段时间后阴极表面有红色固体,气体减少。经检验电解液中有
②
0.1mol/LCuSO4
+过量氨水
阴极表面未观察到气体,一段时间后阴极表面有致密红色固体。经检验电解液中无元素
下列说法不正确的是
A、①中气体减少,推测是由于溶液中减少,且覆盖铁电极,阻碍与铁接触 B、①中检测到 , 推测可能发生反应: C、随阴极析出 , 推测②中溶液减少,平衡逆移 D、②中生成 , 使得比①中溶液的小,缓慢析出,镀层更致密 -
17、自然界中的局部氮循环如下图。

(1)上图含氮物质的各步转化中,属于氮的固定的是( 填数字序号)。
(2) NH3是氮循环中的重要物质,工业合成氨反应的化学方程式为。
(3)某化工厂出现泄漏,大量氨水进入循环水系统,使循环水中含氯杀菌剂(有效成分为Cl2)的杀菌效果降低、硝化作用增强,导致循环水的pH发生波动,最终造成设备腐蚀。
①下列有关氨对循环水影响的说法中,正确的是 ( 填字母序号)。
a.过量氨进入循环水后,水中NO和NO 含量会升高
b.过量氨进入循环水后,不会导致水体富营养化
c.循环水pH的波动中,pH的上升与氨水的碱性有关
d.为减少氨对杀菌剂杀菌效果的影响,可以改用非氧化性杀菌剂
②通过检测循环水中的c(NO)可判断循环水的水质是否恶化,c(NO)检测利用的是酸性条件下I-被NO 氧化为I2的反应,该反应的历程如下:
I. NO+2H+= NO++H2O
II. ……
III.2ONI= I2+2NO
II的离子方程式为。
(4)含NO 的废水可用二硫化亚铁(FeS2)处理,在反硝化细菌的作用下发生以下反应,请将离子方程式补充完整:14NO+ 5FeS2+H+ 7N2↑+10SO+
-
18、乙烯是来自石油的重要的化工原料,乙烯的产量通常用来衡量一个国家的石油化工发展水平。

完成下列填空:
(1)、反应③的有机产物的官能团名称是 .(2)、反应①、⑥的反应类型分别为、。(3)、反应①和反应②的反应方程式分别为、。(4)、反应④得到的产物聚乙烯用来制造塑料,其单体是乙烯,而比乙烯多一个碳原子的同系物也可以通过聚合反应得高聚物,也可以用来制塑料,该同系物的结构简式是 , 其聚合反应方程式是。(5)、石油通过分馏、裂化都可以得到 , 其分馏、裂化过程属于物理变化的是 , 一氯取代有种。 -
19、硫化氢大量存在于天然气及液化石油气中,近年来发现可用于制取氢气、合成硫醇等。回答下列问题:(1)、D.Berk等学者设计的用FeS催化分解包括下列反应:
I.
Ⅱ.
Ⅲ.
①(用、表示)。
②已知单质硫气态时以形式存在(结构为)。键能、、 , 则。
(2)、恒温下在2L密闭容器中,X、Y、Z三种气态物质的量随时间变化曲线如图。
①该反应的化学方程式为。
②从开始至5min,Y的平均反应速率为。
(3)、已知 , , 根据盖斯定律写出(肼)与完全反应生成氮气和气态水的热化学方程式。(4)、化学能与其他能量间的转换在生活中处处可见,以反应为原理设计成利用率高的燃料电池,装置如图。
M极为电池的(填“正”或“负”)极,N处电极反应式为。
-
20、
I.某化学兴趣小组在教师的指导下,利用如图所示装置(夹持和加热装置已省略)和试剂进行的制备及性质探究的一体化实验。请回答下列问题:

(1)实验开始后,关闭打开 , 加热甲处试管。甲处试管内发生反应的化学方程式为________;乙处瓶内观察到的现象为________;丙处烧杯中的试剂为稀硫酸,丙处球形干燥管的作用是________。
(2)一段时间后关闭 , 打开 , 丁处瓶内发生反应的离子方程式为________;继续反应一段时间后,关闭、 , 打开 , 挤压胶头滴管,己处圆底烧瓶内能观察到的现象为________。
Ⅱ.在实验室里制取的乙烯中常混有少量的 , 某化学兴趣小组设计了如图装置验证该混合气体中含有:和。

(3)装置Ⅱ中反应的化学方程式为________。
(4)能说明气体存在的现象分别是________。
(5)下列操作中,可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中混有的乙烯的是_______。
A. 将气体通入盛有水的洗气瓶中 B. 将气体通入盛有足量溴水的洗气瓶中 C. 将气体通入盛有酸性高锰酸钾溶液的洗气瓶中 D. 将气体通入盛有硫酸的洗气瓶中